L'articolo Fare sterili in Farmacia: cosa serve davvero e normativa sembra essere il primo su Farmagalenica.
]]>Parliamo di fare sterili in farmacia: colliri e/o iniettabili. Cosa serve al Farmacista galenista per poter allestire colliri e/o sterili, qual è la normativa che regola la presenza di una “zona sterili” in una Farmacia con Laboratorio Galenico, quali sono i requisiti strutturali, come organizzarsi?
State per leggere cose che non capirete inizialmente, è normale. Procedete nella lettura e se avete dubbi o domande, postate nei commenti.
Potreste trovarvi, come prima reazione, a rifiutare ciò che è scritto in questo articolo. Per questo l’articolo sarà tecnico e dettagliato per spiegarvi al meglio e farvi capire che “le cose sono effettivamente così”.
Basta con questo alone di mistero e cominciamo.
Colliri e iniettabili: quali differenze nella normativa italiana
La prima cosa da chiarire è qual è la base normativa che regola la produzione dei farmaci sterili (colliri o iniettabili) in una Farmacia Galenica italiana. Ci sono 2 testi:
- le Norme di Buona Preparazione (che molti chiamano “le integrali”)
- le Norme di Buona Fabbricazione (note come GMP o Good Manufacturing Practice)
Già qui potrebbe esserci qualche ciglio aggrottato nel leggere la parola GMP e pensare ad un laboratorio galenico. Ma così è e nel corso dell’articolo verrà ben spiegato con tutti i riferimenti normativi. Come anticipo, considerate comunque che il 90% della normativa per fare sterili in farmacia risiede nelle NBP. Ma quel 10% di GMP (vedrete) è fondamentale e non eludibile.
Bene, chiarito questo partiamo con le cose semplici, cioè chiarire cosa serve al Farmacista Galenista che decide di fare colliri e cosa serve al Farmacista Galenista che decide di fare farmaci iniettabili, ossia ai requisiti strutturali (ambienti, locali, ecc…) e tecnici (procedure, controlli, …).
Quali sono i requisiti strutturali per fare sterili in Farmacia: i colliri
Gli stessi identici degli iniettabili.
Quali sono i requisiti strutturali per fare sterili in Farmacia: gli iniettabili
Gli stessi identici dei colliri
Non è chiaro: quali sono le differenze tecniche e strutturali tra chi vuole fare colliri o iniettabili in Farmacia?
Immaginando un po’ di confusione e stordimento nella testa del lettore fin qui, diamo risposta chiara, precisa e concisa alla domanda sopra:
NESSUNA
[OK…]
Si, avete letto bene. Non c’è NESSUNA DIFFERENZA strutturale e legislativa per un Farmacista Galenista che voglia fare colliri sterili o iniettabili sterili. Nessuna significa… nessuna.
FERMI TUTTI: stiamo forse dicendo che se voglio fare colliri galenici devo avere una camera bianca o comunque un isolatore?
Sì.
Si.
Si.
Detto in altra maniera:
Se nel laboratorio galenico non si ha la camera bianca o stanza almeno ISO 8 con isolatore NON PUOI FARE STERILI: COLLIRI O INIETTABILI.
NBP XII ed.. Dal 2002

Impossibile! Sono anni che ho SOLO la cappa per colliri e non ho mai avuto problemi!
Tutto va bene finché va bene.
Proverbio di anonimo autore nel 2024
È normale il rifiuto di quanto sopra, cercando risposte dalla prassi quotidiana:
- “Ma nessuno mi ha mai contestato nulla”
- “Faccio così da sempre e non ho mai avuto problemi” (questa è un evergreen :P)
- “Ma la norma prima non era così! È cambiata recentemente?”
- “Figuriamoci se serve la camera bianca per fare 2 colliri ogni tanto”
- “Al corso di galenica di XYZ mi hanno detto che bastava la cappa”
- “L’azienda ABC mi ha detto che con la cappa posso fare i colliri o iniettabili non endovena”
- “mio cuggino mi ha certificato gli ambienti che ho fatto fare a un amico”
Lo spirito di queste risposte è alla base di quanto successe nel 2013 in America, il cosiddetto “scandalo NCCD“: anche in America i galenici sterili venivano fatti da alcune farmacie in maniera non adeguata (es. senza camera bianca, senza tutte le procedure necessarie, senza seguire i requisiti strutturali e procedurali) in seguito del quale vi furono 64 morti (!) e centinaia di malati (es. meningite).
Come conseguenza a questa scandalo, la FDA Americana modificò le normative sullo sterile in maniera molto più stringente, di fatto ridimensionando e ridisegnato il modo di fare sterile: escludendo la maggior parte delle farmacie.
In Italia? Se succedesse in Italia, guardando a cosa è capitato in casi simili in passato (es. sospette morti per preparazioni galeniche anoressizzanti) si potrebbe ipotizzare, probabilmente, la chiusura dell’attività sterile nelle farmacie galeniche italiane o, in alternativa, l’istituzione di farmacie centralizzate controllate pesantemente da AIFA. Davvero vogliamo questo?
La paura dell’Autore è che sia solo questione di QUANDO (e non di SE) succederà un evento disastroso in Italia nella galenica sterile. Quanto scritto in questo articolo ha anche lo scopo di sensibilizzare il più possibile, promuovere conoscenza (e coscienza), proteggere i pazienti.
Non ci credo! Sono anni che ho SOLO la cappa colliri e nessuno mi ha mai contestato nulla!
Stiamo parlando di avere uno scenario in cui un farmacista ha installato una cappa colliri in un qualsiasi ambiente del laboratorio o comunque senza le indicazioni delle GMP? Qui tocchiamo un tasto parecchio dolente. Come già scritto, la norma sugli sterili è del 2002 (oltre 20 anni dalla data di pubblicazione di questo articolo).
Com’è possibile che in tutto questo tempo non si sia sviluppato una corretta impostazione normativa del laboratorio, ma che ci siano numerose farmacie che eseguono colliri in queste condizioni?
Alcune possibili risposte (alcune politicamente scorrette forse, ma la verità va detta):
- fino a qualche anno fa, lo sterile non se lo filava nessuno

- oltre l’85% (fonte) delle farmacie segue le “NBP semplificate” (DM 2003) e probabilmente non ha mai veramente letto le NBP integrali, dato che il DM 2003 non tratta (e non permette, v. già avanti) la preparazione di galenici sterili
- chi si occupa di verifiche e ispezioni non ha comunque quell’attenzione / approfondimento nel valutare la normativa, tenendo conto che lo sterile oltre alle NBP richiede anche una minima conoscenza delle GMP
- chi vende “cappe per colliri” (certificate?) a un farmacista non è tenuto a sapere cosa quel farmacista ne farà, come la userà. Il venditore è a posto. La responsabilità finale è del Farmacista Galenista.
Da dove nasce l’idea che in farmacia si possano fare colliri senza ambienti previsti dalle NBP?
Con questa domanda ci riferisce al luogo comune per cui “per fare i colliri basta una cappa per colliri”, senza ambienti dedicati A-B-C-D.
Probabilmente, l’equivoco nasce dall’idea che essendo consentito dal Dlgs 16/2010 e succ. mod. in ambienti oculistici avere un ambiente D con all’interno una cappa per colliri, si sia “traslato” questa possibilità anche alla farmacia.
Ora, posto che tale norma nulla ha a che vedere con le farmacie, per i laboratori galenici esiste una specifica normativa (NBP) che descrive esattamente e precisamente quali sono i requisiti per eseguire preparazioni sterili (senza distinguere tra colliri o iniettabili o altro) in un laboratorio galenico.
Dulcis in fundo, la norma dei colliri citata all’inizio prevede comunque che la cappa per i colliri sia una clean room zona D (almeno ISO 8), e non che sia genericamente posizionate in un punto del laboratorio o in una stanza normale, seppur dedicata, senza classificazione ISO.
Le cappe a flusso laminare per sterili (colliri o iniettabili) NON sono le cappe di sicurezza o cappe biologiche!
Sì, c’è bisogno di chiarirlo.
Le NBP per gli sterili in Farmacia, spiegate bene
Adesso entriamo nello specifico. Facciamo nomi delle leggi, riferimenti ai punti, ecc…
Come già detto, la norma che regola la preparazione di farmaci sterili in farmacia nel Laboratorio Galenico sono le Norme di Buona Preparazione, in particolare i paragrafi da pagina 1417 a 1426.
In queste (poche) pagine le NBP descrivono le cose necessarie da fare per garantire la sterilità e quindi la sicurezza del farmaco e, di conseguenza, la sicurezza del paziente. Queste descrizioni dicono COSA serve, ma non COME farlo. Questo punto è importantissimo.
Ma allora possiamo interpretare? Può essere che una cappa colliri sia sufficiente per fare sterili in farmacia?
Ci sono 2 (DUE) specifiche e precise eccezioni a quanto appena affermato sopra: sono 2 punti in cui le NBP sostanzialmente dicono COME fare una determinata cosa non spiegandolo direttamente, ma indicando come riferimento le GMP.
In altre parole, quando nel 2002 usci la Farmacopea Italiana XII edizione, le NBP davano indicazioni di seguire alcune parti del GMP del 2002. Nel 2024 le NBP della Farmacopea Italiana XII edizione non sono cambiate (sic!), ma sono cambiate le GMP e l’Annex I (Agosto 2023 è l’ultimo aggiornamento alla data del presente articolo). Quindi:
- NBP sempre quelle dal 2002
- GMP cambiano nel corso degli anni
Venendo al dunque, sono 2 i punti in cui le NBP “rinunciano” a dare riferimenti e indicano invece di fare riferimento diretto alle GMP, nello specifico l’Annex I (o Allegato I):
- quando si parla di locali in cui fare preparazioni sterili
- quando si parla di limiti microbiologici
Ambienti in cui fare sterili in Farmacia: NBP e GMP
Gli ambienti di preparazione devono essere separati dagli altri locali di preparazione. Gli ambienti dovranno essere classificati secondo il grado di rischio del processo impiegato in conformità all’Allegato 1, Fabbricazione di medicinali sterili, delle Norme di Buona Fabbricazione [GMP, ndr]
Paragrafo 11.1.2 – pag. 1423
Cos’è l’Allegato 1? Nel settore è meglio noto come Annex I (leggasi “Annex primo”) ossia un allegato tecnico in cui sono contenute tantissime informazioni dirette o indirette su sterilità, locali, procedure, personale, strumenti, limiti, test, analisi, metodiche.
Di tutta questa roba  quello che interessa in questo paragrafo delle NBP sono i riferimenti ai locali che le GMP classificano in base alle ISO:
quello che interessa in questo paragrafo delle NBP sono i riferimenti ai locali che le GMP classificano in base alle ISO:
- Zona A: semplificando, la cappa a flusso laminare [nota tecnica: deve essere almeno una ISO 4.8]
- Zona B: zona è in cui è presente la cappa a flusso laminare [nota tecnica: deve essere almeno una ISO 7]
- Zona C: zona di vestizione, filtrazione, autoclave, preparazioni ad alto rischio [nota tecnica: deve essere almeno una ISO 7]
- Zona D: zona di lavoro delle preparazioni a basso rischio [nota tecnica: deve essere almeno una ISO 8]
In base all’Annex I (e quindi anche alle NBP) tutte queste zone devono:
- essere in sovrapressione una con l’altra (dall’ISO minore all’ISO maggiore)
- avere sistemi di apertura che impediscano la contemporanea apertura di più porte
- avere sistemi di controllo per regolazione e controllo della pressione
- ecc
Tutto questo requisito delle NBP/Annex I si può ottenere in un laboratorio galenico solo in 2 modi:
- tramite una camera bianca (con 4 ambienti, ulteriori informazioni)
- tramite un dispositivo detto “isolatore” (ulteriori informazioni) che permette di ottenere 3 ambienti (A-B-C), ma no il 4° motivo per il quale va installato in una clean room (stanza) classificata D (es. ISO 8).
ISO: cosa sono? Camera bianca o isolatore?
Abbiamo parlato finora di ISO, ma non abbiamo spiegato esattamente cosa sono e a cosa si riferiscono nel campo degli ambienti sterili.
La ISO (International Organization for Standardisation) è la più grande istituzione a livello mondiale per lo sviluppo e la pubblicazione di norme internazionali. Con riferimento alla qualità o purezza dell’aria.
La seguente tabella spiega in maniera precisa i valori di particelle ammesse in un determinato ambiente e la relativa classificazione in ISO:
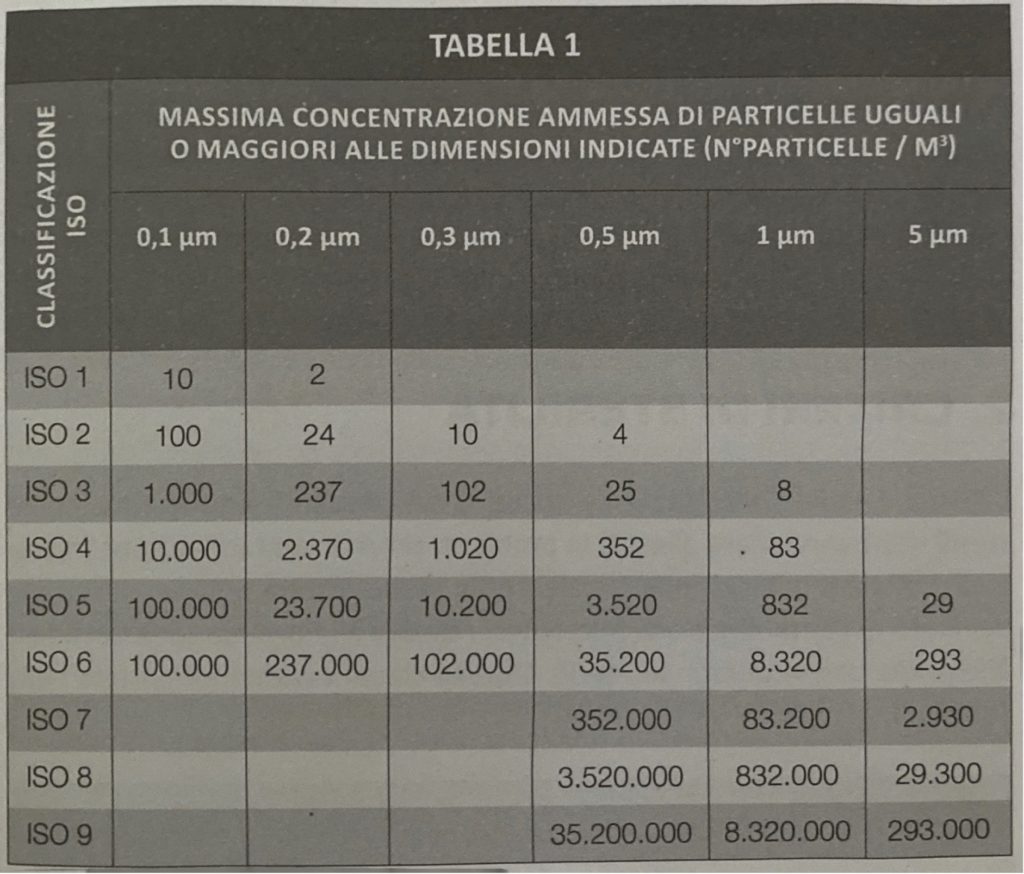
Sembrerà un ripetizione, ma: ribadiamo la differenza dal punto di vista delle zone tra camera bianca (“clean room”) e isolatore:
- la “camera bianca” è un insieme di stanze collegate tra loro classificate con gli ISO in base al tipo di lavorazione da eseguire. Sono MOLTO costose.
- gli isolatori sono macchinari che dispongono delle zone A-B-C. Sono costosi, ma meno di una camera bianca.
Al lettore attento non sarà sfuggito un fatto: un isolatore, per essere a norma, deve essere collocato in una zona D, ossia ISO 8. Ergo, collocare un isolatore in un punto qualunque del laboratorio non permette al Farmacista Galenista di allestire farmacia galenici sterili (colliri o iniettabili), ma è necessario un ambiente isolato e certificato in base all’Annex I.
Limiti microbiologici per gli sterili in farmacia: NBP e GMP
I controlli dovranno essere definiti da un apposito piano di campionamento commisurato agli ambienti e al loro utilizzo, che riporti i punti di prelievo, il numero dei saggi, le frequenze dei controlli, le metodiche utilizzate, le azioni previste al superamento dei valori limite. Per i valori limite l’attuale riferimento è costituito dall’Allegato 1, Fabbricazione di medicinali sterili, delle Norme di Buona Fabbricazione [GMP, ndr]
Paragrafo 11.4 – pag. 1424
Anche in questo caso, le NBP indicano che le “istruzioni precise” sui limiti microbiologici sono da “prendere” nell’Annex I. Il Farmacista Galenista ha l’obbligo di eseguire test sul farmaco, l’ambiente e le procedure. E i limiti di accettabilità di questi test sono nelle GMP (Annex I):

Le GMP sono GMP. Le NBP sono NBP.
Attenzione però alle derive: nello sterile nel laboratorio Galenico della Farmacia NON è obbligatorio seguire tutte le GMP per la preparazione degli sterili (colliri o iniettabili): l’obbligo perentorio è SOLO per i 2 punti specifici dell’Annex I descritti in questo articolo richiamati dalle NBP.
Su tutto il resto, il Farmacista deve seguire le NBP che danno indicazioni generali (ma che richiedono sempre di documentare) su come condurre le gestione dello sterile.
Ciò detto, se il Farmacista Galenista volesse indicazioni meno generali di quelle NBP, preferendo indicazioni chiare e precise può scegliere di attingere all’Annex I delle GMP.
Davvero non c’è altra interpretazione delle NBP per poter fare dei semplici colliri sterili in farmacia?
Davvero. Non c’è.
Ma ammettiamo che ci sia. Solo per un attimo, facciamo (molto) finta che quanto avete letto finora non sia vero. C’è un’altra cosa da considerare nelle NBP: le “semplificate”.
Se sei un Farmacista Galenista, prima di proseguire rispondi a questa domanda: nel laboratorio galenico in cui lavori segui le “semplificate” o le “integrali”? Risposto? Ok, ora continua.
Le norme di seguito descritte [NPB “integrali”, ndr] si applicano alle preparazioni, magistrali o officinali, eseguite in farmacia, sia essa aperta al pubblico che ospedaliera.
CAMPO DI APPLICAZIONE delle NBP – pag. 1417
La farmacia che esegue preparati officinali non sterili su scala ridotta e preparati magistrali non sterili può discostarsi in parte da quanto descritto nei paragrafi che seguono, purché sia in grado di mantenere sotto controllo, dimostrandolo [DM 2003, ndr], l’intero processo.
Avete già capito vero? Chi vuol fare sterili di qualsiasi tipo, PRIMA ANCORA DI RAGIONARE DI CAMERA BIANCA o ISOLATORE, DEVE (imperativo) obbligatoriamente seguire le NBP “integrali“.
Non è legalmente consentito fare colliri o iniettabili in laboratorio galenico se si seguono le norme “semplificate” (DM 2003).
Alla data di pubblicazione dell’articolo, risultano censite circa 2.200 farmacie che fanno preparazioni galeniche, di cui oltre l’85% segue le semplificate ergo non può fare sterili.
Riassumendo:
- semplificate con cappa colliri da qualche parte nel laboratorio? Non a norma
- integrali con cappa colliri da qualche parte nel laboratorio? Non a norma
- integrali con cappa colliri in camera bianca o isolatore in zona D? Legale
Concludiamo ricordando che questo articolo non è una guida allo sterile nel Laboratorio Galenico, per cui c’è molto molto altro da conoscere per chi vuole fare galenici sterili, siano essi colliri o iniettabili.
Da dove partire quindi? Ovvio, dalle NBP (integrali) della Farmacopea Italiana. Leggetele (potete scaricarle da qui sotto).
Se invece volete un “riassunto” con slide che spiegano l’Annex I (anche se in versione datata), in particolare le caratteristiche delle zone A-B-C-D, ecco un link molto utile.
Alla prossima!

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Fare sterili in Farmacia: cosa serve davvero e normativa sembra essere il primo su Farmagalenica.
]]>L'articolo Semaglutide galenica: preparazione in farmacia e brevetto sembra essere il primo su Farmagalenica.
]]>In breve, questa modifica permette al Farmacista di realizzare farmaci galenici utilizzando materie prime coperte da brevetto acquistate da rivenditori terzi con lo scopo di ottenere un prodotto personalizzato rispetto a quanto presente sul mercato farmaceutico.
Per meglio spiegare la portata della modifica normativa, in questo articolo si prenderà a titolo di esempio la molecola semaglutide (principio attivo contenuto in farmaci quali Ozempic® o Wegovy®).
Ad oggi, non sono infatti tante le molecole farmaceutiche rimaste coperte da brevetto per le quali la modifica introdotta dal Legislatore possa avere concretezza.
Si legga a proposito questa intervista al Dr. Marco Ternelli sull’argomento.
Essendo materia farmaceutica recente, si rimanda al seguente disclaimer: le informazioni contenute nel presente articolo hanno carattere generale e non sono da considerarsi un esame esaustivo e corretto né intendono esprimere un parere o fornire una consulenza di natura legale. Le considerazioni e opinioni di seguito riportate non prescindono dalla necessità di ottenere pareri specifici con riguardo alle singole fattispecie descritte.
Nota: non essendo scaduto il brevetto della semaglutide, non esiste ancora il generico (farmaco industriale) corrispondente.

L’eccezione galenica e la protezione brevettuale
Nel 1979, con il DPR 338 veniva introdotta la cosiddetta “eccezione galenica” e a seguito, dopo diversi anni, anche una modifica alla norma che di fatto rendeva impossibile per il Farmacista Galenista utilizzare materie prime coperte da brevetto (a meno di non sintetizzarle nel laboratorio galenico).
Tale modifica venne introdotta con l’art. 68, comma 1 lett. c) del Codice della Proprietà Intellettuale che recita(va):
“La facoltà esclusiva attribuita dal diritto di brevetto non si estende, quale che sia l’oggetto dell’invenzione: [omiss] alla preparazione estemporanea, e per unità, di medicinali nelle farmacie su ricetta medica, e ai medicinali così preparati, purché non vengano utilizzati principi attivi realizzati industrialmente“
art. 68, comma 1 lett. c) del Codice della Proprietà Intellettuale
In parole semplici: “Farmacista Galenista! Va bene, puoi non rispettare il brevetto purchè ti sintetizzi il principio attivo da solo nel laboratorio galenico!”. Ovviamente, impossibile nel 99.999% dei casi.
Nel 2023, con la Legge annuale per il mercato e la concorrenza 2022 pubblicata in GU n. 303 del 30/12/23 in vigore dal 31/12/23 tale comma è stato modificato, abolendo le parole
“purché non si utilizzino principi attivi realizzati industrialmente“
parte di testo abolita con la Legge annuale per il mercato e la concorrenza 2022
permettendo di fatto al Farmacista Galenista di acquistare materie prime coperte da brevetto da grossisti autorizzati, senza doverlo per forza sintetizzare in laboratorio.
Una bellissima e completa disamina di quali erano i limiti per il Farmacista presenti con l'”eccezione galenica” sono riportati in questo articolo dello Studio legale Pandolfini.
Semaglutide in Italia e brevetto
Nella stesura di questo articolo si è preso come esempio la sostanza semaglutide, principio attivo ancora sotto copertura brevettuale, contenuto nel farmaco Ozempic® che ha come indicazione terapeutica il controllo della glicemia nei pazienti diabetici.
In Italia NON è invece in commercio (alla data di pubblicazione del presente articolo) a Luglio 2024 è entrato in commercio il medicinae industriale il Wegovy®, farmaco sempre a base di semaglutide ma con l’indicazione terapeutica per il controllo (e perdita) del peso corporeo.
Il principio attivo LIRAGLUTIDE (non semaglutide!) non è più soggetto a protezione brevettuale dal 2021 e nulla ha a che vedere con quanto riportato nel presente articolo.
In ogni caso, l’argomento è la possibilità di utilizzare la semaglutide nella preparazione galenica, indipendentemente dall’indicazione terapeutica per realizzare farmaci personalizzati per il paziente.
Semaglutide galenica: caratteristiche intrinseche
Il Farmacista Galenista ha dunque la possibilità di ottenere la materia prima purissima di grado farmaceutico e utilizzarla per la preparazione di farmaci galenici.
Questa norma renderà più facilmente accessibile ai pazienti preparati magistrali personalizzati contenenti sostanze ancora coperte da brevetto poiché consente al Farmacista Galenista di acquistare la sostanza purissima da fornitori autorizzati e non necessariamente dall’azienda detentrice del brevetto.
Attenzione: l’eccezione galenica permette al Farmacista di realizzare un galenico solo con ricetta medica e solo per specifiche esigenze. È vietato realizzare un “mercato parallelo” di galenici arrecando un danno all’azienda detentrice del brevetto.
Cosa significa di fatto tutto questo? Tante possibilità, quali:
- avere diverse forme farmaceutiche: iniettabile, compresse, ma anche capsule, liquido (gocce o sciroppo), ecc…
- avere (teoricamente) qualsiasi dosaggio: esempio 0,4 mg/ml, 1 mg/ml, per rendere somministrabile un volume inferiore o maggiore di liquidi o ricalibrando la dose in base a concomitanti patologie di cui il paziente è affetto
- possibiltà di rimuovere un eccipiente cui il paziente è intollerante o allergico, permettendo quindi di somministrare il farmaco
- accesso al farmaco: in caso di carenza sul territorio nazionale, la Galenica permette al paziente di non interrompere (o di iniziare) le terapie continuando a somministrare il medicinale, evitando pericolose ripercussioni sulla salute dei pazienti

Normativa per la vendita della semaglutide galenica
Per la vendita della semaglutide galenica è richiesta una ricetta medica che può essere redatta da QUALSIASI Medico (specialista, non specialista, di medicina generale, ecc…). Tale ricetta cambia requisiti e durata a seconda delle indicazioni terapeutiche per cui è prescritta, qui di seguito riassunte.
E’ esclusiva e assoluta prerogativa del Medico sapere l’indicazione terapeutica per cui un galenico viene prescritto, come descritto in questo articolo.
Indicazioni terapeutiche dimagranti
Nel caso di prescrizione di semaglutide galenica ad uso dimagrante, il riferimento di Legge è il DM 31 Marzo 2017 che indica i precisi formalismi che una ricetta medica galenica ad uso dimagrante deve avere, indipendentemente dalla sostanza o forma farmaceutica.
La ricetta in questo caso è ripetibile e vale 6 mesi per un massimo di 10 volte.
Il Farmacista Galenista deve inviare mensilmente copia della ricetta alla sua AUSL.
Per rendere meglio chiaro il concetto, si allega un facsimile di ricetta di semaglutide galenica redatta con formalismi ad uso dimagrante.
Indicazioni terapeutiche off label
Nel caso di prescrizione di semaglutide galenica off label (non a uso dimagrante), il riferimento normativo è l’art. 5 della Legge 94/98 (Legge di Bella) che prevede i seguenti formalismi:
- indicazione di un codice numerico o alfanumerico al posto del nome e cognome
- le particolari esigenze che giustificano il ricorso alla preparazione estemporanea (“motivazione della prescrizione”)
La ricetta in questo caso è non ripetibile, vale 30 giorni escluso quello di emissione per il numero di confezioni indicato dal Medico (solitamente 1).
Il Farmacista Galenista deve inviare mensilmente copia della ricetta alla sua AUSL.
Per rendere meglio chiaro il concetto, si allega un facsimile di ricetta di semaglutide galenica redatta con formalismi ad uso dimagrante.
Indicazioni terapeutiche autorizzate
Nel caso di prescrizione di semaglutide galenica in label (per indicazioni terapeutiche autorizzate diverse dal dimagrante, es. trattamento diabete), il riferimento normativo è sempre la Legge 94/98 (Legge di Bella) che prevede i seguenti formalismi:
- (auspicabile) nome e cognome del paziente
- principio attivo (es. semaglutide)
- dosaggio (es. 0,45 mg/ml)
- quantità da produrre (es. 3 ml)
- (non obbligatorio) posologia
La ricetta in questo caso è ripetibile e vale 6 mesi per un massimo di 10 volte.
Per rendere meglio chiaro il concetto, si allega un facsimile di ricetta di semaglutide galenica redatta con formalismi per indicazioni terapeutiche in label.
Brevetti, tempi e fattibilità
Così come il Farmacista non può decidere liberamente il prezzo dei farmaci industriali (come Ozempic® o Wegovy®), altrettanto non è libero di decidere liberamente il costo di un medicinale galenico, ma deve attenersi alla Tariffa Nazionale dei Medicinali che impone prezzi fissi.
In base (ma non solo) al tipo di forma farmaceutica e al costo della materia prima, il Farmacista determina il prezzo del medicinale galenico. Come da normativa, la Tariffa deve essere messa a disposizione del paziente che ne faccia richiesta per poter verificare il corretto calcolo del prezzo.
Al fine di agevolare questo requisito di legge, ecco alcuni esempi di prezzi della semaglutide galenica ricordando che possono variare di molto in base
- al costo di partenza della materia prima
- al costo delle penne con cartuccia
- alla quantità prodotta (es. 1 ml avrà un costo maggiore di 3 ml poiché i costi fissi sono gli stessi)
Esempi (ATTENZIONE, sono prezzi indicativi che possono variare, nonostante la Tariffa, al variare del costo della materia prima):
- semaglutide 0,4 mg/ml, cartuccia da 1.5ml = 98,45€
- semaglutide 2,5 mg/ml, cartuccia da 1.5ml = 165,12€
La preparazione può avvenire solo in alcune farmacie Galeniche (tra cui alcune di Farmagalenica) dotate di laboratorio galenico con camera bianca.
Ad oggi però, il principio attivo come tale non è reperibile, pertanto non risultano farmacie di Farmagalenica in grado di allestire preparazioni galeniche con sostanze coperte da brevetto come per la semaglutide galenica descritta finora.

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Semaglutide galenica: preparazione in farmacia e brevetto sembra essere il primo su Farmagalenica.
]]>L'articolo Come fa il Farmacista a capire quando serve la “Di Bella” in Galenica? sembra essere il primo su Farmagalenica.
]]>Oggi finalmente scopriremo la risposta a questa domanda che attanaglia la maggior parte dei Farmacisti Galenisti: quando il Farmacista ha una ricetta medica che prescrive un galenico magistrale, come fa il a capire se serve la “Di Bella”?
Traduzione per il lettore non Farmacista: come fa il Farmacista a capire se la ricetta del galenico magistrale va bene così com’è o se il Farmacista deve richiedere al Medico di cambiarla?
ATTENZIONE: questo è un articolo che darà delle risposte (“E finalmente!” direte). E alcune NON VI PIACERANNO (“Ah!” direte). Ad alcuni faranno chiudere la pagina senza arrivare in fondo. Ad altri farà scuotere la testa. Ad altri cadere la mascella. Ad altri lasciarli affascinati.
Ecco, spero che la maggior parte di voi lettori appartenga all’ultima categoria.
È come un film in cui c’è il colpo di scena finale, e al termine potrete rileggere l’articolo sapendo già come va a finire e quindi capire come fare a capire quando serve la “Di Bella”.
Solo che il colpo di scena in questo articolo è all’inizio.
Dritti al punto: come fa il Farmacista a capire quando serve la “Di Bella” in una ricetta galenica?
Ecco la risposta:
NON PUO’!
Fine. Fin. The end.
…
…
Siete ancora lì? Gira la testa? Se vi sentite presi in giro è normale, solo leggendo e imparando quando segue potrete capire. 
Diamo una spiegazione veloce per non tenerla troppo lunga, ma approfondiremo nel corso di questo articolo: il Farmacista Galenista non può in alcun modo sapere se serve la “Di Bella” perché… quello è un compito professionale del Medico. Non del Farmacista.
Ma andiamo con ordine.
Primo errore: la domanda “Di Bella”
Come accennato all’inizio, quando il Farmacista si chiede “come fa il Farmacista a capire quando serve la “Di Bella”?” intende dire (spoiler: sbagliando) come fare a capire se la ricetta
- è prescritta per indicazioni terapeutiche autorizzate o off label (al di fuori delle indicazioni terapeutiche autorizzate)
- deve contenere un codice numerico o alfanumerico al posto del nome e cognome
- deve riportare la motivazione della prescrizione
In base a questa risposta, il Farmacista Galenista deciderà se la ricetta che ha in mano è da ritenersi valida oppure no.
Bene, il punto fondamentale della “come fa il Farmacista a capire quando serve la “Di Bella”?” è che essa è formulata erroneamente.
QUALSIASI ricetta che prescrive un galenico (magistrale) è una ricetta redatta secondo la Legge “Di Bella” (94/98)
Legge 94/98
In altre parole: la Legge 94/98 (“Di Bella”) è la normativa che dal 1998 regola qualsiasi prescrizione di un galenico redatta da un Medico. Dire “Serve la Di Bella?” significa non sapere bene di cosa si sta parlando perché la “Di Bella” serve sempre, per qualsiasi ricetta galenica.
Per capirci sul termine qualsiasi:
- prescrizione di vaselina salicilica 3.2% = ricetta redatta secondo la Legge Di Bella.
- prescrizione di acqua di calce = ricetta redatta secondo la Legge Di Bella.
- prescrizione di alcool borico = ricetta redatta secondo la Legge Di Bella.
- prescrizione di capsule di fagiolo bianco = ricetta redatta secondo la Legge Di Bella.
- prescrizione di capsule di paroxetine = ricetta redatta secondo la Legge Di Bella.
Chiaro? No? Ok, ci sta.
Secondo errore: cos’è DAVVERO la “Di Bella”?
A questo punto del percorso diversi dovrebbero già avere capito che c’è un grosso misunderstanding (mi spingo a dire una delle tante leggende metropolitane che troppo spesso si incontrano in galenica) su cosa sia la Legge “Di Bella” e cosa dica davvero.
Prima di iniziare: per chi vuole dare una lettura integrale alla legge di “Di Bella”, il link è questo.
1998: nasce la Di Bella
Una brevissima storia di come è nata la Legge 94/98: dovete tornare alla memoria al 1998 (i più giovani possono usare Google), quando in virtù della terapia antitumorale inventata dal Professor Luigi Di Bella si rese necessario regolamentare la prescrizione di farmaci galenici realizzate dal Farmacista Galenista e allo stesso tempo tracciare e capire quello che veniva preparato.
Semplificando molto, lo scopo della legge “Di Bella” era di definire:
- quali sostanze possono essere utilizzate all’interno di una preparazione Galenica
- le modalità da seguire nell’utilizzo in-label o off-label di una formulazione Galenica
- le modalità operative di comportamenti per il medico e il farmacista davanti ad una prescrizione Galenica
Per farlo è necessario un breve e LEGGERO (promesso) ripasso e lettura di alcuni passaggi della Legge 94/98, per spiegare e capire questo argomento su Farmagalenica, con esclusivo riferimento alle parti relative alla galenica (vale a dire che sono escluse le parti che trattano i farmaci industriali presenti all’interno della Legge).

Il Medico
L’articolo che interessa la galenica è l’articolo 5.
Di questo articolo, considerate i seguenti 3 commi:
Fatto salvo il disposto del comma 2, i medici possono prescrivere preparazioni magistrali esclusivamente a base di principi attivi descritti nelle farmacopee dei Paesi dell’Unione europea o contenuti in medicinali prodotti industrialmente di cui e’ autorizzato il commercio in Italia o in altro Paese dell’Unione europea. La prescrizione di preparazioni magistrali per uso orale puo’ includere principi attivi diversi da quelli previsti dal primo periodo del presente comma, qualora questi siano contenuti in prodotti non farmaceutici per uso orale, regolarmente in commercio nei Paesi dell’Unione europea; parimenti, la prescrizione di preparazioni magistrali per uso esterno puo’ includere principi attivi diversi da quelli previsti dal primo periodo del presente comma, qualora questi siano contenuti in prodotti cosmetici regolarmente in commercio in detti Paesi. Sono fatti in ogni caso salvi i divieti e le limitazioni stabiliti dal Ministero della sanita’ per esigenze di tutela della salute pubblica.
Art. 5, comma 1 – Prescrizione di preparazioni magistrali
E poi:
3. Il medico deve ottenere il consenso del paziente al trattamento medico e specificare nella ricetta le esigenze particolari che giustificano il ricorso alla prescrizione estemporanea. Nella ricetta il medico dovrà trascrivere, senza riportare le generalita’ del paziente, un riferimento numerico o alfanumerico di collegamento a dati d’archivio in proprio possesso che consenta, in caso di richiesta da parte dell’autorita’ sanitaria, di risalire all’identità del paziente trattato.
Art. 5, comma 3 – Prescrizione di preparazioni magistrali
E ancora:
5. Le disposizioni dei commi 3 e 4 non si applicano quando il medicinale e’ prescritto per indicazioni terapeutiche corrispondenti a quelle dei medicinali industriali autorizzati a base dello stesso principio attivo.
Art. 5, comma 5 – Prescrizione di preparazioni magistrali
Come avete notato dalle evidenziazioni, qui si parla di una figura professionale ben precisa, il Medico. Chirurgo. La Legge è chiarissima nel riferirsi a lui solo come figura. Il termine “Farmacista” non compare mai.
In questi commi, vengono date istruzioni su come compilare la ricetta medica, sugli adempimenti e le relative indicazioni terapeutiche.
E ora vi domando: in questo scenario chi è la persona che può sapere qual è la patologia del paziente, qual è il principio attivo da usare e se questo è utilizzato secondo le indicazioni terapeutiche (in-label) o no (off label)?
Qual è la risposta? Spero vi venga ovvia, ossia IL MEDICO! Solo lui! È il suo mestiere fare diagnosi e da essa identificare una patologia per poi scegliere il trattamento più idoneo.
OK. Frenate gli entusiasmi! Potrebbe essere che state cominciando a mettere fuoco o addirittura ci siete già arrivati, ma pazienza ancora! Mettete da parte tutto questo e andiamo avanti ancora un poco. Non è finita.
Il Farmacista
L’articolo 5 della Legge 94/98 contiene altri due commi, ma questa volta riferiti ad un altro attore:
4. Le ricette di cui al comma 3, in originale o in copia, sono trasmesse mensilmente dal farmacista all’azienda unità sanitaria locale o all’azienda ospedaliera, che le inoltrano al Ministero bla bla…
Art. 5, comma 4 – Prescrizione di preparazioni magistrali
E poi:
6. La violazione, da parte del medico o del farmacista, delle disposizioni del presente articolo è oggetto di procedimento disciplinare bla bla..
Art. 5, comma 6 – Prescrizione di preparazioni magistrali
Questi sono gli unici due commi della Legge di Bella (94/98) in cui compare quest’altra figura professionale completamente diversa (e c’era bisogno di dirlo?) dal Medico: il FARMACISTA.
È tutto qui.
Quando il Farmacista Galenista ricetta una ricetta medica galenica, cosa deve fare e come farlo è scritto nel comma 4: quando il Farmacista, grazie ai suoi occhi, vede
- che sulla ricetta al posto del nome cognome è presente un codice numerico alfanumerico
- e che è anche presente la particolare esigenza che giustifica ricorso alla preparazione estemporanea (nota ai più come “motivazione della prescrizione”)
ecco che allora E SOLO ALLORA deve seguire degli adempimenti previsti per le preparazioni off-label.
Adempimenti del Farmacista, ossia: cosa FA il Farmacista quando ha una ricetta off label (ex “una ricetta con la Di Bella”)
Il Farmacista saprà che quella ricetta che ha in mano è off-label (perché ha riportato il codice + motivazione della prescrizione) e che quindi:
- la ricetta è non ripetibile e ha validità di 30 giorni escluso quello di emissione (nota della Tabella 5 della FUI Italiana)
- ne invia una copia all’AUSL regionale
Tutto qui.
Davvero.
Non c’è altro.

E se il Farmacista ha un dubbio, come fa capire quando serve la “Di Bella”?
Siamo al gran finale. La risposta delle risposte!
In altre parole: “Io Farmacista Galenista ho una ricetta normale, scritta con “nome e cognome”, senza motivazione della prescrizione, ma ritengo (oppure ho il dubbio) che per il motivo XYZ vada o dovrebbe essere prescritta come off-label.”
Ehm… se avete questa domanda non avete capito nulla. Pardon! Volevo dire che non mi sono spiegato bene. 
Riprovo.
Abbiamo capito (e accettato) che il Farmacista se ne deve frega… ehm… non deve (non può!) entrare nel merito dell’indicazione terapeutica.
FERMI! Ipotizziamo però che il Farmacista lo faccia, cioè che si metta a pensare che forse sarebbe bene o necessario (??) che la ricetta che ha in mano fosse compilata come fosse un off-labe; e magari anche contestare e pure rifiutarsi di spedire (significa “preparare”) una ricetta perché ritenga, appunto, che la ricetta che ha in mano debba davvero essere fatta con la Di Bella.
Scrupoloso il Farmacista, eh?
Peccato che così facendo commetta (almeno) un reato. Art. 348 del Codice Penale: abuso di professione medica.
Già, perché posto che la ricetta sia formalmente corretta e che il Farmacista abbia seguito tutte le norme obbligatorie previste (es. controllo assenza iperdosaggi e verifica di assenza di incompatibilità chimico – fisiche), cimentarsi nel valutare se il principio attivo è prescritto secondo le indicazioni terapeutiche o meno significa che il Farmacista deve fare una diagnosi (!) e ritenere che il principio attivo prescritto non sia conforme per quella condizione (patologia).
Quindi, gran finale:
- cosa il Farmacista Galenista deve fare per capire se la ricetta galenica richiede la prescrizione off-label è scritto chiaramente nei commi dell’art. 5 della Legge 94/98 (“Di Bella”) ed è di competenza sempre e solo del Medico.
- se il Farmacista Galenista per qualsiasi motivo ritenesse che una ricetta galenica in-label debba essere in realtà prescritta come off-label, si sta sostituendo al Medico e commette abuso di professione medica.
Ma il Medico come fa a sapere se esiste o meno una indicazione terapeutica autorizzata?
La legge “Di Bella” è chiarissima nel dire cosa deve fare il Farmacista e quando deve farlo. Non dà alcun potere al Farmacista Galenista di ragionare, interpretare o sindacare se la ricetta sia o meno off-label, ma identifica i due elementi fisici e oggettivi (il codice numerico/alfanumero e la motivazione della prescrizione) come formalismi che il Farmacista Galenista deve utilizzare per adempiere ai suoi doveri di Legge.
Che una ricetta galenica sia off label o meno, quindi, dipende solo ed esclusivamente da come il Medico la compila e dal fatto che riporti un formalismo (es. codice alfanumerico) piuttosto che un’altro (nome e cognome del paziente).
È tutto giustamente solo ed esclusivamente nella mani del Medico
E la domanda successiva: si ma, come fa il Medico a sapere se in Italia o in Europa esiste un Medicinale contenente il principio attivo con l’indicazione terapeutica desiderata?
Risposta non politicamente corretta: ma lo saprà bene il Medico, no?
Risposta politicamente corretta: il Medico
- che conosce la professione
- conosce gli studi disponibili
- che ha conoscenze personali
- che sa consultare banche dati italiane o di singoli Paesi Europa
saprà se quel che cerca esiste, cioè se esiste una indicazione terapeutica approvata. Da cui ne deriva ovviamente che
se il Medico emette una ricetta Medica con le indicazioni terapeutiche in-label è perché sà che può farlo perché sà che il principio attivo ha questa indicazione autorizzata. Se non lo sapesse, non la emetterebbe o la emetterebbe come off-label.
Eccallà!
Non sono d’accordo: il Farmacista in qualche modo deve sapere che…
…che cosa?
Sapere se una indicazione terapeutica è autorizzata o meno per un dato principio attivo? Certo che sì, ma come esercizio mnemonico professionale, nulla di più.
Sapere se quella ricetta che ha in mano è per un’indicazione terapeutica A o B? Certo che no, la Legge non glielo richiede (lo chiede al Medico), piuttosto gli chiede aspetti tecnici e formali, in quanto preparatore tecnico di farmaci, non medico diagnostico.
O forse deve sapere se nel tal Paese dell’Est o del Nord Europa esiste una indicazione terapeutica per il tal principio attivo? Abbiamo già visto che è compito solo ed esclusivamente del Medico.
Anche perché, attenzione, se si sostenesse una tesi del genere si creerebbe il paradosso che a seconda delle conoscenze personali del Farmacista cui il paziente ha davanti, la preparazione potrebbe essere realizzata o meno (in altre parole, la ricetta potrebbe essere spedita o meno):
- paziente Tizio che va nella Farmacia A e dà la ricetta al Farmacista X che interpreta la ricetta con nome e cognome correttamente in-label in quanto il Farmacista X si ricorda che il principio attivo prescritto è autorizzato in Repubblica Ceca per l’indicazione terapeutica che ritiene essere quella della ricetta. Esegue la preparazione.
- sempre il paziente Tizio che va nella Farmacia B e dà la ricetta al Farmacista Y che interpreta la ricetta con nome e cognome non corretta, ma necessitante dell’off-label in quanto al Farmacista Y non risulta tale indicazione. Non esegue la preparazione.
2 pesi e 2 misure. 2 atteggiamenti errati, anche se uno dei 2 con esito favorevole (la preparazione del farmaco). Se si fosse seguita la Legge, non si sarebbero state altre possibilità se non la preparazione del medicinale di fronte ad una ricetta formalmente corretta. Quello che la Legge vuole (ubi lex voluit).
Domande Frequenti
Diciamo che la Cannabis Terapeutica dal punto di vista pratico va considerata come un’eccezione.
Detto che in teoria quanto illustrato nell’articolo vale anche per la cannabis terapeutica, nella realtà non è così. Perché? Per la caccia alle streghe.
È dal 2013 che dal Ministero della Salute escono circolari, richiami, indicazioni per NAS e AUSL circa la necessità (obbligatorietà) di prescrivere la cannabis sempre e solo come off-label in quanto il Ministero stesso ha dichiarato che “non esistono indicazioni terapeutiche approvate per la cannabis terapeutica“.
Ecco dunque che, per evitare contestazioni da parte di chicchessia (poiché la ricetta viene inviata ad AUSL che la invia al Ministero della Salute), è bene che la collaborazione tra Medico e Farmacista sia sempre presente e ci sia piena consapevolezza che le ricette di Cannabis Medica devono sempre essere prescritte come off-label.
Dal punto di vista professionale (e deontologico) la collaborazione tra Medico e Farmacista per aiutarsi vicendevolmente è più che raccomandata e auspicabile. Ma NULLA (ripeto NULLA) può essere imputato al Farmacista circa l’aver spedito una ricetta medica in-label formalmente corretta quando in realtà si scopre che doveva essere off-label. La Legge 94/98 è molto precisa nell’assegnare obblighi e ruoli, oltre che elementi per adempiere al proprio dovere professionale.
A parte il nervoso del non aver ancora capito che “serve la Di Bella” è errata come affermazione :P, la risposta è un’altra domanda: come fai tu Farmacista Galenista a dire che quel principio attivo non è autorizzato in un’altro Paese proprio per quella indicazione in-label? Ah, non lo sai. Ecco allora tac… ehm… fai il tuo mestiere (controllo iperdosaggi, controllo incompatibilità, formalità della prescrizione) e lascia al Medico il suo: come già detto, il Medico SA che se non ci fosse l’indicazione terapeutica autorizzata, avrebbe dovuto fare la ricetta come off-label.

Alcuni esempi per capire
Facciamo alcuni esempi pratici per applicare nella realtà quello che, spero, ormai sia chiaro.
P. S. Se vi tremano le mani o siete sotto shock, coraggio. Passerà 
Finasteride capsule da 1 mg
Scenario: il Farmacista Galenista riceve una ricetta riportante
- nome e cognome del paziente
- prescrizione di “Finasteride 1mg – eccipienti q. b. – di tali 100 capsule”
- timbro, data, firma del medico
Ragionamento (sbagliato) del Farmacista “Di Bella”: in commercio esiste una specialità medicinale da 1mg di finasteride (es. Propecia) registrata con indicazioni terapeutiche nel trattamento dell’alopecia. Essendo la prescrizione galenica di 1 mg di finasteride, vuol dire che è per l’alopecia e quindi la ricetta è “non ripetibile”.
Ragionamento (corretto) del Farmacista Galenista “Di Bella”: la ricetta non presenta incompatibilità chimico fisiche. Non sono superati i dosaggi della Tabella 8 o di specialità industriali o della letteratura disponibile. Tutti i formalismi sono presenti. La finasteride ricade in Tabella 4 della FU per cui la ricetta è valida e ripetibile.
Commento del Medico: ho prescritto la finasteride per l’ipertrofia prostatica benigna di un paziente monorene per il quale necessita di aggiustamento di dosaggio.
Minoxidil, progesterone, estriolo e latanoprost lozione
Scenario: il Farmacista Galenista riceve una ricetta riportante
- nome e cognome del paziente
- prescrizione di “soluzione di minoxidil 3%, progesterone 0.5%, estriolo 1%, latanoprost 0.01% – eccipienti q. b. – di tali 100 ml“
- timbro, data, firma del medico
Ragionamento (sbagliato) del Farmacista “Di Bella”: il latanoprost è un principio attivo registrato per l’ipertensione oculare, mentre in questo caso è per favorire la ricrescita del capello. Non essendo quindi una indicazione autorizzata, serve la “Di Bella”.
Ragionamento (corretto) del Farmacista Galenista “Di Bella”: la ricetta non presenta incompatibilità chimico fisiche. Non sono superati i dosaggi della Tabella 8 o di specialità industriali o della letteratura disponibile. Tutti i formalismi sono presenti. per la presenza di ormoni si ricade in Tabella 5 e la ricetta, valida, è non ripetibile.
Commento del Medico: ho prescritto il preparato per combattere l’alopecia del paziente, aggiungendo il latanoprost per contrastare la caduta, indicazione autorizzata di un medicinale topico registrato in Olanda.
CBD cristalli in crema topica
Scenario: il Farmacista Galenista riceve una ricetta riportante
- nome e cognome del paziente
- prescrizione di “CBD cristalli 1% in crema base beeler q. b. 50g“
- timbro, data, firma del medico
Ragionamento (sbagliato) del Farmacista “Di Bella”: il CBD non ha indicazioni terapeutiche approvate ad uso topico quindi serve la “Di Bella”.
Ragionamento (corretto) del Farmacista Galenista “Di Bella”: la ricetta non presenta incompatibilità chimico fisiche. Non sono superati i dosaggi della Tabella 8 o di specialità industriali o della letteratura disponibile. Tutti i formalismi sono presenti. La ricetta è valida e ripetibile.
Commento del Medico: ho prescritto questa crema per l’attività antiseborroica, autorizzata in cosmesi.
Prilocaina 2% fiale
Scenario: il Farmacista Galenista riceve una ricetta riportante
- nome e cognome del paziente
- prescrizione di “Procaina 2% fiale iniettabili – 5 ml e di tali n° 10“
- timbro, data, firma del medico
Ragionamento (sbagliato) del Farmacista “Di Bella”: la procaina iniettabile in Italia esiste solo ad uso veterinario, quindi per l’umana non ci sono indicazioni autorizzate e di conseguenza serve la “Di Bella”.
Ragionamento (corretto) del Farmacista Galenista “Di Bella”: la ricetta non presenta incompatibilità chimico fisiche. Non sono superati i dosaggi della Tabella 8 o di specialità industriali o della letteratura disponibile. Tutti gli altri formalismi richiesti sono presenti. Avendo fatto la prescrizione, il Medico sa che in Europa esiste un medicinale (indipendentemente dalla forma farmaceutica) a base di procaina autorizzato per l’indicazione terapeutica X. La ricetta è valida e non ripetibile in quanto ricade in Tabella 5 (anestetici) della FUI.
Commento del Medico: ho prescritto queste iniezioni per indicazione terapeutica approvata (es. X = anestesia locale).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Come fa il Farmacista a capire quando serve la “Di Bella” in Galenica? sembra essere il primo su Farmagalenica.
]]>L'articolo Curcuma 95%, 99% e curcumina capsule: possibilità in Galenica sembra essere il primo su Farmagalenica.
]]>Oltre ad essere una pianta nota per il suo uso alimentare, è contenuta in moltissimi integratori alimentari, vanta diverse proprietà terapeutiche ed è presente addirittura in alcuni farmaci (es. iniettabili) anche se come molecola pura. Viene però da tempo preparata come farmaco galenico o officinale (salutistico) da parte dei Farmacisti Galenisti di Farmagalenica dotati di laboratorio galenico (v. farmacie aderenti in fondo all’articolo).
L’articolo che state per leggere nasce per mettere ordine a quello che è successo nel 2023 in Italia (sempre noi!) dopo una circolare del Ministero della Salute:
- ci sono ancora integratori di curcuma estratto secco?
- quali tipo di curcuma si possono ancora trovare?
- che differenze tra curcumina e curcuma, 95 e 99%?
- cosa può fornire il farmacista Galenista in questo scenario?
Tutte le esaustive risposte che state cercando e molto altro nel testo che segue.
Differenza tra curcuma polvere, curcumina e curcuma estratto secco
La curcuma, conosciuta anche come “oro indiano”, è apprezzata sia per le sue proprietà culinarie che terapeutiche.
La curcuma polvere alimentare è la forma più comune, spesso utilizzata come spezia nei piatti per dare colore e sapore. Si tratta essenzialmente di radici di curcuma essiccate e polverizzate.
L’estratto secco di curcuma è una forma concentrata, ottenuta tramite un processo di estrazione che isola i principi attivi della pianta, permettendo di avere un prodotto più potente e meno voluminoso.Tra questi principi attivi, la curcumina è il più conosciuto e studiato.
Mentre la curcuma polvere alimentare può contenere dal 2% al 5% di curcumina, gli estratti secchi di curcuma sono spesso standardizzati al 95% o al 99% di curcumina, offrendo così una potenza maggiore.
La curcumina, da parte sua, può essere ottenuta per estrazione o anche per sintesi chimica (come una qualsiasi molecola sintetizzata pura al 99.x%).
La curcumina è la molecola pura presente nella curcuma, responsabile delle principali attività della pianta curcuma longa.
Curcumina e curcuminoidi: qual è la differenza?
Per capire cosa è successo a Maggio 2023 e perché, è importante sia chiaro che quanto parliamo di
- curcuma estratto secco al 95% titolato in curcumina
- curcuma estratto secco al 95% titolato in curcuminoidi
stiamo parlando di 2 cose che sono un po’ diverse. Veloce spiegazione prima di proseguire, non annoierò, garantisco (sempre io).
Curcuma estratto secco al 95% titolato in curcumina
Significa che, pesati 100 grammi di polvere di estratto secco sulla bilancia, 95 grammi di questa polvere conterranno la molecola pura “curcumina”. Il resto 5% (5 grammi nell’esempio) sono sostanze di supporto (es. maltodestrine e residui dell’estrazione).
In ogni caso, 95 grammi sono solo ed esclusivamente di 1 singola molecola: la curcumina.
Curcuma estratto secco al 95% titolato in curcuminoidi
Riprendendo l’esempio sopra, significa che pesati 100 grammi di polvere di estratto secco sulla bilancia, 95 grammi di questa polvere conterranno una miscela di sostanze (es. curcumina, demetossicurcumina, bisdemetossicurcumina). Anche qui, il restante 5% (5 grammi nell’esempio) sono sostanze di supporto (es. maltodestrine e residui dell’estrazione).
In questo caso, 95 grammi sono diverse molecole raggruppate sotto un unico nome: curcuminoidi.
Prima della circolare del Ministero della Salute Italiano
Prima di Maggio 2023, sul mercato italiano erano reperibili diversi prodotti (farmaceutici e non farmaceutici) che contenevano:
- curcuma polvere
- curcuma estratto secco al 95% titolato in curcumina
- curcuma estratto secco al 95% titolato in curcuminoidi
- curcumina pura al 99%
presenti all’interno di questi prodotti:
- integratori alimentari
- farmaci industriali
- preparati galenici magistrali (con ricetta)
- preparati galenici officinali salutistici (senza ricetta)
Questa una tabella riassuntiva della situazione PRIMA di Maggio 2023:
| curcuma polvere | curcuma E.S. 95% curcumina | curcuma E.S. 95% curcuminoidi | curcumina 99% | |
| alimenti | SI | NO | NO | NO |
| integratori alimentari | SI | SI | SI | NO |
| farmaci industriali | NO | NO | NO | SI |
| preparati galenici magistrali (ricetta) | SI | SI | SI | SI |
| preparati galenici salutistici (senza ricetta) | SI | SI | SI | NO |
Di fatto, il Farmacista Galenista poteva allestire qualsiasi preparazione galenica a base di curcuma o con ricetta o senza ricetta a seconda del caso.
Poi è arrivata una circolare dal Ministero della Salute, del 4 Maggio 2023 scaricabile dal link qui sotto. E le cose sono cambiate (SPOILER: per il Farmacista Galenista poco e niente).

DOPO la circolare del Ministero della Salute Italiano
Riassumendo e andando al sodo, nella Circolare il Ministero dice che
- la curcuma estratto secco al 95% in curcuminoidi ha una ampia storia (uso significativo).
- la curcuma estratto secco al 95% in curcuminoidi è quindi liberamente impiegabile.
- la curcuma estratto secco al 95% in curcumina non ha un’ampia storia di utilizzo (uso significativo)
- la curcuma estratto secco al 95% in curcumina non può essere usata negli integratori alimentari perché classificabile come novel food
Quindi: non possono più essere venduti integratori alimentari che contengono curcuma 95% di curcumina!
Fine. La nota parla di integratori alimentari e per questo si riferisce anche i prodotti salutistici preparati dal Farmacista che sono di libera vendita. Quindi: non possono neanche più essere venduti preparati galenici officinali salutistici che contengono curcuma 95% di curcumina.
Tutto finito? Dobbiamo dire addio all’estratto secco di curcuma 95% titolato in curcumina? NO.
Tabella riepilogativa sulla curcuma concentrata: ricetta o libera vendita?
Il senso dell’intervento del Ministero della Salute è quello di impedire il libero acquisto (da parte del consumatore finale) di prodotti che, sostanzialmente, contengano curcumina pura: gli integratori alimentari sono prodotti che non richiedono ricetta medica e pertanto non la possono contenere sia come molecola pura (curcumina purissima) che estratto altamente titolato (curcuma 95% titolato in curcumina).
E tutto questo NON perché vengono introdotti divieti per la tutela della salute pubblica (cosa che una nota dal punto di vista tecnico-giuridico non può fare): la nota lascia intendere che esistono integratori in Europa a base di curcuma 95% in curcumina, ma pochi e da poco tempo.
Il “divieto” di utilizzo negli integratori alimentari è perché la normativa prevede che in questo contesto i prodotti di libera vendita vengono classificati come novel food e non integratori alimentari ossia che devono seguire un iter regolatori diverso per essere immessi sul mercato.
Va da se che i farmaci industriali o i prodotti con ricetta medica non sono toccati dalla Circolare e possono continuare a contenere curcumina pura e curcuma estratto secco al 95% in curcumina.
Chiesto dal punto di vista dell’utente finale:
- cosa posso acquistare con ricetta?
- cosa possono acquistare senza ricetta?
Rispondiamo semplicemente con una cosa che già conoscete, ossia una tabella con evidenziato il cambiamento:
| curcuma polvere | curcuma E.S. 95% curcumina | curcuma E.S. 95% curcuminoidi | curcumina 99% | |
| alimenti | SI | NO | NO | NO |
| integratori alimentari | SI | NO | SI | NO |
| farmaci industriali | NO | NO | NO | SI |
| preparati galenici magistrali (ricetta) | SI | SI | SI | SI |
| preparati galenici salutistici (senza ricetta) | SI | NO | SI | NO |
Legge Di Bella e Lista BELFRIT
Capitolo breve ma tecnico, saltate pure se non vi interessa: abbiamo detto che l’estratto secco di curcuma 95% in curcumina può essere preparato dal Farmacista Galenista dietro presentazione di ricetta medica. Ma qual è la normativa precisa che regola la prescrizione da parte del Medico?
Risposta: sono 2
- la lista BELFRIT
- la Legge Di Bella
Nel primo caso, è consentito al Medico prescrivere “piante, loro parti e derivati” presenti nella lista BELFRIT. La “curcuma longa rizoma” è presente. Nulla impedisce quindi al medico di prescrivere un estratto secco, glicerico o altro, titolato al 10, 50, 95, 98, 99% in curcumina o curcuminacee essendo la pianta presente nell’elenco.
Similmente, la prescrizione di curcuma pura o curcuma 95% in curcumina o 95% in curcuminoidi è possibile in quanto la sostanza curcumina è presente in monografie di farmacopea o è contenuta in almeno 1 integratore in commercio in Europa.
Che sia quindi per un motivo o per l’altro, il Medico può prescrivere la curcuma come vuole e piace.

Ruolo del Farmacista Galenista e curcuma 95%
Il Farmacista Galenista può continuare a preparare galenici (detti magistrali) a base di curcuma 95% titolata in curcumina con ricetta medica!
Chiaro e semplice
Effetti collaterali della curcuma 95% titolata in curcumina
La curcuma è generalmente considerata sicura quando consumata come spezia o in dosi moderate come integratore.
Tuttavia, come qualsiasi sostanza, un eccessivo consumo può portare a potenziali effetti collaterali. Potrebbero aversi infatti effetti collaterali tipici quali
- disturbi gastrointestinali
- nausea
- diarrea
La curcumina può anche interagire con alcuni farmaci, come anticoagulanti o antiaggreganti piastrinici, aumentando il rischio di sanguinamento.
Importante è sapere che diversi integratori di curcuma contengono anche piper nigrum (pepe nero) per aumentare la biodisponibilità della curcuma. Il retro della medaglia è che ha un impatto molto significativo sul fegato, quindi attenzione a chi ha problemi epatici o assume molti farmaci (per rischio di interazioni significative).
Inoltre, dosi elevate di curcumina possono causare un abbassamento della pressione sanguigna o influenzare i livelli di zucchero nel sangue.
Quanto costa la curcuma 95% estratto secco preparata dal Farmacista?
Costo curcuma capsule con ricetta medica
Per la vendita di curcuma 95% in curcumina o curcumina pura abbiamo ormai ampiamente capito che serve ricetta medica. Tale ricetta è una ricetta ripetibile valida 6 mesi per un massimo di 10 volte.
In questo caso il costo del preparato non è deciso liberamente dal Farmacista Galenista, ma dalla Tariffa Nazionale dei Medicinali che all’art. 12 impone sia liberamente consultabile per l’acquirente: a titolo di esempio, quindi, ecco alcuni prezzi per dare un’idea, ma ricordate che possono ampiamente variare in base al costo della materia prima (che ragionevolmente aumenterà con il passare del tempo diventando sempre più rara e meno richiesta):
- capsule di estratto secco curcuma 95% in curcumina 500 mg – 30 capsule = CIRCA 25€
- capsule di estratto secco curcuma 95% in curcumina 500 mg – 90 capsule = CIRCA 69€
Costo curcuma capsule senza ricetta medica (di libera vendita)
Nel caso si voglia invece acquistare curcuma con curcuminoidi, il prodotto è definito salutistico e non richiede ricetta. La norma prevede che in questo caso, il farmacista sia libero di applicare il prezzo che preferisce. Fate dunque riferimento alla Farmacia Galenica per chiedere il costo che varierà in base
- al dosaggio
- al numero di capsule
Essendo la curcuma capsule un FARMACO galenico, come tutti i farmaci è fiscalmente detraibile. Consultare questa pagina per maggiori informazioni.
Per cercare e visualizzare la Farmacie di Farmagalenica in grado di preparare curcuma capsule (curcuma 95%, curcumina, curcuminoidi), consultare il motore di ricerca cercagalenico.it (si aprirà una nuova pagina).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Curcuma 95%, 99% e curcumina capsule: possibilità in Galenica sembra essere il primo su Farmagalenica.
]]>L'articolo Galenici conto terzi per altre farmacie: la Cassazione apre la via? sembra essere il primo su Farmagalenica.
]]>Sulla liceità o meno della questione che non è regolata né vietata (leggere qui) da alcuna legge, la maggior parte dei Farmacisti (anche i più “su”) assume la posizione del non si può fare e non ci sono alternative.
Ma la Sentenza della Cassazione (48839/2022 – sezione sesta penale, depositata il 22 dicembre 2022), che pur riguarda un altro caso specifico, contiene riferimenti e indicazioni che di fatto aprono alla via a quello che (a parere dello scrivente) era già ovvio da tanto, tanto tempo ossia che è possibile per una farmacia preparare farmaci galenici e inviarli per il ritiro presso un’altra farmacia “satellite”.
SPOILER:  In realtà non si tratta di vero e proprio conto terzi, quanto della possibilità per una farmacia satellite di offrire un servizio di consegna di galenici preparati da un’altra farmacia.
In realtà non si tratta di vero e proprio conto terzi, quanto della possibilità per una farmacia satellite di offrire un servizio di consegna di galenici preparati da un’altra farmacia.
In questo articolo, di natura puramente didattica ed indicativa il cui scopo è stimolare il dibattito e affrontarne le implicazioni, si andranno ad analizzare tutti i riferimenti normativi e le indicazioni della Cassazione per stabilire una delle seguenti possibilità:
- o perché ad oggi è legittima la produzione di galenici magistrali per conto di un’altra farmacia
- o perché è consentito inviare ad una Farmacia preparati galenici per essere forniti al cliente.
L’articolo è esclusivamente di natura didattica e nulla è garantito se quanto riportato sia o meno a norma di legge. L’autore non si assume nessuna responsabilità per le scelte individuali o aziendali e azioni che dovessero derivare dalla lettura del seguente articolo.
DISCLAIMER
Introduzione e background
Prima di procedere è bene sia chiaro lo scenario di cui stiamo parlando: è il caso in cui un paziente ha una ricetta medica per una preparazione galenica (v. dopo), ma la farmacia più vicina che effettua una preparazione galenica si trova a centinaia di Km, per cui chiede ad una Farmacia che non fa galenica (che chiameremo d’ora in poi Farmacia Z o satellite) la preparazione del medicinale galenico con ricetta medica. Questa Farmacia Z non ha un laboratorio galenico funzionante, dato che non effettua preparazioni galeniche perciò chiede alla Farmacia A (che chiameremo galenica o preparatrice) di allestire per conto il farmaco galenico e recapitarlo alla Farmacia Z affinché lo fornisca al paziente.
A questo punto, possiamo avere 2 scenari:
- Scenario 1: la farmacia A vende il farmaco alla farmacia Z che lo rivende al paziente
- Scenario 2: la farmacia A cede il farmaco alla farmacia Z che lo consegna al paziente
Quale è lo scenario corretto in cui operare dopo la sentenza della Cassazione? Scopriamolo 
Definizione dei Farmaci Galenici
Anche se alcuni conosco l’argomento, è importantissimo sapere esattamente parola per parola cosa dice la Legge, che in questa parte iniziale sono le Norme di Buona Preparazione della Farmacopea Ufficiale Italiana XII ed. e successive modificazioni (pagina 1426). Ci si riferisce alla definizione di:
- Preparato Magistrale o Formula Magistrale: medicinale preparato in farmacia in base ad una prescrizione medica destinata ad un determinato paziente. Sono tecnicamente assimilabili ai preparati magistrali anche tutte le miscelazioni, diluizioni, ripartizioni, ecc., eseguite per il singolo paziente su indicazione medica.
- Preparato officinale o Formula officinale: medicinale preparato in farmacia in base alle indica- zioni di una farmacopea e destinato ad essere fornito direttamente ai pazienti che si servono in tale farmacia.

Galenici cono terzi: Magistrali sì e Officinali no?
Consideriamo lo scenario 1, ossia la Farmacia A che vende il farmaco alla Farmacia Z che lo rivende al paziente.
Partiamo dalla definizione del preparato officinale: dalla lettura precisa del testo risulta che
…destinato ad essere fornito direttamente ai pazienti che si servono in tale farmacia.
È abbastanza evidente e palese come tale definizione chiude la strada alla possibilità di una vendita per conto, ossia che la Farmacia A (preparatrice) possa preparare un officinale da vendere alla Farmacia Z (satellite) affinché lo rivenda ai sui clienti.
Esempio pratico: la Farmacia A prepara un farmaco galenico officinale come l’aciclovir 5% unguento ai PEG in tubetti da 10g che vende ai propri clienti a 10€. La Farmacia Z (satellite) vuole acquistarli a 8€ per vedenderli a 10 o anche 12€ ai propri clienti. Tutto questo NON si può fare!
Si noti il termine finora usato: VENDERE. Dal punto di vista giuridico, significa che viene concluso un contratto avente per oggetto il trasferimento della proprietà di una cosa o il trasferimento di un altro diritto verso il corrispettivo di un prezzo.
Art. 1470 del codice civile
Non è quindi possibile per una Farmacia A (galenica) preparare un farmaco officinale, trasferirne la proprietà alla Farmacia Z ossia venderlo alla Farmacia Z (affinché lo rivenda) ossia preparalo per conto.
Tenendo a mente la definizione del codice civile appena enunciata, passiamo al preparato magistrale: nella definizione della formula magistrale non vi è invece alcun limite legato alla dispensazione diretta al paziente.
In altre parole, nel caso del galenico magistrale non vi sono limiti a come e dove verrà venduto e fornito il farmaco magistrale (cioè preparato con una ricetta medica).
Viene quindi lineare sulla base del precedente ragionamento, affermare che è possibile per una Farmacia A (preparatrice) preparare un farmaco magistrale, trasferirne la proprietà alla Farmacia Z ossia venderlo ossia preparalo per conto.
ATTENZIONE PRIMA DI ESULTARE! Calma e continuate a leggere.
Produzione conto terzi e vendita all’ingrosso: il D.lgs 219/2006
La prima (unica?) obiezione che potrebbe nascere dall’idea che una Farmacia A (preparatrice) possa preparare un galenico magistrale e venderlo a una Farmacia Z (satellite) è: se c’è un contratto di vendita tra le 2 farmacie (B2B), si tratta di una vendita all’ingrosso. Vero.
Per commercio all’ingrosso si intende l’attività svolta da chiunque che professionalmente acquista merci in nome e per conto proprio e le rivende ad altri commercianti, all’ingrosso o al dettaglio, o ad utilizzatori professionali, o ad altri utilizzatori in grande.
Camera di Commercio
Per la vendita all’ingrosso da parte di una Farmacia a un soggetto terzo (magazzino, farmacia, ecc…), il D.lgs 219/2006 prevede agli artt. 99 – 112 che la Farmacia che vende all’ingrosso sia autorizzata con opportuna licenza.
Ah, stiamo dunque dicendo che per una Farmacia A (preparatrice) che vende un galenico magistrale alla Farmacia Z (satellite) deve avere l’autorizzazione all’ingrosso? Nonostante verrebbe da dire di sì, la risposta è no, non serve alcuna autorizzazione di grossista in questo caso.
Come? Perché?
Perché sempre il D.lgs 219/2006 si occupa SOLO del farmaco industriale e non dei farmaci galenici. Vi sembra troppo generico? Sappiate che il Titolo II, art. 3 c. 1 di tale Decreto recita:
Le disposizioni del presente decreto non si applicano: a) ai medicinali preparati in farmacia in base ad una prescrizione medica destinata ad un determinato paziente, detti “formule magistrali“, che restano disciplinati dall’articolo 5 del decreto-legge 17 febbraio 1998, n. 23, convertito, con modificazioni, dalla legge 8 aprile 1998, n. 94;
D.lgs 219/2006
Ergo, TUTTO quello che contiene e disciplina il D.lgs 219/2006, incluse le autorizzazioni all’ingrosso, non si applicano al campo della galenica.
Cool, eh?
MA ATTENZIONE. Non è finita. Continuate a leggere. 
Prima della Cassazione
In base a quanto esposto finora, parrebbe dunque sostenibile la tesi del “La Farmacia A prepara un galenico magistrale e lo vende alla Farmacia Z che a sua volta lo rivenderà al paziente”, ma ad oggi sulle modalità operative non vi è alcune riferimento preciso pur considerando che:
- il prezzo del farmaco magistrale è calcolato obbligatoriamente tramite Tariffa Nazionale dei Medicinali e non può essere in nessun caso superato (è una sanzione pesante)
- ci sono adempimenti secondari da considerare nella dispensazione da parte della Farmacia Z: chi timbra la ricetta (nel gergo si dice “spedisce la ricetta”). E se la ricetta viene timbrata dala Farmacia A (che deve timbrarla pure se allestisce galenici conto terzi), anche la Z deve timbrarla dato che effettua una dispensazione vera e propria?
- poiché la Farmacia Z ha dispensato, di chi sono le responsabilità in caso di problemi? Della Farmacia A, Z o di entrambi?
- la Sentenza della Cassazione (che vedremo a brevissimo nel prossimo paragrafo) dà indicazioni in merito. E non giocano a favore di questa possibilità (v. dopo).
Ora, non arrabbiatevi ma la morale è che attualmente, nonostante sembri tutto possibile (e magari lo è) la vendita di un galenico magistrale da parte di una farmacia ad un’altra è una strada impervia e piena di possibili contestazioni, soprattuto considerando l’avanguardia della materia.
Morale: una farmacia non può produrre e vendere galenici conto terzi magistrali o officinali a un’altra farmacia.
Scenario 1: non attuabile
Inoltre, tutta la discussione finora trattata nell’articolo non è oggetto della sentenza della Cassazione di cui si sta per parlare, ergo non ci sono riferimenti normativi precisi a differenza di quanto verrà esposto nello Scenario 2.
Continuate a leggere, tutto sarà più chiaro tra pochissimo 

Galenici conto terzi: Cassazione e sentenza 48839/2022
Andiamo ora allo Scenario 2.
Scenario 2: la farmacia A (preparatrice) prepara il galenico magistrale e lo cede alla farmacia Z che lo consegna al paziente.
Importante: in Italia non esiste il common law, ossia le sentenze non modificano o creano una legge. Danno una indicazione, creano giurisprudenza e maggiore è il grado di giudizio, maggiore è l’autorevolezza e di conseguenza l’indicazione da seguire. La Cassazione (come ben noto a tutti) è uno dei più alti e autorevoli gradi di giudizio.
La storia affrontata dalla Cassazione non riguarda in realtà i farmaci galenici magistrali, ma affronta un caso di abuso di professione di Farmacista in cui una Farmacia di Messina inviava pacchi sigillati contenenti farmaci industriali (soggetti a ricetta medica o anche di libera vendita) ad attività esterne alla farmacia (es. macelleria del paese) affinché i pazienti si recassero poi a ritirarli.
Per i dettagli della storia (che per buona parte a noi non interessa) rimandiamo a questo articolo.
Dalla lettura della sentenza, emergono però diverse considerazioni interessanti per il tema qui trattato. Vediamole una a una.
Non è illegale consegnare un farmaco a una attività esterna affinché venga ritirato dal cliente
Nella sentenza si legge che la persona diversa dal Farmacista (commerciante, macellaio, lattaio, ecc…) che riceve un pacco sigillato indirizzato ad una data persona, identificabile dai dati riportati sull’esterno del pacco, non può essere tacciata di abuso di professione di Farmacista dato che, per i Giudici della Cassazione, tale attività non è classificabile come somministrazione diretta poiché tutti gli adempimenti di Legge sulla dispensazione e preparazione dei farmaci, evidenziano i Giudici, sono stati effettuati preventivamente dal Farmacista in Farmacia.
Per assurdo dunque la Farmacia A potrebbe preparare non tanto dei galenici conto terzi (magistrali o officinali) per una Farmacia Z, ma galenici magistrali e officinali e fornirli ad una attività diversa dalla Farmacia Z dove il paziente andrà a ritirarli!
Non è illegale la vendita a distanza di farmaci soggetti a ricetta medica quando la spedizione della ricetta avviene in Farmacia
Una delle tante leggende metropolitane che circolano è il divieto assoluto di vedere farmaci soggetti a ricetta medica a distanza, come stabilito dal D.lgs 219/2006 art. 112-quater (pronto? Avete presente durante il periodo COVID quante erano le aziende che prelevavano ricette legalmente, le portavano in farmacia e riconsegnavano i farmaci a domicilio ossia distanza?).
Ecco cosa recita l’art. 112-quater del D.lgs 219/2006:
È vietata la fornitura a distanza al pubblico dei medicinali con obbligo di prescrizione medica.
Vendita on line da parte di farmacie e esercizi commerciali di cui al decreto-legge 4 luglio 2006, n.223, convertito, con modificazioni, dalla legge 4 agosto 2006, n. 248.
Anche al lettore più distratto non saranno sfuggite 3 osservazioni:
- è sempre il D.lgs 219/2006, quello che abbiamo già visto prima escludere categoricamente i galenici magistrali. Ergo questa disposizione non si applica i farmaci galenici (o galenici conto terzi).
- il Titolo VII-bis parla di “Vendita on line da parte di farmacie e esercizi commerciali di cui [omiss]” ossia la norma fa riferimento a INTERNET, cioè al divieto di vendere su e-commerce farmaci con ricetta medica per l’impossibilità del Farmacista di “spedire” la ricetta medica sul o tramite sito internet.
- i Giudici della Cassazione non hanno neppure considerato questo aspetto normativo nel valutare il comportamento della Farmacia di Messina.
Si consideri anche che il Codice Deontologico del Farmacista prevede esplicitamente la consegna a domicilio (giuro!), inclusa specificatamente quella dei farmaci soggetti a ricetta medica senza distinzione sul tipo (esempio stupefacenti o non stupefacenti) o sulle modalità (direttamente dal Farmacista, tramite fattorino o personale interno o corriere interno o corriere esterno.
1. La consegna a domicilio dei medicinali soggetti a prescrizione medica può essere effettuata soltanto dopo che in farmacia sia avvenuta la spedizione della ricetta originale.
2. Il farmacista che pone in essere iniziative di consegna a domicilio dei medicinali deve garantire che tale servizio sia svolto nel rispetto di quanto previsto dagli artt. 11, 12 e 36 e assicurare corrette condizioni di conservazione dei medicinali.
Art. 28 del Codice Deontologico del Farmacista, 2018
Tenendo conto delle indicazioni della Cassazione nella Sentenza (pag. ) e del Codice Deontologico del Farmacista è chiaro che spedire un medicinale che richiede ricetta medica in un pacco sigillato, garantendone la corretta conservazione durante trasporto e stoccaggio (nei locali in cui viene conservato in attesa di essere ritirato dal paziente), è legale.
Non è illegale fornire farmaci soggetti a ricetta medica a distanza opportunamente conservati
Nel caso in esame, l’oggetto del contendere sono farmaci probabilmente industriali (non galenici) di libera vendita o soggetti a ricetta medica. Non è dato di conoscere dalla sentenza il tipo di farmaco (es. mutabili, stupefacenti, convenzionati, ecc…).
Si pone l’accento al fatto che le contestazioni sulla incorretta conservazione dei farmaci presso locali (es. macelleria) non sono state dimostrate, ma solo desunte. Da ciò è evidente come una Farmacia Z (satellite) che riceve un pacco sigillato avrà certamente modo di conservarlo correttamente, così come il corriere farmaceutico (es. vettore interno di un grossista oppure corriere esterno certificato) potrà assolvere alle Norme di Buona Conservazione (es. conservazione tra 2-8°C o <25°C).
Ecco che se una Farmacia A prepara galenici conto terzi magistrali e li invia alla Farmacia Z anziché altre attività commerciali, si avrà la certezza della corretta conservazione.
Non è illegale che il cessionario (es. farmacia satellite) ritiri il pagamento per conto della Farmacia che ha spedito
La Cassazione chiarisce che se al momento della consegna del pacco sigillato, il commerciante ritira l’importo in denaro corrispondente al costo del farmaco e questo importo viene girato pacificamente (per intero) alla Farmacia A (galenica), questo non costituisce prestazione o contratto i vendita.
Questo ci permette di dire che la Farmacia Z (satellite) può consegnare un pacco chiuso, sigillato, contenente scontrino, farmaci e ricette (eventuali) ad un cliente, ritirando il pagamento (contanti) da girare tal quale alla Farmacia A; e tutto questo non costituisce vendita di galenici conto terzi.
Proposta di modalità operative per agire secondo le indicazioni della Cassazione
Ecco quindi che lo scenario 2 (la farmacia A cede il farmaco alla farmacia Z che lo consegna al paziente) diventa il praticabile, non più come un vero e proprio conto terzi, ma piuttosto come servizio di recupero ricetta, invio alla Farmacia galenica e offrendo supporto logistico per il ritiro del farmaco galenico da parte del paziente.
Dopo tutto questo excursus e analisi della sentenza della Cassazione, si propone come spunto teorico un possibile modus operandi che tenga conto di ogni aspetto, legge e indicazione della giurisprudenza e che permetta ad una Farmacia Galenica A (preparatrice) di preparare galenici magistrali per una Farmacia Z (satellite). O meglio: che permeta ad una farmacia A (galenica) di prepara un galenico magistrale richiesto con ricetta medica e inviarlo come cessione (non vendita) in pacco chiuso alla Farmacia Z (satellite) dove il paziente potrà ritirarlo.
- La Farmacia Z (satellite) riceve la prescrizione galenica nella propria farmacia.
- La Farmacia Z (satellite) invia la prescrizione galenica alla Farmacia A (preparatrice) affinché venga preparato il farmaco.
- La Farmacia A (preparatrice) realizza il farmaco, determina il prezzo e “spedisce” la ricetta medica.
- La Farmacia A (preparatrice) emette scontrino fiscale/fattura di vendita per il cliente.
- Il pagamento del cliente può avvenire direttamente alla Farmacia A (es. tramite bonifico) oppure tramite la Farmacia Z (satellite) che rigira il 100% dell’importo alla Farmacia A (preparatrice), senza operare alcuna trattenuta, fee, margine, ecc…
- La Farmacia A (preparatrice) prepara un pacco chiuso al cui interno verrà posto il farmaco, scontrino/fattura, copia ricetta o originale se del caso.
- La Farmacia A (preparatrice) invia il medicinale tramite corriere farmaceutico interno o esterno che assicuri la conservazione corretta a seconda di quanto necessario (es. 2-8°C o <25°C). Viene riportato il nome e cognome della persona sull’esterno del pacco.
- La Farmacia Z (satellite) riceve il pacco. Lascia il pacco sigillato conservandolo correttamente secondo le modalità necessarie (verosimilmente indicate all’esterno).
- La Farmacia Z (satellite) consegna il pacco sigillato al cliente, eventualmente ritirando il pagamento (se necessario o se non effettuato in precedenza) per girarlo pacificamente alla Farmacia A.
Più facile a farsi che a dirsi.
Considerazioni sul rapporto economico tra Farmacia A (preparatrice) e farmacia Z (satellite)
Sicuramente dalla lettura del testo fin qui, ad alcuni Farmacisti potrebbe nascere la domanda “Ma per quale motivo la farmacia Z deve fornire il medicinale (chiuso nel pacco) al paziente senza guadagnarci nulla?“.
Un elenco di alcune riposte immediate cui segue una breve discussione:
- la Farmacia Z offre un servizio ai propri clienti con un ritorno diretto enorme e rapidamente verificabile
- i clienti avranno un motivo in più, molto specialistico, per scegliere quella farmacia anziché altre
- la Farmacia A è un fabbricante, la cui marginalità è in teoria imposta al 40%, in pratica (a causa di una Tariffa miope e aumento inflazione) è molto meno
- nulla impedisce alla Farmacia Z di iniziare a fare Galenica e preparare lei stessa il farmaco…
- le indicazioni della Cassazione non consentono alla Farmacia Z (in qualità di cessionario del pacco) di poter avere un guadagno
Molto importante, al di là delle considerazioni elencate, è il punto 5 che emerge dalla lettura della Sentenza, che può essere riassunto così:
Non può esistere alcun rapporto economico (ricarico, sconto, percentuale, ecc…) tra la Farmacia A e la Farmacia Z.
Infatti, nel momento in cui la Farmacia Z (satellite) ha un guadagno economico, cade l’impalcatura su cui si basa la Sentenza della Cassazione dato che:
Risulta del tutto erronea la valutazione del primo giudice circa l’attività di vendita al pubblico di farmaci svolta dagli imputati solo in forza del pagamento dei farmaci, pacificamente destinato alla farmacista XXX [omiss]
Una nota dell’Autore su questo aspetto: la farmacia Z ha un ritorno dello 0% sul prezzo di vendita, ma del 100% sul ritorno per la farmacia: un servizio fornitura di “galenici conto terzi” permette alla Farmacia Z di soddisfare l’esigenza di un cliente/paziente che si rivolge a quella Farmacia Z, fornendogli il medicinale galenico (preparato presso la farmacia A) ed evitando che il paziente si rivolga ad altre (quindi garantendo quindi l’accesso alla Farmacia Z).
Di fatto viene offerto un servizio a chi si rivolge alla Farmacia Z che tante altre farmacie non possono offrire: oltre ad un ritorno di immagine, nel tempo si consolida un ritorno in termini di accessi per preparazioni galeniche (e vendite collaterali).
E il paziente?
Il paziente è al centro di tutta la vicenda, essendo lui il promotore di tutta la catena: il servizio di fornitura del farmaco galenico tramite la Farmacia Z rappresenta la possibilità di accedere al farmaco sfruttando la capillarità delle Farmacie.
Il paziente non ha idea se una farmacia galenica preparerà direttamente il farmaco o se gli verrà fornito tramite “conto terzi”: quello a cui lui interessa è ricevere il medicinale, con le garanzie della corretta conservazione e qualità assicurata dalle Norme di Buona Preparazione.
Si noti che la stessa Cassazione definisce la consegna di farmaci in pacco chiuso tramite altra logistica:
servizio di consegna e recapito dei farmaci in un luogo concordato, comodo per il cliente.
Domande varie
Alcune domande che sicuramente potranno essere sorte nella lettura dell’articolo, che si ricorda è solo un’analisi ragionata sulle possibilità (giuste o sbagliate, condivisibili o meno) ricavabili dalla lettura della Sentenza.
Se ne avete ulteriori, scrivetele nei commenti: verranno inserite nella lista delle domande sotto.
No. Dalle indicazioni della Sentenza, i Giudici identificano che il fornire un pacco chiuso non costituisce attività di somministrazione del Farmaco. Quindi la Farmacia Z NON dispensa alcunché, limitandosi a dare un pacco al cui interno si trova un medicinale galenico (e chi lo dice? Potrebbero essere libri, alimenti, giocattoli, ecc…).
Dalla sentenza non si entra nel particolare sul tipo di farmaco né i Giudici danno rilievo alla tipologia, ma concentrandosi sul concetto generale che i farmaci (TUTTI).
Quindi sì, potenzialmente anche per i farmaci galenici stupefacenti, anche se per gli stupefacenti in sez. A sarebbe meglio astenersi, dati gli adempimenti di trascrizione dati dell’acquirente ed evitare così ulteriori contestazioni (che andrebbero immediatamente portate all’attenzione dei Giudici).
Assolutamente sì, sarebbe meglio. Ma per ora c’è questa sentenza della Cassazione, bisogna augurarsi che il Legislatore ne prenda atto e regoli con paletti la questione.
Criticità e possibili contestazioni?
Sempre a questo mondo.
Una lista di possibili criticità:
- la Sentenza nello specifico riguarda l’abuso di professione di farmacista. È corretto ricavarne spunti per un contesto diverso?
- l’art. 122 del TULLS non può essere interpretato in maniera per cui alla Farmacista della vicenda viene comunque contestata la vendita fuori farmacia?
[Spoiler: tutte le criticità hanno un debunking e controdeduzioni che verrà a breve descritto]
Ricordate che:
L’articolo è esclusivamente di natura didattica e nulla è garantito se quanto riportato sia o meno a norma di legge. L’autore non si assume nessuna responsabilità per le scelte individuali o aziendali e azioni che dovessero derivare dalla lettura del seguente articolo.
DISCLAIMER
Per lasciare commenti, domande o opinioni utilizzate i commenti sotto l’articolo.

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Galenici conto terzi per altre farmacie: la Cassazione apre la via? sembra essere il primo su Farmagalenica.
]]>L'articolo Importazione cannabis medica, bando italiano e farmacie sembra essere il primo su Farmagalenica.
]]>In Italia, la cannabis medica terapeutica arriva in 3 modi:
- produzione cannabis in Italia tramite lo Stabilimento Chimico Farmaceutico Militare di Firenze
- importazione cannabis medica dall’Olanda
- importazione cannabis medica tramite bando italiano (solitamente dal Canada o Danimarca)
In questo articolo si parlerà del bando italiano per l’importazione di cannabis Medica, di come funziona, perché è stato necessario, quali e quanti bandi ci sono stati in Italia, le società vincitrici dei bandi passati, eccetera…
Perché si è fatto un bando italiano per l’ importazione cannabis medica?
La ragione è una e una sola: per la carenza di cannabis medica in Italia, ovvero l’insufficiente disponibilità di cannabis medica per i pazienti italiani che ne fanno richiesta.
L’argomento è talmente vasto che ha un suo dettagliatissimo articolo dedicato. La lettura, anche parziale, è consigliata prima di procedere con il presente articolo.
Quanti bandi per l’ importazione di cannabis medica ci sono stati finora in Italia?
Ad oggi 3 e mezzo, anche se dovremmo dire 4:
- nel 2018, bando di importazione per 100 Kg/anno per 1 anno, vinto da Aurora
- nel 2019, bando di importazione per 200 Kg/anno per 2 anni, vinto da Aurora
- nel 2021, assegnazione diretta di 110 Kg, vinto da Little Green Pharma
- l’ultimo nel 2022, bando di importazione per 630 Kg/ anno per 1 anno, in corso
Verranno descritti anno per anno, volendo potete scorrere passando direttamente a quello che vi interessa.
Bando del 2018 per l’ importazione cannabis medica [informazioni storiche, non aggiornate ad oggi]
Il bando, lo ricordiamo, nacque per far fronte alla carenza di cannabis iniziata a Giugno 2017 nel nostro Paese (i dettagli qui).
Il bando si aprì nel Novembre 2017, si concluse nel Gennaio 2019 e a Marzo 2019 arrivarono i primi grammi alle Farmacie di cannabis Canadese
Le ditte partecipanti furono 2:
Dal Febbraio 2018, i Farmacisti Galenisti Italiani di Farmagalenica ebbero a disposizione ulteriore cannabis medica da utilizzare per le preparazioni galeniche: la cannabis Pedanios (marchio Aurora) o Spektrum potrebbe infatti arrivare in Italia se una delle due società riuscirà a vincere il bando (anche se ad oggi non sono ancora state aperte le buste) per l’importazione di 100 Kg nel corso del 2018, che si andranno a sommare ai 250 Kg di importazione dalla Bedrocan BV (Olandese).
Chi vinse il bando per importazione cannabis medica nel 2018?
Siamo lieti di pubblicare in esclusiva, la prima intervista ad Aurora/Pedanios (vincitrice del bando), in fondo a questo articolo.
Dal comunicato stampa del Ministero della Difesa (v. sotto), si evince che la cannabis Pedanios Aurora è l’unica rimasta delle 2 Società presentatesi. Una è stata esclusa, rimane solo Pedanios. Va da se…Update fine Dicembre 2017: contro quanto riportato nel verbale, Spektrum (l’altra ditta del bando) è stata riammessa. Le buste NON sono ancora state aperte (dovevano esserlo il 22 Dicembre), ma lo saranno dopo le festività. Update inizio Gennaio 2018: l’apertura delle buste era prevista per il 10 Gennaio, ma per la valutazione dei ricorsi si slitterà ancora. I tempi si allungano ancora…
Update metà Gennaio 2018: Aurora Pedanios ha vinto tutte e 3 le varietà previste nel bando (leggi comunicato stampa ufficiale).
Pedanios Aurora ha vinto tutti e 3 i lotti previsti dal bando (qui il comunicato stampa ufficiale del Ministero della Difesa) e le varietà aggiudicate sono le seguenti:
- cannabis ad alto contenuto in THC 22% e < 1% CBD
- cannabis con THC 8% e CBD 8%
- cannabis con basso THC < 1% e alto CBD 8-10%
ovvero 3 varietà da sovrapporre (come contenuto in THC e CBD) a quelle esistenti, cannabis medica olandese e cannabis medica italiana. I dati sono riportati qui di seguito:
Una fondamentale differenza rispetto alle altre varietà di cannabis terapeutica legali e prescrivibili dal Medico in Italia è che la varietà cannabis Pedanios Aurora NON ha nome di marchio (es. Bediol, FM2, ecc…), ma è identificata solo dal contenuto in THC e CBD.
Cosa cambiò nel panorama della cannabis terapeutica italiana con la cannabis Pedanios del 2018?
Si aprirono 2 nuovi scenari:
- il Medico in ricetta può indicare anche solo il titolo in THC della cannabis, senza specificare un nome di marchio (es. Cannabis flos/infiorescenze 22% THC).
- davanti ad una generica ricetta di (es.) Cannabis flos/infiorescenze 22% THC, il farmacista può dispensare (di sua volontà? In base a quello che c’è? Sentito o non sentito il Medico? E lo deve dichiarare che lo ha sentito?) qualsiasi varietà di cannabis sovrapponibile (equivalente) tra quelle reperibili/disponibili. Più avanti verrà chiarito tutto.
Per chiarire meglio il punto 2, si consideri la seguente tabella di confronto:
| Cannabis Medica | Varietà | Olandese | Italiana | Canadese |
|---|---|---|---|---|
| 22% THC <1% CBD | SATIVA | Bedrocan | – | Pedanios |
| 14% THC <1% CBD | INDICA | Bedica | – | – |
| 12% THC <1% CBD | SATIVA | Bedrobinol | – | – |
| 7.5-8% THC 8-12% CBD | SATIVA | Bediol | FM2 | Pedanios (INDICA) |
| < 1% THC 9% CBD | SATIVA | Bedrolite | – | Pedanios (HYBRID) |
In base a questa, il Medico che volesse prescrivere una varietà di cannabis con il 22% in THC, potrebbe scegliere tra Bedrocan e Pedanios. Oppure se volesse prescrivere Bediol, potrebbe “sostituirlo” con FM2 o Pedanios 8/8.
Quando saranno disponibili queste varietà di marijuana canadese?
Secondo stime ufficiale degli addetti ai lavori, si potranno avere i primi lotti disponibili in Italia verso FINE Febbraio 2018. Inizio o fine… non si sa. Si consideri che alla data della pubblicazione del presente articolo, ancora non sono state aperte le buste con le offerte della cannabis Pedanios Aurora.
Questa cannabis Pedanios verrà venduta (come acquirente) al Ministero della Difesa e importata presso lo Stabilimento Chimico Farmaceutico Militare di Firenze affinché la distribuisca alle Farmacie Italiane che ne faranno richiesta.
Le altre varietà di cannabis continueranno a essere importate e vendute sempre come prima (v. articolo).
Cambierà qualcosa a livello prescrittivo?
FORSE. Le modalità prescrittive e i facsimile presenti su questo sito sono state aggiornate A QUESTO ARTICOLO è possibile reperire facsimile di ricette mediche ed indicazioni tecnico normative sulla prescrizione di cannabis Pedanios, BedrocanBV (olandese) e italiana.
Il “forse” è perché se da una parte si vuole rendere più facile l’accesso alla cannabis (ovvero, con una ricetta generica di “Cannabis 22%”, si può avere la varietà olandese o canadese senza rifare la ricetta), dall’altra non è detto che 2 varietà aventi lo stesso contenuto in THC e/o CBD siano considerabili sovrapponibili a priori.
Cambierà qualcosa a livello di prezzo di cannabis con la cannabis Pedanios Aurora?
No, assolutamente. Il prezzo di vendita della cannabis ai pazienti è fisso e stabilito per Decreto Ministeriale ed è immodificabile: 9€/grammo + IVA + costi di produzione del Farmacista. Si veda l’articolo dedicato.
Farmagalenica.it invita pubblicamente sia Spektrum che Pedanios a rilasciare una intervista/dichiarazione su sito.
Per approfondire meglio la situazione della cannabis medica in Italia (perché non si trova più cannabis fino a fine gennaio? la risposta è qui), Farmagalenica è lieta di pubblicare la prima intervista in esclusiva a Aurora/Pedanios a mezzo di Andrea Ferrari, ha intervistato la vincitrice del Bando, a mezzo di Andre Ferrari, direttore vendite per il mercato italiano (vedi ultimo paragrafo della pagina).

Bando del 2019 per importazione cannabis medica [informazioni storiche, non aggiornate ad oggi]
Il bando si aprì nel Giugno 2019 ed è alla data attuale, tutt’ora in corso.
I documenti del bando sono reperibili a questa pagina.
Le ditte partecipanti al bando importazione cannabis medica nel 2019 sono 5:
- WAYLAND ITALIA
- TILRAY PORTUGAL
- MEDICINAL ORGANIC CANNABIS AUSTRALIA
- AURORA DEUTSCHLAND
- CANOPY GROWTH GERMANY
Il 03 Luglio 2019, alla presentazione dell’offerta NESSUNA dei partecipanti ha fornito una documentazione completa e formalmente corretta (fonte:)
Per questo motivo, il bando si è “prolungato” di circa 10 giorni per permettere ai partecipanti di sanare le irregolarità.
Le buste con le offerte non sono ancora state aperte.
Update: vince Aurora, tutti e 3 i lotti del bando. Per i prossimi 2 anni, in Italia avremo le stesse varietà del 2018:
| Cannabis Medica | Varietà | Olandese | Italiana | Canadese |
|---|---|---|---|---|
| 22% THC <1% CBD | SATIVA | Bedrocan | – | Pedanios |
| 14% THC <1% CBD | INDICA | Bedica | – | – |
| 12% THC <1% CBD | SATIVA | Bedrobinol | – | – |
| 7.5-8% THC 8-12% CBD | SATIVA | Bediol | FM2 | Pedanios |
| < 1% THC 12% CBD | SATIVA | Bedrolite | – | Pedanios (HYBRID) |

Intervista esclusiva per Farmagalenica a Pedanios Italia nel 2018
Segue il testo integrale realizzato a inizio 2018, all’indomani della vincita del bando da parte di Aurora
Buongiorno Andrea, chi è e qual è il Suo ruolo presso Aurora/Pedanios?
Sono direttore vendite per il mercato italiano e il mio background è di carattere tecnico-commerciale in ambito internazionale.
Aurora e Pedanios. Quali differenze tra le 2 società?
Pedanios GmbH è la società tedesca che ha partecipato e vinto il bando di gara indetto dal Ministero della Difesa Italiano. Pedanios è la filiale europea di proprietà 100% di Aurora Cannabis Inc. ed è un’azienda certificata GMP in Germania per import, export, immagazzinamento e distribuzione all’ingrosso di cannabis medica. In futuro la nostra filiale potrebbe anche diventare produttore di cannabis medica, in caso di vincita del bando per l’assegnazione di 10 licenze alla produzione di cannabis medica sul suolo tedesco.
La nostra casa madre Aurora Cannabis Inc. è, invece, una società canadese che coltiva cannabis terapeutica con la certificazione GMP per la produzione. Con una capitalizzazione in borsa di quasi 5 miliardi di €, è uno dei due più importanti produttori mondiali. È in fase di avviamento il nostro nuovo sito produttivo Aurora Sky con 80.000 mq di superficie coperta, un impianto di coltivazione e raccolta completamente automatizzato, una logistica integrata (direttamente nel sito di un aeroporto internazionale) e con una capacità produttiva di 100 tonnellate/anno di cannabis di altissima qualità.
Dove viene coltivata la cannabis medica di Aurora?
In Canada, indoor in serre ermetiche. La coltivazione in Canada nel medio periodo sarà destinata, prevalentemente, al mercato nazionale e meno all’export. Difatti a partire dal 18 luglio di quest’anno, il Canada legalizzerà l’utilizzo della cannabis anche per uso ricreativo in tutto il paese rendendo necessario un ulteriore incremento della produzione.
Produrremo nel medesimo sito, seppure in sezioni separate, sia cannabis terapeutica (con certificazione GMP e standard di controllo elevatissimi) che cannabis per uso ricreativo (con standard comunque molto alti).
Per quanto riguarda l’Europa, oltre alla licenza che stiamo cercando di ottenere per la coltivazione in Germania e per la quale abbiamo già identificato un sito strategico, abbiamo costituito una joint-venture in Danimarca chiamata Aurora Nordic Cannabis con la quale stiamo costruendo un impianto con una capacità produttiva annua di 120 tonnellate per servire il mercato scandinavo.
In Australia, altro mercato in forte fermento, abbiamo acquisito grosse quote della Cann Group, prima azienda ad avere in questo paese la licenza per coltivare cannabis. Tramite una serie di acquisizioni strategiche e grazie a una crescita organica sui principali mercati intendiamo consolidare la nostra posizione di leadership mondiale.
Il nostro obbiettivo in ogni paese è di produrre localmente, vicino ai nostri pazienti.
Come dimostrato, infine, dalle nostre attività in settori tecnologici limitrofi, intendiamo affermarci come provider di prodotti e servizi per l’industria della cannabis e non solo come semplici produttori. Alcuni esempi di queste attività collaterali sono la nostra controllata Radient Technologies Inc. proprietaria di vari brevetti per l’estrazione dei principi attivi tramite il processo delle microonde oppure CanvasRx, la nostra azienda che si occupa di educazione e training del personale medico in Canada.
Bando italiano: avete vinto tutti e 3 i lotti richiesti. Un commento a caldo?
Siamo, naturalmente, molto soddisfatti del risultato. Dopo alcuni colpi di scena e due soccorsi istruttori, il bando si è fortunatamente concluso a nostro favore.
Vista l’urgenza delle forniture, il bando è stato indetto mediante procedura accelerata. Abbiamo dovuto correre parecchio per potere fornire in tempo tutta la documentazione ritenuta necessaria da parte delle autorità per garantire la qualità delle aziende e dei prodotti concorrenti e tutelare, quindi, la salute dei pazienti italiani.
I responsabili dell’Agenzia Industrie e Difesa (AID) e dello Stabilimento Chimico Farmaceutico Militare di Firenze hanno organizzato e gestito questo bando con molto professionalità e trasparenza. Come azienda straniera partecipante per la prima volta a un bando di gara europeo in Italia, abbiamo avuto tutto il supporto e la disponibilità da parte dei responsabili del procedimento.
Il nostro più grosso concorrente a livello mondiale, anch’esso partecipante al bando di gara, ha fatto un’offerta molto competitiva e alla fine abbiamo vinto per poco. Questo testimonia la genuinità e l’alta competitività del bando di gara.
Ci siamo aggiudicati il bando a un prezzo di 320.000 € con un ribasso di quasi la metà rispetto alla base d’asta fissata a 570.000 €. I pazienti italiani, quindi, potranno avere presto accesso a prodotti di alta qualità mentre lo Stato potrà ottenere un risparmio economico [per Decreto Ministeriale, il prezzo di vendita al pubblico della cannabis medica è fisso a 9€/g indipendentemente dal prezzo di acquisto, ndr].
Forniremo in prima battuta le 3 varietà Pedanios richieste. Le nostre varietà standard sono 5: 2 con THC alto, 2 con CBD alto, 1 bilanciato.
Quando arriveranno le prime importazioni di cannabis Pedanios in Italia?
Ci sono i tempi di autorizzazione all’esportazione e all’importazione (le cosiddette import/export licences) che dipendono dalle autorità canadesi, tedesche e italiane. Da parte nostra ci impegneremo al massimo per fare arrivare prima possibile i prodotti ai pazienti. Stimiamo che la merce potrebbe arrivare verso fine febbraio.
Una volta importato dallo Stabilimento Chimico Farmaceutico Militare di Firenze, le farmacie potranno ordinarlo utilizzando il normale sistema dei buoni di acquisto.
Il bando riguarda 100 Kg. Esauriti i 100 KG che succederà?
Il bando permette di aumentare queste quantità di alcune decine di KG senza indire una nuova gara. Non sappiamo ancora quali sono le intenzioni e il programma di acquisto del Ministero su successive forniture. È comunque probabile che queste quantità siano sufficienti per alcuni mesi ma non per coprire l’intero fabbisogno dell’anno 2018.

Bando importazione cannabis medica del 2022
Questo bando rappresenta FINALMENTE qualcosa di diverso e concreto (non risolutivo però) nel panorama della cannabis per un motivo:
è il primo bando con un quantitativo “interessante” di infiorescenze importate, ossia 630 Kg
Domande semplici sul bando per l’ importazione cannabis terapeutica di Settembre 2022
Per approfondire l’argomento del bando del Ministero della Difesa (link ufficiale) per l’ importazione cannabis terapeutica, abbiamo chiesto ad un veterano, già noto ai lettori del sito: Andrea Ferrari, advisor per Aurora prima e LGP a tutt’oggi.
Aspetti positivi del bando importazione cannabis terapeutica di Settembre 2022
Criticità del bando importazione cannabis terapeutica di Settembre 2022
Quando arriverà effettivamente la cannabis del bando nelle farmacie italiane?
Per cercare e visualizzare la Farmacie di Farmagalenica in grado di preparare cannabis terapeutica consultare il motore di ricerca cercagalenico.it (si aprirà una nuova pagina).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Importazione cannabis medica, bando italiano e farmacie sembra essere il primo su Farmagalenica.
]]>L'articolo Sostanze vietate in galenica: l’elenco completo al 2024 sembra essere il primo su Farmagalenica.
]]>Le sostanze che il Farmacista Galenista può usare sono diverse e virtualmente infinite.
In realtà la risposta tecnica a quali sostanze possano esse usate in un laboratorio galenico di una farmacia per preparare farmaci va cercata nell’art. 5 comma 1 della Legge 94/98:
Fatto salvo il disposto del comma 2, i medici possono prescrivere preparazioni magistrali esclusivamente a base di principi attivi descritti nelle farmacopee dei Paesi dell’Unione europea o contenuti in medicinali prodotti industrialmente di cui e’ autorizzato il commercio in Italia o in altro Paese dell’Unione europea. La prescrizione di preparazioni magistrali per uso orale può includere principi attivi diversi da quelli previsti dal primo periodo del presente comma, qualora questi siano contenuti in prodotti non farmaceutici per uso orale, regolarmente in commercio nei Paesi dell’Unione europea; parimenti, la prescrizione di preparazioni magistrali per uso esterno può includere principi attivi diversi da quelli previsti dal primo periodo del presente comma, qualora questi siano contenuti in prodotti cosmetici regolarmente in commercio in detti Paesi. Sono fatti in ogni caso salvi i divieti e le limitazioni stabiliti dal Ministero della Sanità per esigenze di tutela della salute pubblica.
Legge 94/98, art. 5 c. 1
L’evidenziato va al cuore del problema: il Ministero della Salute (ex – sanità) può vietare sostanze o preparazioni magistrali per tutelare la salute pubblica. Ma è tutto qui? Certo che no…
Perché vengono vietate le preparazioni galeniche a base della sostanza XYZ?
Tra i tanti motivi:
- esiste un rischio per la salute pubblica
- “ce lo chiede l’Europa”
- è più facile vietare tout-court che controllare
I decreti che vietano e limitano le preparazioni galeniche escono quasi sempre nel periodo estivo o natalizio. Da ciò, ecco perché li chiamo “decreti vaselina”
Dr. Marco Ternelli
Le sostanze vietate in galenica sono le stesse dei farmaci industriali?
Logica e giustizia vorrebbero che la risposta a questa domanda fosse si.
La Legge stessa lo impone:
Il Ministro della salute può vietare l’utilizzazione di medicinali, anche preparati in farmacia, ritenuti pericolosi per la salute pubblica, senza che ciò comporti differenziazione tra il medicinale di origine industriale e il preparato magistrale
Tabella 5 Farmacopea Italiana XII ed.
Ovviamente la risposta è NO: ci sono diversi casi (v. oltre) in cui i farmaci galenici a base di certe sostanze sono stati vietati, mentre i farmaci industriali a base delle stesse sostanze non sono vietati o anche solo limitati.
Vediamo dunque tutte le sostanze vietate o limitate nelle preparazioni galeniche magistrali e officinali.

Elenco delle sostanze vietate o limitate in galenica
Ormoni
Pregnenolone
Viene vietata la preparazione con il classico “decreto vaselina” (v. prima) con il Decreto dell’8 Agosto 2022. Ergo, dal 9 Agosto è vietata QUALSIASI PREPARAZIONE galenica a base di pregnenolone.
Anabolizzanti S1 [divieto]
Sono vietati tutti gli steroidi anabolizzanti androgeni (classificazione doping S1): vedi articolo dedicato
DHEA [limite]
Pur essendo classificato come anabolizzante S1, il prasterone o diidroepiandrosterone o DHEA ha subito forti limitazioni e divieti, che potete leggere nel dettaglio sempre in questo articolo dedicato.
Sostanze vietate ad uso dimagrante
Premessa non polemica: se avessero potuto vietare l’acqua ad uso dimagrante lo avrebbero fatto…
Sono vietate:
- Le “7 sorelle” (vedi articolo)
- Efedrina
- Sibutramina
- Fendimetrazina
- Benfluorex
Essendoci molte cose da dire su queste sostanze, è disponibile l’articolo aggiornato (vedi articolo dedicato riepilogativo) per evitare ripetizioni.
Altre sostanze minori vietate
Fenilpropanolamina / norefedrina
È stata vietata con il Decreto 20 maggio 2015 nonostante esista in commercio un medicinale ad uso veterinario, regolarmente vendibile con ricetta. Di fatto, è vietata la preparazione tout-court, anche se per uso veterinario.
Metilrosanilinio cloruro (violetto di genziana)
Ritenuto potenzialmente cancerogeno, nonostante non ci siano segnalazioni ma essendoci altre terapie disponibili (??) è stato vietato anche questo tout-court con il Decreto 1 giugno 2021 del Ministero della Salute.
Ora vi sentite tutti un po’ più sicuri, dite la verità…
Sostanze ad uso vegetale
Sinefrina estratto fino al 10%
La sinefrina pura ad uso dimagrante è vietata.
La polvere di estratto secco titolata, più precisamente estratto di Citrus aurantium L. ssp. amara Engl. purificato ai fini dell’arricchimento in sinefrina con percentuale finale superiore al 10%, è vietata sempre a scopo dimagrante con il Decreto 1 giugno 2021 (ergo, si può usare per preparazioni non a scopo dimagrante, ma per maggiori fino è necessario leggere questo articolo).
Estratti vegetali ad alto titolo
Con 2 circolari (una nel Giugno 2019 e una nel Maggio 2022) il Ministero della Salute, rivolgendosi agli integratori alimentari (ma per riflesso questo si ripercuote ai preparati salutistici realizzati in farmacia): in poche parole
non può essere definito come “estratto” un ingrediente rappresentato di fatto da una singola sostanza rivendicata come “titolo”.
Circolare del Ministero della Salute
In altre parole, con un esempio:
- è consentito utilizzare in galenica (e negli integratori) un estratto di griffonia al 17% in 5 – idrossido triptofano
- NON è consentito utilizzare in galenica (e negli integratori) un estratto di griffonia al 98% in 5 – idrossido triptofano, in quanto di fatto si tratta di 5 idrossido triptofano puro
Domanda: e un estratto di griffonia al 48%? O al 70%? Come capire quando è si, quando è no? Bella domanda…
Aloe, emodina e idrossiantracene
Questo non è un divieto della galenica, quanto un limite posto dall’Unione Europea sugli integratori (quindi anche i prodotti salutistici) tramite il Regolamento 2021/468 che ha inserite alcune sostanze nell’allegato III del Regolamento 1925/2006:
- aloe – emodina e tutte le preparazioni in cui è presente tale sostanza
- emodina e tutte le preparazioni in cui è presente tale sostanza
- preparazioni a base di foglie di specie di Aloe contenenti derivati dell’idrossiantracene
- dantrone e tutte le preparazioni in cui è presente tale sostanza
In pratica: non è consentito al Farmacista preparare officinali / prodotti salutistici con questi componenti.
È però consentita la loro preparazione nei galenici magistrali ossia con ricetta medica, dato che in quel caso il Regolamento non si applica.

Sostanze vietate o limitate… che non lo sono
Come bonus track alla fine di questo articolo, una piccola sezione su alcune sostanze che a torto sono ritenute limitate nella galenica, ma in pratica non lo sono.
Come è possibile? Per esempio per un intervento del Legislatore su prodotti quali gli integratori (quindi libera vendita), mentre i galenici magistrali sono prodotti con ricetta medica.
Monacolina
La monacolina (o monakolina) è stata regolata nel Giugno 2022 ma non con un intervento diretto sulla galenica, quanto da una disposizione Europea (Regolamento n. 2022/860) riguardante gli integratori ossia prodotti di libera vendita, limitando il dosaggio ad un massimo di 3 mg (esclusi) al giorno.
NULLA CAMBIA PER LA GALENICA!
La monacolina non è preparabile come prodotto salutistico, ma solo con ricetta medica dove il Medico, all’atto della prescrizione, deve “solo” riferirsi alla Legge 94/98 (attenzione: non off-label) che consente la prescrizione di sostanze contenute in integratori in commercio all’interno della UE; di conseguenza, il medico può prescrivere la monacolina a qualsiasi dosaggio ritenga necessario (fatti salvi quanto disposto in caso di iperdosaggi dalla Tabella 8 della FU Italiana).
Potete lasciare nei commenti domande o considerazioni sulle sostanze vietate in galenica o limitate dal Ministero della Salute.

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Sostanze vietate in galenica: l’elenco completo al 2024 sembra essere il primo su Farmagalenica.
]]>L'articolo Potassio ioduro compresse, farmaco contro iodio radioattivo sembra essere il primo su Farmagalenica.
]]>Pur essendo un medicinale usato da tempo e realizzato storicamente come galenico, torna spesso alla ribalta in caso di emergenza nucleare, come nell’esplosione del reattore di Fukushima o nella recente guerra in Ucraina.
Nell’articolo andremo a vedere come le farmacie galeniche lo producono, quali sono le caratteristiche, i dosaggi, la legislazione per la vendita in Italia, eccetera.
A cosa serve il potassio ioduro
Il potassio ioduro è un sale inorganico dello iodo che ha diverse funzioni, alcune fondamentali, quali il
- trattamento dell’ipertiroidismo
- coadiuvante tecnico per la solubilizzazione dello iodio
- protezione in caso di somministrazione di radiofarmaci
Tra gli usi riconosciuti, quello di interesse in questo contesto è quello di saturare la tiroide di iodio non radioattivo impedendo così la fissazione di quello radioattivo nella tiroide stessa.
Per una trattazione estesa su questa sostanza, è disponibile questo articolo.
“Iodio” e “potassio ioduro” sono due cose molto diverse
Attenzione a non confondere lo iodio (simbolo chimico I) con il potassio ioduro (simbolo KI). Sono 2 cose diverse!
È molta la confusione attorno alle “compresse di iodio” e “compresse di potassio ioduro”.
Lo iodio infatti è un elemento necessario al nostro corpo, presente (es.) nel sale (sale iodato) ed è presente da solo o associato ad altri elementi naturali (vitamine, microelementi, ecc…) come integratore alimentare. NON SERVE A NULLA per quanto trattato in questo articolo, se non a fornire un supplemento di iodio all’organismo nell’ordine di microgrammi (la millesima parte del milligrammo).
Tenete infatti presente che le dosi di iodio fornite con le compresse di potassio ioduro sono nell’ordine di milligrammi, ossia mille volte di più rispetto ai microgrammi.
130 mg (milligrammi) di potassio ioduro contengono 100 mg (milligrammi) di iodio
Un conto è il potassio ioduro, un altro lo iodio
Nel resto dell’articolo viene spiegato tutto. Buona lettura.
Dove è venduto il potassio ioduro capsule o compresse in Italia
In Italia non esiste un medicinale realizzato industrialmente, ossia preparato dall’industria farmaceutica e immediatamente disponibile all’acquisto delle farmacie italiane. È quindi ritenuto un farmaco orfano.
Gli unici modi, quindi, di poter ottenere un farmaco a base di potassio ioduro sono:
- acquistarlo dallo Stabilimento Chimico Farmaceutico Militare che però lo fornisce solamente in caso di emergenze e su richiesta del Ministero della Salute, degli Ospedali e dell’Istituto Superiore di Sanità
- importarlo dall’estero
- richiederne la fabbricazione ad una farmacia Galenica italiana (l’articolo che stai leggendo).
“potassio ioduro” o “ioduro di potassio” sono la stessa cosa
Solo nomenclatura
Caratteristiche della preparazione galenica di potassio ioduro compresse
Il Farmacista Galenista può infatti disporre della materia prima purissima (ioduro di potassio) e utilizzarla per la preparazione di diversi medicinali quali
- tintura di iodio
- iodio soluzione cutanea
- ungenti con iodio
- potassio ioduro compresse o capsule
- potassio ioduro in gocce
- soluzione di Lugol
- …
Il Farmacista, in base all’indicazione di una farmacopea o di una ricetta medica, realizza quindi un farmaco nella dose, forma e quantità richiesta.
A tal proposito, essendo un medicinale fabbricato partendo da 0, la possibilità di avere un Farmacista che realizza potassio ioduro compresse permette indiscutibili benefici:
- possibilità di disporre di un medicinale altrimenti non reperibile in commercio
- possibilità di ottenere un medicinale in qualsiasi forma farmaceutica, non solo compresse: sciroppi, gocce, capsule, creme, ecc…
- disponibilità in caso di emergenza di un antidoto
- possibilità di realizzare qualsiasi dosaggio sia necessario (es. 10mg, 65mg, 99mg, 130mg, ecc…)
- possibilità di realizzare qualunque quantità (es. 10 compresse, 100, 1000, ecc…)
- brevi tempi di realizzazione (solitamente due o tre giorni lavorativi)
Posologia ed effetti collaterali del potassio ioduro comprese
Chiarito che il Farmacista può realizzare qualsiasi dosaggio di potassio ioduro compresse richiesto dal Medico, solitamente i dosaggi richiesti e più utilizzati sono:
- 65 mg di potassio ioduro ossia circa 50 milligrammi (non microgrammi) di iodio
- 100 mg di potassio ioduro circa 75 milligrammi (non microgrammi) di iodio
- 130 mg di potassio ioduro ossia circa 100 milligrammi (non microgrammi) di iodio
ATTENZIONE: SOLO il MEDICO conosce il dosaggio adatto per ogni paziente. I dosaggi di seguito riportati sono a titolo esemplificativo e non vanno intesi come consulto medico.
Stando alla letteratura su Pubmed (es. qui e qui) il dosaggio giornaliero da assumere, prima che si sia verificata l’emissione di materiale radioattivo è di una compressa al giorno da 130 mg o due insieme da 65 mg, per tutto il periodo indicato dal Medico.
Le compresse (o capsule) vanno deglutite con un po’ di acqua, ma possono essere sbriciolate (sapore abbastanza sgradevole) in succhi di frutta, yogurt, marmellata, ecc… In essi possono essere disperse anche gocce.
Maggiori indicazioni su posologie e dosaggi sono disponibili qui.
Infine, come tutti i medicinali, è bene ricordare che se assunto senza necessità terapeutica o senza indicazione medica, il potassio ioduro può causare danni anche gravi alla tiroide e non solo.
Integratori di potassio ioduro? Decisamente non sono quel che sembra
Esistono integratori di “potassio ioduro compresse” che possono essere acquistati senza ricetta medica e al consumatore poco attendo potrebbero apparire come la soluzione rapida ed immediata. Non è così: sono sì compresse che contengono potassio ioduro, ma ad una dose fino a 500 volte inferiore a quella necessaria per la protezione contro radiazioni.
Potreste trovare integratori che dichiarano “compresse da 120 mg” e pensare “bhe, è quasi come i 130mg che ho letto sopra, quindi va bene”. SBAGLIATO.
120 mg è il peso totale della compressa, di tutte le polveri presenti (eccipienti, potassio ioduro, rivestimento), ma il contenuto reale di iodio è solo di 0,225 mg (225 microgrammi).
Ricapitolando: assumendo una compressa di un integratore al potassio ioduro compresse KI che pesa 120 mg (eccipienti + potassio ioduro) state assumendo una dose di iodio da 0,225 mg anziché 65 o 130 mg. È evidente come non serva all’uso di cui si parla in questo articolo, ma solo come, appunto, integratore.
Legislazione per la vendita di potassio ioduro compresse
Il potassio ioduro compresse può essere preparato dal farmacista sia come farmaco magistrale (cioè sul momento) che come farmaco officinale (prepararlo e tenerlo pronto) essendo riportato in FU Italiana XII edizione.
ATTENZIONE: la vendita del potassio ioduro richiede SEMPRE ricetta medica, indipendentemente che sia preparato come magistrale sia come officinale.
La preparazione di potassio ioduro ricade in Tabella 4 della FU Italiana XII (non è “veleno” essendo sale inorganico dello iodio) edizione e richiede quindi una ricetta medica ripetibile valida 6 mesi per un massimo di 10 preparazioni.
Tale ricetta può essere redatta da qualsiasi Medico (di medicina generale, specialista, ospedaliero, privato, ecc…).
Al fine di agevolare la comprensione di quanto appena riportato, si allega un facsimile esplicativo della ricetta medica.
Costi e tariffazione del potassio ioduro compresse
Il potassio ioduro preparato come magistrale (cioè preparato estemporaneamente) ha un prezzo calcolato imposto con Tariffa Nazionale dei Medicinali. Nel caso di compresse, per dare un esempio
- 30 compresse di potassio ioduro da 65 mg = CIRCA 40€
- 60 compresse di potassio ioduro da 65 mg = CIRCA 55 €
- 30 compresse di potassio ioduro da 130 mg = CIRCA 49 €
Non è quindi il Farmacista che decide il prezzo liberamente per il farmaco magistrale, ma deve sottostare a queste tariffe ministeriali. Ovviamente al variare della quantità, varierà il prezzo finale (più materia prima necessaria = più costi).
Se invece il potassio ioduro compresse è preparato come officinale (cioè in lotto, da tenere subito pronto), il prezzo viene fissato liberamente dal Farmacista.
Come tutti i farmaci galenici, anche il potassio ioduro compresse è fiscalmente detraibile.

Per trovare e visualizzare quali Farmacie di Farmagalenica sono in grado di preparare e vendere il farmaco galenico potassio ioduro compresse o capsule, consultare il motore di ricerca disponibile su www.cercagalenico.it (si aprirà una nuova pagina).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Potassio ioduro compresse, farmaco contro iodio radioattivo sembra essere il primo su Farmagalenica.
]]>L'articolo Estratto di cannabis Farmalabor 15% THC, olio galenico sembra essere il primo su Farmagalenica.
]]>Dal 15 Dicembre 2021 a tutto questo si affianca un estratto concentrato al 15% in THC che il Farmacista deve diluire in proporzioni stechiometriche per ottenere la concentrazione di THC voluta dal medico: l’ estratto di cannabis Farmalabor 15% THC, unico rivenditore ad oggi autorizzato in Italia (alla data dell’ultimo aggiornamento dell’articolo).
Questo articolo è dedicato a coloro che vogliono informarsi su questa novità nel panorama della cannabis medica terapeutica in Italia: sapere come prepararlo, come acquistarlo, che ricetta serve, i costi, prezzi, differenze, eccetera.
È un articolo semplice da leggere nonostante la lunghezza ed è stato diviso in sezioni per agevolare il lettore che volesse approfondire un contenuto specifico.
Buona lettura, se avete domande ci sono i commenti a fondo articolo.
Estratto di cannabis (concentrato) di Farmalabor
Si tratta di estratto di cannabis concentrato al 15% di THC (ossia 150mg/g) che è stato prodotto mediante estrazione in etanolo (che viene poi completamente rimosso) da una azienda europea autorizzata e viene successivamente importato e confezionato dalla Farmalabor SRL che è autorizzata dall’AIFA alla ripartizione e produzione lotti.
Dal punto di vista regolatorio non è un prodotto finito destinato al pubblico, ma una materia prima GMP che il Farmacista Galenista deve utilizzare nel laboratorio della Farmacia Galenica per preparare un olio di cannabis alla concentrazione desiderata dal Medico.
L’ estratto di cannabis Farmalabor 15% THC è una materia prima per preparare l’olio di cannabis con THC in farmacia
La preparazione avviene diluendo l’estratto in opportuni eccipienti quali:
- tensioattivi
- olio vegetale (MCT, olio extravergine di oliva, olio di oliva, eccetera)
Quali differenze come concentrazione e composizione dall’olio di Bedrocan o Pedanios rispetto all’ estratto di cannabis Farmalabor?
Ogni infiorescenza di cannabis medica è unica in quanto derivata da una genetica proprietaria dell’azienda (es. Bedrocan BV, Aurora, Canopy, ecc…) che la produce.
Ogni olio di cannabis è quindi diverso se preparato con infiorescenze di cannabis diverse.
Per quanto riguarda la composizione dell’estratto di cannabis Farmalabor 15% THC in terpeni e altri cannabinoidi (es. THCA, CBG, CBN, ecc…) queste sono le informazioni disponibili da certificato di analisi:
- CBD: max 1%
- CBN: max 0,5%
- THCA: ??
Si sottolinea che le specifiche (e i relativi contenuti in cannabinoidi, acido o neutri) sono conformi alla monografia tedesca Cannabis Extractum.
Di seguito, una analisi in HPLC-UV dell’estratto puro:
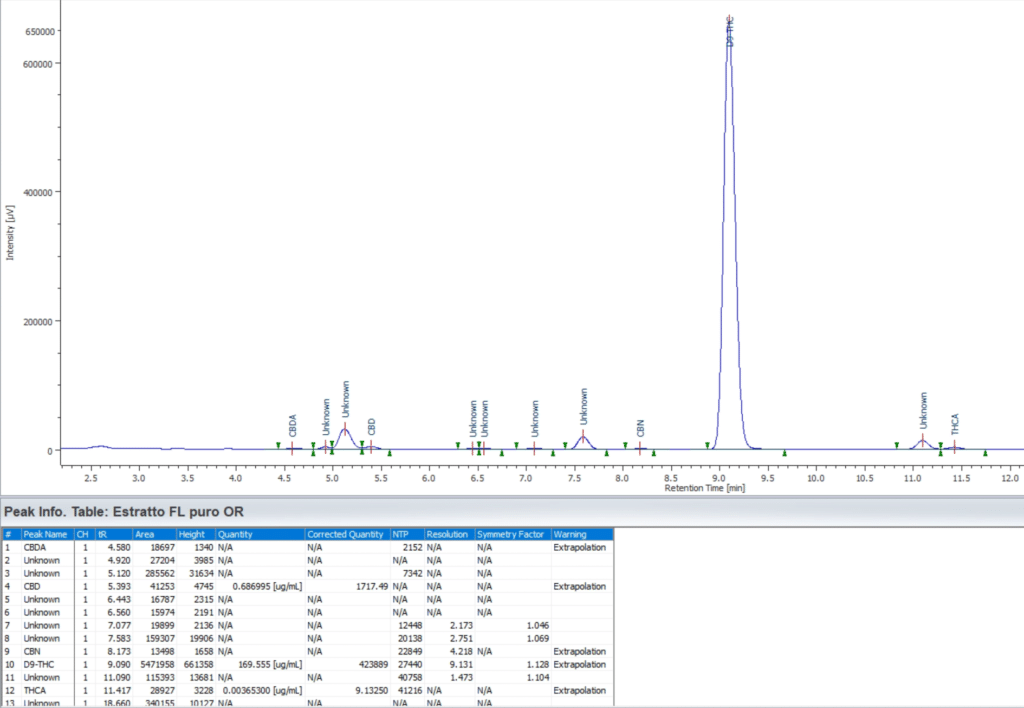
Sativa o Indica?
L’ estratto di cannabis Farmalabor dovrebbe essere ottenuto da varietà ibride di infiorescenze (e foglie?), ma attualmente non sono disponibili informazioni più precise.
Leggere la sezione tecnica più avanti per maggiori informazioni.
L’estratto di cannabis Farmalabor NON è un isolato, cioè non è solo THC, ma contiene anche altri cannabinoidi e sostanze della cannabis
È “solo” più concentrato
Diluendo opportunamente l’estratto di cannabis 15% THC, è possibile ottenere oli analoghi all’olio di Bedrocan o Pedanios, ma anche Bediol o FM2 (aggiungendo CBD cristalli).
“Analoghi” significa che avranno la stesso identica quantità di THC e/o CBD, che avranno diversa composizione in terpeni, cannabinoidi, eccetera.
Questo estratto di cannabis Farmalabor NON è ottenuto da Bedrocan o Pedanios, ma da altre infiorescenze. Come già detto, è un analogo, non identico.
In particolare, se parliamo di concentrazione del THC all’interno dell’olio finale (quello che il paziente acquisterà e assumerà) occorre precisare una cosa importantissima:
- gli oli di cannabis con THC realizzati nelle Farmacie Galeniche negli ultimi 8 anni in Italia, hanno una concentrazione che varia dallo 0,5% p/v (cioè 5 mg/ml) ad un massimo di circa 1,8% p/v (cioè 18 mg/ml)
- ottenere concentrazioni di THC maggiori al 2,0% con varietà come il Bedrocan o Pedanios sarebbe in teoria possibile, ma inutile: l’olio ottenuto sarebbe poco dosabile, alto rischio di effetti collaterali, difficoltà a costruire tolleranza.
- allo stesso modo, un olio di cannabis con concentrazioni > 2% THC ottenuto dall’estratto di cannabis Farmalabor non ha molto senso.
Autorizzazioni
L’AIFA ha autorizzato Farmalabor alla produzione e al rilascio di un nuovo principio attivo farmaceutico (ESTRATTO DI CANNABIS 15% THC), con rilascio del GMP, Certificate No: IT- API/158/H/2021.
Il Ministero della Salute, Ufficio Centrale Stupefacenti, con D.D. n°392/2021 del 18/10/2021 ha autorizzato la Farmalabor alla manipolazione dell’ESTRATTO DI CANNABIS 15% THC.

Consigli pratici per il Farmacista per la preparazione dell’olio di cannabis dall’estratto di cannabis Farmalabor 15% THC
Nota: paragrafo un po’ tecnico, per Farmacisti e Medici. Se non vi interessa passate pure al successivo. Ma è interessante, sappiatelo 
Prima di tutto, la regola madre da cui tutto dipende: essendo una soluzione oleosa, la densità non è 1 (circa 0,964, ma varia da lotto a lotto) perciò 1 g di estratto NON è uguale a 1 ml di estratto.
Da fine 2022, l’estratto di cannabis Farmalabor 15% THC viene venduto in millilitri (non più in grammi come avveniva fin dall’inizio, fine 2021). È bene quindi intestare una nuova pagina di registro in cui caricare i nuovi estratti gestiti in ml. Ovviamente, il Farmacista Gallerista può terminare di utilizzare le “vecchie versioni” caricate ancora in g.
Versione vecchio estratto: 1 g (NON 1 ml) di estratto di cannabis Farmalabor 15% contiene 150mg di THC*.
Valore teorico, ogni lotto avrà un valore preciso (es. 160mg) come da Certificato di analisi
Versione nuovo estratto: 1 ml (NON 1g) di estratto di cannabis Farmalabor 15% contiene 150mg di THC*.
Prescrizioni, grammi e millilitri
A seconda dell’estratto di cui si dispone, si possono aver da gestire conversioni tra grammi e millilitri o viceversa.
Per questo è necessario che ogni volta il Farmacista effettui la conversione da ml a g (o da grammi a millilitri) tramite la densità fornita sul certificato di analisi.
A volte il risultato di conversione sarà di cifre precise, altre volte si porterebbero generare cifre infinitesimali che, causa approssimazione matematica, dovranno essere sapientemente registrate (e annotate) onde evitare errori di giacenza sul Registro di entrata e uscita stupefacenti.
Per facilitare le conversioni, Farmalabor mette a disposizione questo documento PDF per facilitare le operazioni.
Questo invece un esempio di certificato di analisi:
Diluizioni: come ottenere olio di cannabis partendo dall’estratto 15% THC
Di seguito è riportata una tabella con le principali diluizioni dell’estratto di cannabis 15% THC per ottenere olio di cannabis a diverse concentrazioni di THC a diversi volumi.
Fondamentale: oltre a miscelare, prestare molta attenzione a verificare la completa dissoluzione dell’estratto nell’eccipiente. Se ciò non avvenisse completamente, si avrebbe un estratto a concentrazione non uniforme, con potenziali problemi per il paziente.
Quello che va fatto è:
- PESARE con bilancia i GRAMMI di estratto
- portare a VOLUME mediante siringa, cilindro graduato, pallone o matraccio (ASSOLUTAMENTE NO direttamente nel contenitore finale) con l’eccipiente finale
Nota MOLTO bene: per evitare il problema delle approssimazioni infinitesimali, tutti i grammi di estratto sono stati approssimati all’unità in modo da semplificare la prescrizione, pesata e scarico. Pertanto, la concentrazione in THC indicata può subire leggere variazioni entro 5% del dichiarato (es. 5 mg/ml +-5%), anche in base alla reale concentrazione del lotto.
Disclaimer: è responsabilità del Farmacista assicurarsi che i calcoli stechiometrici, nonché i valori del certificato di analisi siano corretti per assicurarsi del contenuto finale di THC nell’olio. Farmagalenica SRL esclude ogni responsabilità per errori o imprecisioni dovessero derivare dall’uso della presente tabella.
Calcolatore dosi personalizzate
Oltre alla tabella sopra riportata, si fornisce questo calcolatore online per permettere un rapido calcolo della quantità in grammi di estratto necessario (da pesare o indicare in ricetta) rispetto al volume finale desiderato di olio.
Il calcolatore delle dosi personalizzate è fornito ad uso dimostrativo; si esclude ogni responsabilità per eventuali errori in quanto la responsabilità del calcolo è sempre del Farmacista / Medico.
Eccipienti da usare
L’estratto di cannabis Farmalabor 15% THC è realizzato in Labrafac Lipophile WL1349 (abbrev. Labrafac), ossia l’estratto, una volta realizzato, è stato diluito al 15% in una massa costituita da una materia prima GMP a base di MCT, il Labrafac appunto.
Lipophile WL1349 (abbrev. Labrafac), ossia l’estratto, una volta realizzato, è stato diluito al 15% in una massa costituita da una materia prima GMP a base di MCT, il Labrafac appunto.
È quindi consigliato utilizzare lo stesso solvente per diluire l’estratto e realizzare l’olio di cannabis.
Confezionamento
Come per l’olio di cannabis ottenuto da infiorescenze, è necessario utilizzare un flacone contagocce, solitamente un flacone in vetro ambrato di classe III con tappo child-proof (a prova di bambino) cui può essere aggiunto un riduttore e siringa graduata per la somministrazione.
Conservazione
L’estratto di cannabis Farmalabor così come l’olio di cannabis realizzato con esso, va conservato al di sotto dei 25°C, ma il produttore ne raccomanda la conservazione in frigorifero tra 2 e 8°C.
Scadenza
La shelf life dell’estratto di cannabis 15% THC (quindi la materia prima da lavorare) ha un scadenza di circa 12 mesi. ATTENZIONE PERO’: l’olio di cannabis realizzato con esso se conservato in frigorifero può avere una scadenza massima di 6 mesi, ma ancora non sono disponibili studi sulla stabilità definitiva. È ipotizzabile un periodo di qualche mese in frigorifero.

Vantaggi e svantaggi
Ci sono diverse peculiarità nell’uso di un estratto di cannabis medica concentrato come quello della Farmalabor; come tutte le cose alcune sono positive, altre negative. E ci sono pure considerazioni neutre.
Vediamole velocemente, ma approfonditamente.
Vantaggio: disponibilità di olio con THC in carenza di infiorescenze
Innegabilmente in questo periodo di carenza di cannabis infiorescenze anche per preparare olio di cannabis terapeutico in Farmacia o cartine da decotto o vaporizzare, avere a disposizione una alternativa permette di sopperire alla carenza.
Vale la piena chiedersi se, fatte le opportune valutazioni, questo vantaggio rimarrà tale in un ipotetico futuro in cui le infiorescenze dovessero tornare (e lo saranno entro il 2023) abbondantemente disponibili.
Vantaggio: semplicità di preparazione e meno tempo
Realizzare un olio di cannabis da infiorescenze nel Laboratorio Galenico della Farmacia richiedere da 1 a 2 giorni a seconda della metodica da utilizzare; in questo caso si tratta di miscelare “semplicemente” (virgolette perché di semplice non c’è mai nulla nella attività di un Farmacista Galenista, i problemi sono sempre dietro l’angolo) l’estratto con gli eccipienti.
Il punto fondamentale è che il Farmacista Galenista si assicuri che la massa dell’ estratto di cannabis Farmalabor sia perfettamente disciolta negli eccipienti, evitando la formazione di “sacche” di olio più concentrate e altre meno concentrate.
Vantaggio: standardizzazione = niente analisi HPLC
L’ estratto di cannabis Farmalabor è già titolato al 15% di THC, ossia è noto che ogni ml di estratto contiene 150mg di THC. Per questo, facendo una diluizione precisa, con pochi calcoli stechiometrici il Farmacista è in grado di indicare la concentrazione finale di THC contenuta in
- 1 ml finale di olio di cannabis
- 1 goccia di olio di cannabis
Esempio: sapendo che in 1 g sono presenti 150mg di THC come da certificato di analisi, avendo messo 5 g di estratto e portato a volume di 50 ml con olio di MCT, significa che in 1 ml finale di olio di cannabis saranno presenti 15 mg di THC. Inoltre, sapendo che 1 ml di olio sono circa 28 gocce, significa che ogni goccia conterrà circa 0,5 mg di THC.
Vantaggio: costo finale minore al paziente per oli analoghi a basso THC
In base alla Tariffa Nazionale dei Medicinali, il Farmacista non può decidere in autonomia il costo di un farmaco galenico, ma tenersi ad essa per calcolare il prezzo finale.
Per quanto riguarda i costi:
Vecchi flaconi in grammi
- 50 g: 26,5 €/g + IVA
- 900 g: 17,5 €/g + IVA
Nuovi flaconi in millilitri (ml)
- 50 g: 16,625 €/ml + IVA
- 900 ml = 16,15 €/ml + IVA
Come già stato detto, ogni singolo millilitro (ossia 150mg di THC) di estratto di cannabis Farmalabor 15% ha un costo netto di acquisto di sui 16 € + IVA che è più alto rispetto agli estratti preparati in farmacia partendo da infiorescenze.
Nella tabella seguente sono elencati alcuni esempi di prezzi (a parità di THC e quantitativo finale) per far capire le differenze di prezzo tra il prezzo al paziente di un estratto realizzato farmacia da infiorescenze e un olio realizzato diluendo l’ estratto di cannabis Farmalabor.
Vecchi flaconi in grammi: costi al paziente
| CONCENTRAZIONE | VOLUME | Prezzo finale al paziente (IVA 10% inclusa) | |
| Bediol / FM2 Olio 5g (Metodica Romano & Hazekamp) | 5 mg/ml THC | 50 ml | CIRCA 95€ |
| Bediol / FM2 Olio 5g (Metodica Ternelli / Calvi) | 5 mg/ml THC | 50 ml | CIRCA 119€ |
| Olio di cannabis diluito Farmalabor analogo Bediol / FM2 (1,5 ml di estratto necessari) | 5 mg/ml THC | 50 ml | CIRCA 101€ |
Nuovi flaconi in millilitri: costi al paziente
| CONCENTRAZIONE | VOLUME | Prezzo finale al paziente (IVA 10% inclusa) | |
| Bediol / FM2 Olio 5g (Metodica Romano & Hazekamp) | 5 mg/ml THC | 50 ml | CIRCA 95€ |
| Bediol / FM2 Olio 5g (Metodica Ternelli / Calvi) | 5 mg/ml THC | 50 ml | CIRCA 119€ |
| Olio di cannabis diluito Farmalabor analogo Bediol / FM2 (1,5 ml di estratto necessari) | 5 mg/ml THC | 50 ml | CIRCA 85€ |
Svantaggio: costo finale maggiore al paziente per oli analoghi ad alto THC
Sempre base alla Tariffa Nazionale dei Medicinali, il Farmacista non può decidere in autonomia il costo di un farmaco galenico, ma tenersi ad essa per calcolare il prezzo finale. Come già stato detto, ogni singolo millilitro (ossia 150mg di THC) di estratto di cannabis Farmalabor 15% ha un costo netto di acquisto di sui 16 € + IVA che è più alto rispetto agli estratti preparati in farmacia partendo da infiorescenze..
Nella tabella seguente sono elencati alcuni esempi di prezzi (a parità di THC e quantitativo finale) per far capire le differenze di prezzo tra il prezzo al paziente di un estratto realizzato farmacia da infiorescenze e un olio realizzato diluendo l’ estratto di cannabis Farmalabor:
| CONCENTRAZIONE | VOLUME | Prezzo finale al paziente (IVA 10% inclusa) | |
| Bedrocan / Pedanios Olio 5g (Metodica Romano & Hazekamp) | 15 mg/ml THC | 50 ml | CIRCA 95€ |
| Bedrocan / Pedanios Olio 5g (Metodica Ternelli / Calvi) | 15 mg/ml THC | 50 ml | CIRCA 119€ |
| Olio di cannabis diluito Farmalabor analogo Bedrocan / Pedanios (5 ml di estratto necessari) [23,30 €/g] | 15 mg/ml THC | 50 ml | CIRCA 169€ |
| Olio di cannabis diluito Farmalabor analogo Bedrocan / Pedanios (10 ml di estratto necessari) [23,30 €/g] | 15 mg/ml THC | 100 ml | CIRCA 289€ |
Nuovi flaconi in millilitri: costi al paziente
| CONCENTRAZIONE | VOLUME | Prezzo finale al paziente (IVA 10% inclusa) | |
| Bedrocan / Pedanios Olio 5g (Metodica Romano & Hazekamp) | 15 mg/ml THC | 50 ml | CIRCA 95€ |
| Bedrocan / Pedanios Olio 5g (Metodica Ternelli / Calvi) | 15 mg/ml THC | 50 ml | CIRCA 119€ |
| Olio di cannabis diluito Farmalabor analogo Bedrocan / Pedanios / Billy Buttons (5 ml di estratto necessari) | 15 mg/ml THC | 50 ml | CIRCA 137€ |
| Olio di cannabis diluito Farmalabor analogo Bedrocan / Pedanios / Billy Buttons (10 ml di estratto necessari) | 15 mg/ml THC | 100 ml | CIRCA 230€ |
Svantaggio: costo al Farmacista
In base alla Tariffa Nazionale dei Medicinali e tenuto conto che l’estratto di cannabis materia prima GMP non è contenuto nell’allegato A, la sostanza/materia prima deve essere venduta al prezzo di costo (0% ricarico). In altre parole, per il Farmacista pagare 1 g di estratto (es.) 5€, 27 € o 50€ non cambia in termini di guadano: il guadagno che avrà su questo estratto è sempre lo stesso ossia 0€.
Per le sostanze non comprese nell’allegato A si applica il prezzo di acquisto, al netto dell’IVA, del quale deve essere conservata prova documentale.
Art. 5, Tariffa Nazionale dei Medicinali, la “grande” conquista del 2017
Di contro, il farmacista dovrà sostenere ingenti costi di acquisto legati all’elevato costo della materia prima e alle pezzature disponibili (notare che i prezzi e tagli possono essere soggetti a variazioni: far riferimento al fornitore per le quotazioni aggiornate):
- 50 g di estratto di cannabis Farmalabor 15% (a 17,50€/g) = 875€ + IVA 22% = 1.067,5€
- 900 g di estratto di cannabis Farmalabor 15% (a 17,00€/g) = 15.300€ + IVA 22% = 18.666€
- –
- 50 ml di estratto di cannabis Farmalabor 15% (a 16,625€/ml) = 831€ + IVA 22% = 1.014,13€
- 900 ml di estratto di cannabis Farmalabor 15% (a 16,15€/ml) = 14.535€ + IVA 22% = 17.732€
Considerando che chi ha aggiornato la Tariffa (…) ha pensato di non distinguere il carico di lavoro nel preparare piccoli flaconi (es. 50 ml) e grandi flaconi (es. 200ml), il ricavo economico del Farmacista è sempre lo stesso ed è rappresentato esclusivamente dalla somma dei diritti addizionali di miscele di olii più i costi di lavorazione, per un ricavo totale di circa 25€.
Indipendentemente dalla quantità preparata.
Nella tabella seguente è riportato il confronto sul ricavo (al netto dell’IVA 10%) tra gli estratti di cannabis realizzati in Farmacia da infiorescenze e per diluizione dell’estratto di cannabis Farmalabor:
| CONCENTRAZIONE | VOLUME | TEMPO DI LAVORO | COSTI AL FARMACISTA | RICAVO (netto IVA 10%) | |
| Bedrocan / Pedanios Olio 5g (Metodica Romano & Hazekamp) | 15 mg/ml THC | 50 ml | 4 – 8 h | CIRCA 50€ | CIRCA 40€* |
| Bedrocan / Pedanios Olio 5g (Metodica Ternelli / Calvi) | 15 mg/ml THC | 50 ml | 24 – 48 h | CIRCA 60€ | CIRCA 50€* |
| Olio di cannabis diluito Farmalabor analogo Bedrocan / Pedanios (5 ml di estratto necessari) [26,20 €/g] | 15 mg/ml THC | 50 ml | 1,5 h | CIRCA 140€ | CIRCA 30€ |
| Olio di cannabis diluito Farmalabor analogo Bedrocan / Pedanios (5 ml di estratto necessari) [23,30 €/g] | 15 mg/ml THC | 50 ml | 1,5 h | CIRCA 120€ | CIRCA 30€ |
| Bedrocan / Pedanios Olio 5g (Metodica Romano & Hazekamp) | 15 mg/ml THC | 100 ml | 4 – 8 h | CIRCA 85€ | CIRCA 55€* |
| Bedrocan / Pedanios Olio 5g (Metodica Ternelli / Calvi) | 15 mg/ml THC | 100 ml | 24 – 48 h | CIRCA 100€ | CIRCA 70€* |
| Olio di cannabis diluito Farmalabor analogo Bedrocan / Pedanios (10 ml di estratto necessari) [26,20 €/g] | 15 mg/ml THC | 100 ml | 1,5 h | CIRCA 295€ | CIRCA 30€ |
| Olio di cannabis diluito Farmalabor analogo Bedrocan / Pedanios (10 ml di estratto necessari) [23,30 €/g] | 15 mg/ml THC | 100 ml | 1,5 h | CIRCA 260€ | CIRCA 30€ |
Svantaggio: non rimborsato da tutto il SSN o SSR
Pur parlando sempre di cannabis, questo estratto rappresenta una novità in termini assoluti, quindi a differenza degli estratti di cannabis preparati in farmacia (già rimborsati), in questo caso l’olio di cannabis ottenuto da questo estratto di cannabis Farmalabor non è ad oggi mutuabile in diverse Regioni: ogni singola Regione dovrà emettere un nuovo atto normativo per riconoscerne la mutuabilità (gratuità).
Ci sono però Regioni che ad oggi già concedono gratuitamente (mutabile) l’estratto e sono:
- Emilia Romagna
- Lombardia
- Liguria
- Marche
- Campania
- Puglia
- Toscana
- Piemonte
- Sicilia
- Friuli Venezia Giulia
- Veneto
Le domande a cui rispondere sono:
- le Regioni faranno queste delibere?
- QUANDO lo faranno?
- dati i costi molto più elevati, è sensato pensare che molte cercheranno di “prendere tempo” per evitare aggravi economici delle casse Regionali?
Rilordate che i tempi tecnici sono sempre mesi che diventano anni in alcuni casi.
Svantaggio: niente THCA
Non risulta essere presente se non in tracce il THCA (THC acido), il precursore del THC. Diversi studi presenti su Pubmed (ad esempio qui e qui) hanno evidenziato come anche il THCA possieda attività terapeutiche e svolga dunque una azione importante.
Nell’estratto risultano tracce di THCA, mentre negli estratti realizzati in farmacia da infiorescenze esso è presente in concentrazioni variabili a seconda del metodo, ma comunque a dosi importanti.
Potrà capitare quindi che una preparazione di cannabis con solo THC abbia un effetto diverso da una con THC e THCA.
Ultima considerazione: unica fonte di THC
La cannabis non è THC. Il THC non è cannabis.
Immaginando un futuro in cui gli estratti saranno solo come questo (cioè non più preparati in Farmacia partendo dalle infiorescenze), di fatto vorrebbe dire addio alla personalizzazione della varietà di cannabis da utilizzare: se serve un olio con THC questo è, prendere o lasciare.
Questo potrebbe cambiare se in futuro ci fossero più estratti, di più varietà. Ma non abbiamo la sfera di cristallo..
Domande frequenti (FAQ) sull’olio di cannabis estratto di cannabis Farmalabor
Sono almeno i seguenti:
– pesata
– misurazione volumetrica
– miscelazione
– dissoluzione
In alcune circostanze (es. aggiunto di altri attivi) può essere applicato anche:
– riscaldamento
– sonicazione
– raffreddamento
– ecc…
per un totale minimo di 4 operazioni tecnologiche a preparazione.
DIFFIDATE da chi sostiene ve ne siano meno.
Certamente, il Medico può indicare l’aggiunta di cristalli di CBD nell’olio per ottenere qualsiasi rapporto di THC e CBD desiderato, esattamente come già avveniva con gli estratti realizzati in Farmacia partendo da infiorescenze.
Ad esempio, è possibile miscelare l’estratto di THC e aggiungere CBD per ottenere un olio di cannabis analogo al Bediol o FM2.
Poiché tutte le registrazioni a livello ministeriale e del fornitore sono in grammi, va registrato in GRAMMI.
In ogni caso bisogna prestare molta attenzione quando si prelevano millilitri e vanno convertiti in grammi. L’errore di giacenza è dietro l’angolo…
La tariffazione segue miscele di olii (punto 3).
NO soluzioni.
NO estratti e tinture.
Normativa per la vendita e acquisto dell’ estratto di cannabis Farmalabor
L’olio di cannabis può essere prescritto sia per uso umano che per uso veterinario.
Uso umano
Trattandosi di una preparazione galenica, per l’acquisto dell’estratto di cannabis Farmalabor diluito alla concentrazione desiderata, serve una ricetta non ripetibile valida 30 giorni escluso quello di emissione, per una sola preparazione (si tratta di un farmaco galenico stupefacente e psicotropo).
Tutte le prescrizioni di olio di cannabis da estratto di cannabis Farmalabor sono SEMPRE OFF-LABEL
Tale ricetta può essere redatta da qualsiasi medico e sempre in OFF LABEL (come per le ricette di infiorescenze di cannabis) secondo l’art. 5 della Legge 94/98 (“Di Bella”) e deve prevedere almeno:
- data di redazione
- timbro (o intestazione) del Medico
- firma del Medico
- codice numerico o alfanumerico + motivazione della prescrizione
- quantità di estratto di cannabis Farmalabor 15% THC in grammi
- quantità e qualità di eccipienti (es. MCT o olio di oliva o Labrafac)
- (non obbligatoria ma consigliata) posologia
Per semplificarne la comprensione, si rendono disponibili a scopo didattico i seguenti esempi facsimile uso umano in PDF con diverse concentrazioni nel formato da 50 ml (il più usato) che possono essere scaricati, ricordando che il Medico può personalizzare la concentrazione o gli eccipienti a qualsiasi dosaggio e tipo, secondo le specifiche esigenze del paziente:

Uso veterinario dell’ estratto di cannabis Farmalabor
Trattandosi di una preparazione galenica, per l’acquisto dell’estratto di cannabis Farmalabor diluito alla concentrazione desiderata, serve una ricetta veterinaria non ripetibile valida 30 giorni escluso quello di emissione, per una sola preparazione. Essendo un farmaco galenico stupefacente e psicotropo va prescritto con ricetta REV.
Tale ricetta può essere redatta da qualsiasi medico veterinario in base al quanto disposto dall’art. 84 del Dlgs 193/2006 e solo per PET o nDPA (animali da compagnia quali cani e gatti, detti anche non destinati alla produzione di alimenti); la ricetta veterinaria elettronica dovrà riportare:
- data di redazione
- timbro (o intestazione) del Medico Veterinario
- firma del Medico Veterinario
- nome, cognome e indirizzo del proprietario dell’animale
- quantità di estratto di cannabis Farmalabor 15% THC in grammi
- quantità e qualità di eccipienti (es. MCT o olio di oliva o Labrafac)
- posologia (obbligatoria)
Per semplificarne la comprensione, si rendono disponibili a scopo didattico i seguenti esempi facsimile uso veterinario in PDF con diverse concentrazioni nel formato da 50 ml (il più usato) che possono essere comodamente scaricati, ricordando che il Medico Veterinario può personalizzare la concentrazione o gli eccipienti a qualsiasi dosaggio e tipo, secondo le specifiche esigenze del paziente:
Per trovare e visualizzare quali Farmacie di Farmagalenica sono in grado di vendere prodotti derivati dalla canapa, consultare il motore di ricerca disponibile su www.cercagalenico.it (si aprirà una nuova pagina).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Estratto di cannabis Farmalabor 15% THC, olio galenico sembra essere il primo su Farmagalenica.
]]>L'articolo DHEA galenico in Italia: prescrizione e divieti sembra essere il primo su Farmagalenica.
]]>La risposta è che alcune Farmacie italiane aderenti a Farmagalenica sono in grado di preparare farmaci a base di DHEA: è un medicinale galenico che viene preparato dal Farmacista nel Laboratorio Galenico della Farmacia (v. fondo dell’articolo per la lista delle Farmacie), ma da Giugno 2021 sono state introdotti importantissimi divieti sul DHEA galenico.
Cos’è il DHEA
Il DHEA è un ormone steroideo anabolizzante utilizzato per diverse patologie:
- trattamento di patologie autoimmuni
- deficit di testosterone
- terapie ormonali anti invecchiamento
ma assolutamente controindicato in caso di neoplasie (cancro) essendo un ormone ad azione anabolizzante. Per una esaustiva trattazione degli effetti collaterali del DHEA invitiamo a leggere questo articolo.
In questo articolo potete invece approfondire l’aspetto chimico farmaceutico del DHEA galenico o non galenico.
Normativa e divieti sul DHEA capsule o uso sistemico
Prima del 17 Giugno 2021, il DHEA galenico era prescrivibile in qualsiasi modo e forma.
Con DM 1 Giugno 2021 è stata vietata la prescrizione di DHEA galenico ad uso sistemico. Resta possibile SOLO la prescrizione topica.
Firmato: il Ministero della salute
Tutte le preparazioni di DHEA galenico datate e spedite fino al 16 Giugno 2021 sono legittime.
A partire dal 17 Giugno 2021, non è possibile per il Farmacista prescrivere nuove ricette di DHEA o allestire vecchie ricette di DHEA galenico.
Con la pubblicazione in Gazzetta Ufficiale del 17 Giugno 2021 (link) del DM 1 GIUGNO 2021 “Divieto di preparazione di medicinali galenici contenenti le sostanze classificate steroidi anabolizzanti androgeni“, con entrata in vigore il giorno stesso, sono state vietate tutte le preparazioni sistemiche di DHEA galenico.
In particolare, l’art. 1 stabilisce che
1. È fatto divieto ai medici di prescrivere ed ai farmacisti di eseguire preparazioni galeniche contenenti le sostanze classificate steroidi anabolizzanti androgeni nel decreto emanato dal Ministro della salute, d'intesa con il Ministro per lo sport, su proposta della Commissione per la vigilanza ed il controllo sul doping e per la tutela della salute nelle attività' sportive, ai sensi dell'art. 2 della legge 14 dicembre 2000, n. 376.
L’art. 2 del DM 1 GIUGNO 2021 stabilisce invece che
2. Sono escluse dall'ambito di applicazione del presente decreto le preparazioni galeniche contenenti testosterone o nandrolone, fermo restando che esse restino soggette alle condizioni e limitazioni per la prescrizione previste per le corrispondenti specialità medicinali, nonché le preparazioni galeniche a base dei medicinali di cui al comma 1 che per caratteristiche e formulazione siano destinate esclusivamente all'uso topico, escludendo a qualsiasi titolo la possibilità di un uso sistemico.
Si ponga l’attenzione sul fatto che si parla di “uso topico” e non di “uso esterno”.
Possibilità prescrittive del DHEA in Italia
Poiché in Italia non esistono medicinali industriali (c. d. “specialità”) a base di deidroepiandrosterone è assolutamente necessario ricorrere al lavoro del Farmacista Galenico per poter avere il medicinale. A scanso di equivoci chiariamo che le Farmacie preparano il farmaco utilizzando materie prime purissime, non derivati o integratori (es. estratto secco di dioscorea).
In alcuni casi, il Farmacista può utilizzare capsule “gastroresistenti” rispetto alle normali capsule, in modo da preservare il farmaco dall’acidità dello stomaco.
In base alla normativa in vigore precedentemente esposta, non è quindi possibile prescrivere e allestire preparazioni galeniche di
- DHEA capsule o compresse o altre forme orali
- DHEA gocce orali
- DHEA sciroppo
- DHEA iniettabile
- DHEA gel/crema transdermico (v. oltre)
È invece possibile prescrivere e allestire preparazioni galeniche di
- DHEA gel
- DHEA crema / unguento non transdermico
- DHEA supposte
- DHEA ovuli
Il medico potrà richiede gel o creme per uso topico a qualsiasi concentrazione desideri e qualsiasi quantità (es. 30ml, 50ml, 100ml, ecc..).
Nota: in fondo all’articolo è disponibile una pratica tabella riepilogativa su cosa è possibile o non è possibile prescrivere.
DHEA galenico transdermico. Se è topico, perché no?
Vero che un gel o crema transdermico è un uso topico e quindi sembrerebbe previsto dall’art. 2 del DM 1 Giugno 2021.
Ma è anche vero che un gel transdermico può essere realizzato per far arrivare il principio attivo al sangue = uso sistemico.
Se a prima vista potrebbe comunque sembrare un escamotage, in realtà l’art. 2 del DM 1 Giugno 2021 è molto chiaro nell’indicare che:
- “che per caratteristiche e formulazione siano destinate esclusivamente all’uso topico”
- “escludendo a qualsiasi titolo la possibilità di un uso sistemico”
Il combinato di queste 2 affermazioni non lascia dubbi: la prima deve relegare l’attività all’uso topico (cosa che il gel transdermico non fa), la seconda esclude categoricamente che si possa avere un minimo di effetto sistemico (cosa che con il gel PLO è non solo possibile, ma praticamente certa).
Dal punto di vista normativo, le preparazioni a base di DHEA (deidroepiandrosterone) sono classificate doping e sono soggette a una rigida normativa che impone alle Farmacie che preparano DHEA di indicare specifici avvisi su ogni etichetta del preparato e segnalare ogni anno al Ministero della Salute, i quantitativi di DHEA galenico deidroepiandrosterone.
Ulteriori informazioni sull’uso (e abuso) del DHEA possono essere trovate in questo esaustivo articolo.
Altre sostanze vietate per uso sistemico oltre al DHEA galenico
Ecco un elenco delle sostante classificate steroidi anabolizzanti androgeni S1 non più prescrivibili per uso sistemico ma solo topico:
- 19-norandrostenediolo (estr-4-ene-3,17-diolo)
- 19-norandrostenedione (estr-4-ene-3,17-dione)
- 1-androstenediolo (5alfa-androst-1-ene-3beta,17beta-diolo)
- 1-androstenedione (5alfa-androst-1-ene-3,17-dione)
- 1-androsterone (3alfa-idrossi-5alfa-androst-1-ene-17-one)
- 1-testosterone (17beta-idrossi-5alfa-androst-1-en-3-one)
- 4-androstenediolo (androst-4-ene-3beta,17beta-diolo)
- 4-idrossitestosterone (4,17beta-diidrossi-androst-4-en-3-one)
- 5-androstenedione (androst-5-ene-3,17-dione)
- 7alfa idrossi-DHEA
- 7beta idrossi-DHEA
- 7-keto-DHEA (v. dopo)
- Androstanolone (5α-diidrotestosterone, 17β-idrossi-5α-androstan-3-one)
- Androstenediolo (androst-5-ene-3beta,17beta-diolo)
- Androstenedione (androst-4-ene-3,17-dione)
- Bolasterone
- Boldenone
- Boldione (androsta-1,4-diene-3,17-dione)
- Calusterone
- Clenbuterolo
- Clostebol
- Danazolo ([1,2]ossazolo[4′,5′:2,3]pregna-4-en-20-in-17alfa-olo)
- Deidroclormetiltestosterone (4-cloro-17beta-idrossi-17alfa-metil-androsta-1,4-dien-3-one)
- Desossimetiltestosterone (17alfa-metil-5alfa-androst-2-en-17beta-olo; 17alfa-metil-5alfa-androst-3-en-17beta-olo)
- Drostanolone
- Epiandrosterone (3beta-idrossi-5alfa-androstan-17-one)
- Epi-diidrotestosterone (17beta-idrossi-5beta-androstan-3-one)
- Epitestosterone
- Etilestrenolo (19-norpregna-4-en-17alfa-olo)
- Fluossimesterone
- Formebolone
- Furazabolo (17alfa-metil[1,2,5]ossadiazolo[3′,4′:2,3]-5alfa-androstan-17beta-olo)
- Gestrinone
- Mestanolone
- Mesterolone
- Metandienone (17beta-idrossi-17alfa-metilandrosta-1,4-dien-3-one)
- Metandriolo
- Metasterone (17beta-idrossi-2alfa,17alfa-dimetil- 5alfa-androstan-3-one)
- Metenolone
- Metil-1-testosterone (17beta-idrossi-17alfa-metil- 5alfa-androst-1-en-3-one)
- Metildienolone (17beta-idrossi-17alfa-metilestra-4,9-dien-3-one)
- Metilnortestosterone (17beta-idrossi-17alfa-metilestr-4-en-3-one)
- Metiltestosterone
- Metribolone (metiltrienolone, 17beta-idrossi-17alfa-metilestra-4,9,11-trien-3-one)
- Mibolerone
- Norboletone
- Norclostebol
- Noretandrolone
- Ossabolone
- Ossandrolone
- Ossimesterone
- Ossimetolone
- Prasterone (deidroepiandrosterone, DHEA, 3beta-idrossi-androst-5-en-17-one)
- Prostanozolo (17beta-[(tetraidropiran-2-il)ossi]- 1’H-pirazolo[3,4:2,3]-5alfa-androstano)
- Quinbolone
- Stanozololo
- Stenbolone
- Tetraidrogestrinone (17-idrossi-18alfa-omo-19-nor-17alfa-pregna-4,9,11-trien-3-one)
- Trenbolone (17beta-idrossiestr-4,9,11-trien-3-one)
- Andarina (vedi “SARMS”)
- Enobosarm (ostarina, vedi “SARMS”)
- LGD-4033 (vedi “SARMs”)
- RAD140 (vedi “SARMs”)
- SARMs (Modulatori selettivi dei recettori degli androgeni)
- Tibolone
- Zeranolo
- Zilpaterolo

E per quanto riguarda il 7-keto-DHEA? È acquistabile in Italia?
Il 7-Ketodehydroepiandrosterone (comunemente noto come 7-keto-DHEA o 7-oxoprasterone) è un metabolita del DHEA che come viene venduto come integratore alimentare in America, ma NON in Europa.
Di fatto, anche alla luce del DM 1 GIUGNO 2021 il 7-keto-DHEA NON è allestibile come galenico magistrale o altro. E quindi, non è legalmente acquistabile in Farmacia.
Acquistare DHEA legalmente. Si può?
Diciamo che se andate su siti online quali Amazon e cercate “DHEA” troverete integratori (non registrati in Italia) vendibili legalmente in quanto classificati, a quei dosaggi, appunto come integratori alimentari.
Come è possibile ciò? La spiegazione più rapida (non unica) è che il Ministero della Salute ha bloccato in Italia un’intera categoria di molecole, anche molto diverse tra loro, che però in tanti altri paesi del mondo sono venduti come farmaco con ricetta (come era per il DHEA galenico) o anche senza ricetta medica, generando paradossi.
Qualcuno farà ricorso?
Qualcuno ha fatto ricorso sul DHEA capsule vietato in Italia
Giunge notizia che nel mese di Ottobre è stato presentato un ricorso al TAR contro questo decreto, da parte di un Medico e di un farmacista.
In caso di aggiornamenti, il sito sarà prontamente aggiornato.
Tabella riepilogativa
A questo punto, una tabella riepilogativa può sicuramente far capire meglio cosa può essere ancora legalmente prescrivibile dal Medico e preparabile dal Farmacista Galenista:
| USO SISTEMICO | USO TOPICO | ALTRI USI (es. vaginale, rettale, nasale) | |
| DHEA | NON AMMESSO | AMMESSO | AMMESSO |
| Testosterone | AMMESSO | AMMESSO | AMMESSO |
| Nandrolone | AMMESSO | AMMESSO | AMMESSO |
| Tutti gli altri anabolizzanti | NON AMMESSO | AMMESSO | NON AMMESSO |
Legislazione per la vendita di DHEA galenico in Farmacia
Per poter essere preparato in Farmacia, il DHEA galenico topico richiede ricetta medica non ripetibile, valida per 30 giorni escluso quello di emissione, solitamente per una sola preparazione.
Tale ricetta viene trattenuta dal Farmacista ed è necessario presentarne una nuova per ogni preparazione. Essendo un farmaco realizzato estemporaneamente per ogni singola richiesta, il DHEA può essere preparato in qualsiasi quantità e qualsiasi dosaggio a seconda della necessità.
Per cercare e visualizzare quali Farmacie di Farmagalenica sono dotate di laboratorio galenico per preparare DHEA galenico, consultare il motore di ricerca disponibile su www.cercagalenico.it (si aprirà una nuova pagina).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo DHEA galenico in Italia: prescrizione e divieti sembra essere il primo su Farmagalenica.
]]>