L'articolo Estratti di cannabis TILRAY: arrivano in Italia sembra essere il primo su Farmagalenica.
]]>Prima sono arrivate le infiorescenze grezze, poi gli oli galenici (fatti dal Farmacista), poi il primo estratto industriale Farmalabor 15% THC (articolo dedicato); ora è la volta di TILRAY che importa e rende disponibile in Italia 3 nuovi estratti industriali di cannabis tramite l’azienda Fl-Group, unico rivenditore autorizzato per l’Italia (alla data dell’ultimo aggiornamento dell’articolo).
Quando si parla di estratto di cannabis si intende genericamente il c. d. olio di cannabis.
Quali sono questi estratti? Che caratteristiche hanno? Usi? Quali pro e quali contro? Costo? Che ricetta serve? Dove? Come? Quando?
C’è tutto nell’articolo che state per leggere 
Estratto di cannabis TILRAY
Sono estratti in MCT a diverse concentrazioni di THC e CBD. Eccole di seguito, con all’inizio il “nome in codice” che per praticità e facilità di comprensione verrà adottato nel corso dell’articolo:
- T25 = estratto al 2,5% THC e < 1% CBD
- T10C10 = estratto al 1% THC e 1% CBD
- T5C20 = estratto al 0,5% THC e 2% CBD
Sono venduti in singoli flaconi da 25 ml di liquido e la disponibilità è
- da Maggio 2023 per il T25
- da Giugno in avanti per gli altri.
Nell’articolo che segue, quindi, ci si riferirà ai 3 estratti con le sigle di T25, T10C10 e T5C20.
“T” sta per THC. “C” sta per CBD. Il numero (es. “25”) NON sta per la % di THC o CBD, ma la concentrazione mg/ml di THC o CBD.
Importantissimo da capire
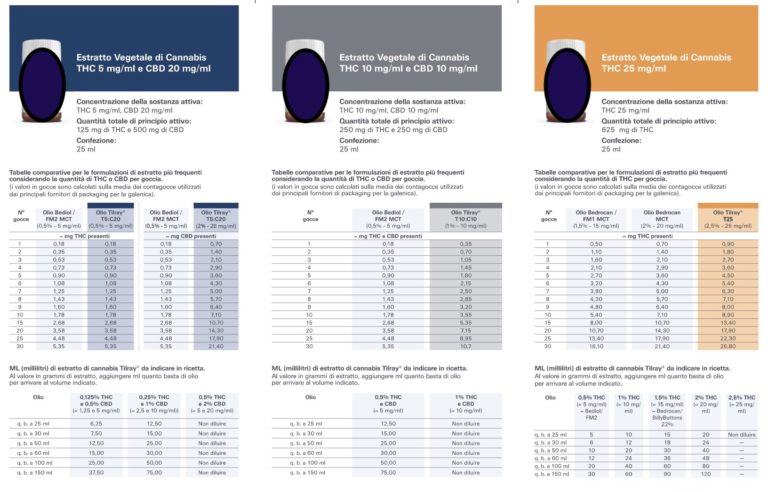
Poiché le percentuali possono creare confusione sul reale contenuto di THC e CBD, ecco una tabella riepilogativa con le concentrazioni espresse chiaramente, raffrontando mg/ml e %:
| Estratto TILRAY | Concentrazione % | Concentrazione mg/ml |
| T25 | 2,5% THC e < 1% CBD | 25 mg/ml THC |
| T10C10 | 1% THC e 1% CBD | 10 mg/ml THC e 10 mg/ml CBD |
| T5C20 | 0,5% THC e 2% CBD | 5 mg/ml THC e 20 mg/ml CBD |
Spesso si tende a confrontare una percentuale nel fiore di cannabis (es. fiore di Bedrocan 22%) con un estratto di cannabis (es. estratto di cannabis Tilray 2,5%) pensando che sia corretto. NON è così!
Matematica docet
Gli estratti di cannabis Tilray sono classificati come materia prima per preparare farmaci galenici a base di cannabis medica, ma per le loro concentrazioni di THC e CBD possono anche essere forniti anche puri, senza diluizione.
La preparazione del farmaco galenico avviene diluendo l’estratto in opportuni eccipienti quali:
- tensioattivi
- olio vegetale (MCT principalmente, olio extravergine di oliva, olio di oliva, eccetera)
Ora, sappiate che ogni infiorescenza di cannabis medica di una determinata azienda farmaceutica è unica, in quanto derivata da una genetica proprietaria dell’azienda (es. Bedrocan BV, Aurora, Canopy, ecc…) che la produce/coltiva.
Ogni olio di cannabis è quindi diverso se preparato con infiorescenze di cannabis diverse.
Per quanto riguarda la composizione dell’estratto di cannabis TILRAY in terpeni e altri cannabinoidi (es. THCA, CBG, CBN, ecc…) queste sono le informazioni disponibili da certificato di analisi:
- CBD: [varia da estratto a estratto]
- CBN: < 2,5%
- THCA: not declared
Come per tutti gli estratti industriali, le specifiche (e i relativi contenuti in cannabinoidi, acido o neutri) di questi estratti TILRAY sono conformi alla monografia tedesca Cannabis Extractum.
Appena disponibile, verrà pubblicata un’analisi HPLC degli estratti con maggiori informazioni sui terpeni contenuti.
Sativa o Indica?
Gli estratto di cannabis TILRAY possono essere sia SATIVA che INDICA, dipende dal prodotto:
–
Leggere la sezione tecnica più avanti per maggiori informazioni.
Questi estratti sono stati autorizzati dal Ministero della Salute italiano, come si può leggere in questo comunicato.
Gli estratto di cannabis TILRAY NON sono “isolati”, ossia non sono un liquido contenente solamente THC e/o CBD, ma contengono anche altri cannabinoidi e sostanze della cannabis
È comunque una materia prima “raffinata”, trattata per standardizzare il contenuto
Gli estratti di THC e CBD Tilray, come detto, possono essere usati puri o diluiti per ottenere oli di cannabis analoghi all’olio di Bedrocan o Billy Buttons oppure al Bediol o FM2 (aggiungendo CBD cristalli alla soluzione) anche se in questo ultimo caso avrebbe senso utilizzare un estratto TILRAY come il T10C10 che ha una concentrazione doppia rispetto a (es.) l’olio di Bediol.
ATTENZIONE: “analoghi” significa solo che avranno la stesso identica quantità di THC e/o CBD, ma che avranno diversa composizione in terpeni, cannabinoidi secondari, eccetera.
Questi estratto di cannabis TILRAY NON sono ottenuto da Bedrocan o Billy Buttons o Pedanios, ma da altre infiorescenze di proprietà di Tilray. Come già detto, è un analogo, non identico.
Dettagli sulle Concentrazioni degli estratti di cannabis TILRAY
In particolare, se parliamo di concentrazione del THC all’interno dell’olio finale (quello che il paziente acquisterà e assumerà) occorre precisare una cosa importantissima:
- gli oli di cannabis con THC realizzati nelle Farmacie Galeniche negli ultimi 9 anni in Italia, hanno in media una concentrazione che varia dallo 0,5% p/v (cioè 5 mg/ml) ad un massimo di circa 1,8% p/v (cioè 18 mg/ml)
- ottenere concentrazioni di THC maggiori al 2,0% con varietà come il Bedrocan o Pedanios è in teoria possibile (es. metodica Ternelli/Pellati), ma inutile: l’olio ottenuto sarebbe poco dosabile, alto rischio di effetti collaterali, difficoltà a costruire tolleranza.
- allo stesso modo, un olio di cannabis con concentrazioni > 2% THC ottenuto dall’estratto di cannabis TILRAY T25 non ha molto senso, pertanto è l’unico che è bene diluire, ma il Medico può comunque ritenere di prescrivere l’estratto T25 non diluito.
Quali differenze come concentrazione e composizione dall’olio di Bedrocan o Billy Buttons rispetto all’ estratto di cannabis TILRAY?
Per rendere il concetto più chiaro, sono disponibili le seguenti tabelle comparative:
Consigli pratici per il Farmacista per la preparazione dell’olio di cannabis dall’estratto di cannabis TILRAY
Nota: paragrafo un po’ tecnico, per Farmacisti e Medici. Se non vi interessa passate pure al successivo. Ma è interessante, sappiatelo 
Prima di tutto, la regola madre da cui tutto dipende: essendo una soluzione oleosa, la densità degli estratti di cannabis TILRAY non è 1 (circa 0.963, ma varia da lotto a lotto) perciò 1 g di estratto di cannabis TILRAY NON è la stessa cosa di 1 ml di estratto di cannabis TILRAY.
Essendo la concentrazione espressa in % p/v (w/v), andranno caricati in MILLILITRI sul Registro di Entrata e Uscita degli Stupefacenti della Farmacia.
Per ordinarli all’azienda Fl-Group, il Buono Acquisto andrà compilato indicando:
- o il numero di flaconi da 25 ml (più pratico, esempio “Estratto di cannabis 2.5% THC 25ml – di tali 1“)
- o gli ml totali da richiedere. Ovviamente devono essere multipli di 25 (esempio, “Estratto di cannabis 2.5% THC – di tali 250 ml”)
Prescrizioni, diluizioni e millilitri
A seconda dell’estratto TILRAY che serve, serve una ricetta diversa a seconda che:
- venga prescritto puro: tipicamente il T10C10 e il T5C20
- venga prescritto diluito: tipicamente il T25
Per facilitare le operazioni di confronto e diluizione, Fl-Group mette a disposizione questo documento PDF per facilitare le operazioni.
Disclaimer: è responsabilità del Farmacista assicurarsi che i calcoli stechiometrici, nonché i valori del certificato di analisi siano corretti per assicurarsi del contenuto finale di THC nell’olio. Farmagalenica SRL esclude ogni responsabilità per errori o imprecisioni dovessero derivare dall’uso della presente tabella.
Di seguito, invece, un esempio della scheda tecnica dei 3 estratti:


Diluizioni: come ottenere olio di cannabis partendo dall’estratto T25 TILRAY
Spiegato e capito che se in teoria tutti gli estratti di cannabis TILRAY possono essere diluiti, quello che ha più senso è il T25 (25 mg/ml THC): ecco alcune indicazioni su come operare correttamente.
Fondamentale: oltre a miscelare, prestare molta attenzione a verificare la completa dissoluzione dell’estratto nell’eccipiente. Se ciò non avvenisse completamente, si avrebbe un estratto a concentrazione non uniforme, con potenziali problemi per il paziente.
Quello che va fatto è:
- PESARE con bilancia i MILLILITRI di estratto
- portare a VOLUME mediante siringa, cilindro graduato, pallone o matraccio (ASSOLUTAMENTE NO direttamente nel contenitore finale) con l’eccipiente finale
- miscelare con agitatore elettromagnetico o a pale (comunque meccanico)
- travasare nel contenitore finale
Calcolatore diluizioni per estratto TILRAY T25
Oltre alla tabella sopra riportata, si fornisce questo calcolatore online per permettere un rapido calcolo della quantità in millilitri di estratto T25 necessario (da pesare o indicare in ricetta) rispetto al volume finale desiderato di olio.
Il calcolatore delle dosi personalizzate è fornito ad uso dimostrativo; si esclude ogni responsabilità per eventuali errori in quanto la responsabilità del calcolo è sempre del Farmacista / Medico.
Eccipienti da usare
L’estratto di cannabis Tilray è realizzato in MCT (Medium Chain Trigliceridis, olio di cocco raffinato), ossia l’estratto è diluito in una massa costituita da una materia prima GMP a base di MCT.
È quindi consigliato utilizzare lo stesso solvente per diluire l’estratto e realizzare l’olio di cannabis.
Nulla vieta al Medico o al Farmacista di prescrive o usare un olio diverso (es. oliva, mais, ecc…) sempre di grado farmaceutico.
Confezionamento
Come per l’olio di cannabis ottenuto da infiorescenze, è necessario utilizzare un flacone contagocce, solitamente un flacone in vetro ambrato di classe III con tappo child-proof (a prova di bambino) cui può essere aggiunto un riduttore e siringa graduata per la somministrazione.
Conservazione
Gli estratti di cannabis TILRAY così come l’olio di cannabis realizzato con essi vanno conservati, in base a quanto raccomandato dal produttore, a temperatura ambiente a < 25°C.
Scadenza
La shelf life degli estratti di cannabis TILRAY puro (quindi la materia prima da lavorare) ha un scadenza di circa 6 mesi. ATTENZIONE PERO’: l’olio di cannabis realizzato con essi se conservato in frigorifero può avere una scadenza massima di 2 mesi, ma ancora non sono disponibili studi sulla stabilità definitiva. È ipotizzabile un periodo di qualche mese a temperatura ambiente.

Vantaggi e svantaggi
Ci sono diverse peculiarità nell’uso di un estratto di cannabis industriale come quello TILRAY: come tutte le cose alcune sono positive, altre negative. E ci sono pure considerazioni neutre.
Vediamole velocemente, ma nello specifico.
Vantaggio: disponibilità di olio con THC in carenza di infiorescenze
Innegabilmente in questo periodo di carenza di cannabis infiorescenze anche per preparare olio di cannabis terapeutico in Farmacia o cartine da decotto o vaporizzare, avere a disposizione una alternativa permette di sopperire alla carenza.
Vale la pena sottolineare, però, come in Italia ci sia una “cultura” dell’olio di cannabis galenico, ossia una abitudine del Medico, del paziente, del Farmacista e anche di norme Regionali, in cui quello che viene trattato e richiesto è l’olio di infiorescenze fatto in Farmacia dal Farmacista.
Vantaggio: semplicità di preparazione e meno tempo
Realizzare un olio di cannabis da infiorescenze nel Laboratorio Galenico della Farmacia richiedere da 1 a 2 giorni a seconda della metodica da utilizzare; in questo caso si tratta di miscelare “semplicemente” (virgolette perché di semplice non c’è mai nulla nella attività di un Farmacista Galenista, i problemi sono sempre dietro l’angolo) l’estratto con gli eccipienti quando addirittura semplicemente di ripartire direttamente il volume finale richiesto dal Medico in ricetta nel nuovo contenitore ed etichettarlo.
Il Farmacista, nel dispensare l’estratto di cannabis TILRAY puro non può MAI fornirlo nel contenitore originale, ma deve travasarlo in apposito flacone e rietichettarlo in base alle NBP.
Come da indicazioni riportate sulla confezione
Ripetendolo ancora, è fondamentale che il Farmacista Galenista si assicuri che la massa dell’ estratto di cannabis TILRAY sia perfettamente disciolta negli eccipienti, evitando la formazione di “sacche” di olio più concentrate e altre meno concentrate.
Vantaggio: standardizzazione = niente analisi HPLC
Gli estratto di cannabis TILRAY sono già titolati, ossia è noto cosa contiene ogni ml di estratto:
- T25 = estratto a 25 mg/ml THC e < 1 mg/ml CBD
- T10C10 = estratto al 10 mg/ml THC e 10 mg/ml CBD
- T5C20 = estratto al 5 mg/ml THC e 20 mg/ml CBD
Per questo con pochi calcoli stechiometrici il Farmacista è in grado di indicare la concentrazione finale di THC contenuta in
- 1 ml finale di olio di cannabis
- 1 goccia di olio di cannabis
Esempio tecnico: sapendo che in 1 ml sono presenti 25mg di THC come da certificato di analisi, avendo messo 20 ml di estratto e portato a volume di 50 ml con olio di MCT, significa che in 1 ml finale di olio di cannabis saranno presenti 10 mg di THC. Inoltre, sapendo che 1 ml di olio sono circa 28 gocce, significa che ogni goccia conterrà circa 0,9 mg di THC.
Vantaggio: maggiore reperibilità per il paziente
È innegabile che un prodotto come gli estratti di cannabis Tilray che non richiede la lavorazione galenica “tipica” degli estratti galenici realizzati in Farmacia, possa permettere anche a qualche farmacia in più di disporre del medicinale e fornirlo al paziente che può quindi reperirlo più facilmente.
Dall’altra parte è anche giusto considerare che non si tratta di un prodotto industriale finito, che comunque va manipolato in un laboratorio galenico, richiede registrazioni, va gestito come scadenze e residui (“incorretta tenuta del registro”, ehm…) e questo terrà comunque “lontane” diverse farmacie.
Vantaggio: costo finale minore al paziente per oli analoghi a basso THC
In base alla Tariffa Nazionale dei Medicinali, il Farmacista non può decidere in autonomia il costo di un farmaco galenico, ma attenersi ad essa per calcolare il prezzo finale.
Per quanto riguarda i costi degli estratti di cannabis Tilray è riportato di seguito il costo proposto dal rivenditore alla Farmacia, indipendentemente dalla concentrazione di THC e CBD:
- € 70-80 + IVA 22% a flacone (MOQ = 2 flaconi)
Poichè in base alla Tariffa Nazionale dei Medicinali il Farmacista ha un ricarico dello 0% (sì, avete letto bene, zero) sulle materie prime, ossia che deve vendere la materia prima a prezzo di costo, deriva che meno spende il Farmacista, meno spende il paziente.
La stessa preparazione fatta con lo stesso estratto di Cannabis TILRAY da farmacie diverse, può avere costi diversi a seconda di “quanto bene” ha acquistato il Farmacista.
Nella tabella seguente sono elencati alcuni esempi di prezzi (a parità di THC e quantitativo finale) calcolati in base alla Tariffa Nazionale dei Medicinali per far capire le differenze di prezzo tra il prezzo al paziente di un estratto realizzato farmacia da infiorescenze e un olio realizzato diluendo l’estratto di cannabis TILRAY:
Costi al paziente per “alto THC” – flacone da 50ml
| CONCENTRAZIONE FINALE DI THC | VOLUME | THC TOTALE NEL FLACONE | Prezzo finale al paziente (IVA 10% inclusa) | Costo €/mg THC | |
| Bedrocan Olio 5g (Metodica Romano & Hazekamp) [OBSOLETA E SCONSIGLIATA] | 5 mg/ml THC | 50 ml | 250 mg | CIRCA 95€ | 0,38€ |
| Bedrocan Olio 5g (Metodica Ternelli / Calvi) | 15 mg/ml THC | 50 ml | 750 mg | CIRCA 119€ | 0,158€ |
| Olio di cannabis da T25 diluito TILRAY analogo Bedrocan (30 ml di estratto necessari) [70€/fl] | 15 mg/ml THC | 50 ml | 750 mg | CIRCA 130€ | 0,176€ |
| Olio di cannabis T25 puro TILRAY [70€/fl] | 25 mg/ml THC | 50 ml | 1250 mg | CIRCA 192€ | 0,073€ |
Costi al paziente per “alto THC” – flacone da 25ml
| CONCENTRAZIONE FINALE DI THC | VOLUME | THC TOTALE NEL FLACONE | Prezzo finale al paziente (IVA 10% inclusa) | Costo €/mg THC | |
| Bedrocan Olio 5g (Metodica Romano & Hazekamp) [OBSOLETA E SCONSIGLIATA] | 5 mg/ml THC | 25 ml | 125 mg | CIRCA 80€ | 0,640€ |
| Bedrocan Olio 5g (Metodica Ternelli / Calvi) | 15 mg/ml THC | 25 ml | 375 mg | CIRCA 85€ | 0,227€ |
| Olio di cannabis da T25 diluito TILRAY analogo Bedrocan (15 ml di estratto necessari) [70€/fl] | 15 mg/ml THC | 25 ml | 375 mg | CIRCA 85€ | 0,227€ |
| Olio di cannabis T25 puro TILRAY [70€/fl] | 25 mg/ml THC | 25 ml | 625 mg | CIRCA 115€ | 0,184€ |
Costi al paziente per “THC:CBD bilanciato” – flacone da 50 ml
| CONCENTRAZIONE FINALE DI THC/CBD | VOLUME | THC/CBD TOTALE NEL FLACONE | Prezzo finale al paziente (IVA 10% inclusa) | Costo €/mg THC-CBD | |
| Bediol/FM2 Olio 5g (Metodica Romano & Hazekamp) [OBSOLETA E SCONSIGLIATA] | 3 mg/ml THC&CBD | 50 ml | 150 mg | CIRCA 95€ | 0,633€ |
| Bediol/FM2 Olio 5g (Metodica Ternelli / Calvi) | 5 mg/ml THC&CBD | 50 ml | 250 mg | CIRCA 119€ | 0,476€ |
| Olio di cannabis da T10C10 diluito TILRAY analogo Bediol/FM2 (25 ml di estratto necessari) [70€/fl] | 5 mg/ml THC&CBD | 50 ml | 250 mg | CIRCA 125€ | 0,50€ |
| Olio di cannabis T10C10 puro TILRAY [70€/fl] | 10 mg/ml THC&CBD | 50 ml | 500 mg | CIRCA 192€ | 0,384€ |
Costi al paziente per “THC:CBD bilanciato” – flacone da 25 ml
| CONCENTRAZIONE FINALE DI THC/CBD | VOLUME | THC/CBD TOTALE NEL FLACONE | Prezzo finale al paziente (IVA 10% inclusa) | Costo €/mg THC-CBD | |
| Bediol/FM2 Olio 5g (Metodica Romano & Hazekamp) [OBSOLETA E SCONSIGLIATA] | 3 mg/ml THC&CBD | 25 ml | 75 mg | CIRCA 80€ | 1,067€ |
| Bediol/FM2 Olio 5g (Metodica Ternelli / Calvi) | 5 mg/ml THC&CBD | 25 ml | 125 mg | CIRCA 85€ | 0,680€ |
| Olio di cannabis da T10C10 diluito TILRAY analogo Bediol/FM2 (12,5 ml di estratto necessari) [70€/fl] | 5 mg/ml THC&CBD | 25 ml | 125 mg | CIRCA 83€ | 0,664€ |
| Olio di cannabis T10C10 puro TILRAY [70€/fl] | 10 mg/ml THC&CBD | 25 ml | 250 mg | CIRCA 115€ | 0,460€ |

Svantaggio: costo assoluto maggiore al paziente
Ribadendo ancora che il prezzo di un olio di cannabis è deciso in base alla Tariffa Nazionale dei Medicinali e che il Farmacista non può decidere in autonomia il costo di un farmaco galenico, un possibile svantaggio (apparente?) è il costo assoluto finale che il paziente deve sostenere per acquistare alcuni tipi di oli di cannabis Tilray.
Per “assoluto” si intende l’esborso monetario che il paziente deve sostenere per poter acquistare il farmaco galenico.
Riprendendo le tabelle precedentemente proposte, si ponga attenzione alla colonna del “Prezzo finale al paziente (IVA 10% inclusa)“: ci saranno casi in cui il paziente non considererà dimensione del flacone, rapporto €/mg di THC o CBD, ma guarderà solo l’importo che spende in virtù (es.):
- di una disponibilità economica
- che essendo la prima volta, vorrà solo provare il farmaco senza rischiare di aver sprecato l’importo se poi il farmaco non può essere utilizzato
D’altra parte, se il paziente sa per certo che userà tutto il flacone, in alcuni casi (quando l’estratto di cannabis TILRAY non è diluito) avrà un risparmio rispetto ad altre preparazioni.
Svantaggio: meno Galenica per il Farmacista
Può sembrare strano, ma l’uso di estratti industriali (già pronti) se apparentemente semplifica la vita al Farmacista Galenista, dall’altro riduce il suo lavoro ad un semplice riconfezionamento o semplice diluizione con altro olio.
Intendiamoci, niente di sbagliato o deprecabile. Ma forse la personalizzazione di ogni singolo preparato da infiorescenze per ogni singolo paziente è qualcosa di auspicabile per il futuro; se sarà anche grazie alla Galenica, lo vedremo nei decenni a venire.
Svantaggio: non rimborsato da tutto il SSN o SSR
Pur parlando sempre di cannabis, questo estratto rappresenta una novità in termini assoluti, quindi a differenza degli estratti di cannabis preparati in farmacia (già rimborsati), in questo caso l’olio di cannabis ottenuto da questo estratto di cannabis TILRAY non è ad oggi mutuabile in diverse Regioni: ogni singola Regione dovrà emettere un nuovo atto normativo per riconoscerne la mutuabilità (gratuità).
Ad oggi, per quanto dato di sapere, le Regioni in cui gli estratti Tilray sono rimborsabili (mutuabili) sono:
- Emilia Romagna
Le domande a cui rispondere sono, specie dopo aver visto l’iter di altri estratti industriali:
- le Regioni faranno queste delibere?
- QUANDO lo faranno?
Rilordate che i tempi tecnici sono sempre mesi che diventano anni in alcuni casi.
Svantaggio: niente THCA. E i terpeni?
Non risulta essere presente se non in tracce il THCA (THC acido), il precursore del THC. Diversi studi presenti su Pubmed (ad esempio qui e qui) hanno evidenziato come anche il THCA possieda attività terapeutiche e svolga dunque una azione importante.
Nell’estratto risultano tracce di THCA, mentre negli estratti realizzati in farmacia da infiorescenze esso è presente in concentrazioni variabili a seconda del metodo, ma comunque a dosi importanti.
Potrà capitare quindi che una preparazione di cannabis con solo THC abbia un effetto diverso da una con THC e THCA.
Per i terpeni, si attendono analisi o documentazione da parte del produttore.
Considerazione: unica fonte di THC
La cannabis non è THC. Il THC non è cannabis.
Immaginando un futuro in cui gli estratti saranno solo come questo (cioè non più preparati in Farmacia partendo dalle infiorescenze), di fatto vorrebbe dire addio alla personalizzazione della varietà di cannabis da utilizzare: se serve un olio con THC (o CBD) questo è, prendere o lasciare.
Questo potrebbe cambiare se in futuro ci fossero più estratti, di più varietà. Ma non abbiamo la sfera di cristallo..
Domande frequenti (FAQ) sull’olio di cannabis estratto di cannabis TILRAY
Sono almeno i seguenti:
– pesata
– misurazione volumetrica
– miscelazione
– dissoluzione
In alcune circostanze (es. aggiunto di altri attivi) può essere applicato anche:
– riscaldamento
– sonicazione
– raffreddamento
– ecc…
per un totale minimo di 4 operazioni tecnologiche a preparazione.
DIFFIDATE da chi sostiene ve ne siano meno.
Certamente, il Medico può indicare l’aggiunta di cristalli di CBD nell’olio per ottenere qualsiasi rapporto di THC e CBD desiderato, esattamente come già avveniva con gli estratti realizzati in Farmacia partendo da infiorescenze.
Ad esempio, è possibile miscelare l’estratto di THC e aggiungere CBD per ottenere un olio di cannabis analogo al Bediol o FM2.
Poiché tutte le registrazioni a livello ministeriale e del fornitore sono in MILLILITRI, va registrato in MILLILITRI. Anche perché scaricare “flaconi mezzi” diventa alquanto difficile se un medico prescrive 30 ml o 60 ml.
La tariffazione segue miscele di oli (punto 3).
NO soluzioni.
NO estratti e tinture.
Normativa per la vendita e acquisto degli estratti di cannabis TILRAY
L’olio di cannabis può essere prescritto sia per uso umano che per uso veterinario.
Uso umano
Trattandosi di una preparazione galenica, per l’acquisto dell’estratto di cannabis TILRAY alla concentrazione desiderata, serve una ricetta non ripetibile valida 30 giorni escluso quello di emissione, per una sola preparazione (si tratta di un farmaco galenico stupefacente e psicotropo).
Tutte le prescrizioni di olio di cannabis da estratto di cannabis TILRAY sono SEMPRE OFF-LABEL
Legge 94/98 art. 5
Tale ricetta può essere redatta da qualsiasi medico e sempre in OFF LABEL (come per le ricette di infiorescenze di cannabis) secondo l’art. 5 della Legge 94/98 (“Di Bella”) e deve prevedere almeno:
- data di redazione
- timbro (o intestazione) del Medico
- firma del Medico
- codice numerico o alfanumerico + motivazione della prescrizione
- quantità di estratto di cannabis TILRAY in millilitri
- (non necessario se estratto non va diluito) quantità e qualità di eccipienti (es. MCT o olio di oliva)
- (non obbligatoria ma consigliata) posologia
Per semplificarne la comprensione, si rendono disponibili a scopo didattico i seguenti esempi facsimile uso umano in PDF con diverse concentrazioni nel formato da 50 ml (il più usato) che possono essere scaricati, ricordando che il Medico può personalizzare la concentrazione o gli eccipienti a qualsiasi dosaggio e tipo, secondo le specifiche esigenze del paziente:
Uso veterinario dell’ estratto di cannabis TILRAY
Trattandosi di una preparazione galenica, per l’acquisto degli estratti di cannabis TILRAY alla concentrazione desiderata, serve una ricetta veterinaria non ripetibile valida 30 giorni escluso quello di emissione, per una sola preparazione. Essendo un farmaco galenico stupefacente e psicotropo va prescritto con ricetta REV.
Tale ricetta può essere redatta da qualsiasi medico veterinario in base al quanto disposto dall’art. 84 del Dlgs 193/2006 e solo per PET o nDPA (animali da compagnia quali cani e gatti, detti anche non destinati alla produzione di alimenti); la ricetta veterinaria elettronica dovrà riportare:
- data di redazione
- timbro (o intestazione) del Medico Veterinario
- firma del Medico Veterinario
- nome, cognome e indirizzo del proprietario dell’animale
- quantità di estratto di cannabis TILRAY THC in millilitri
- (non necessario se estratto non va diluito) quantità e qualità di eccipienti (es. MCT o olio di oliva)
- posologia (obbligatoria)
Per semplificarne la comprensione, si rendono disponibili a scopo didattico i seguenti esempi facsimile uso veterinario in PDF con diverse concentrazioni nel formato da 50 ml (il più usato) che possono essere comodamente scaricati, ricordando che il Medico Veterinario può personalizzare la concentrazione o gli eccipienti a qualsiasi dosaggio e tipo, secondo le specifiche esigenze del paziente:
Per trovare e visualizzare quali Farmacie di Farmagalenica sono in grado di vendere prodotti derivati dalla canapa, consultare il motore di ricerca disponibile su www.cercagalenico.it (si aprirà una nuova pagina).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Estratti di cannabis TILRAY: arrivano in Italia sembra essere il primo su Farmagalenica.
]]>L'articolo Importazione cannabis medica, bando italiano e farmacie sembra essere il primo su Farmagalenica.
]]>In Italia, la cannabis medica terapeutica arriva in 3 modi:
- produzione cannabis in Italia tramite lo Stabilimento Chimico Farmaceutico Militare di Firenze
- importazione cannabis medica dall’Olanda
- importazione cannabis medica tramite bando italiano (solitamente dal Canada o Danimarca)
In questo articolo si parlerà del bando italiano per l’importazione di cannabis Medica, di come funziona, perché è stato necessario, quali e quanti bandi ci sono stati in Italia, le società vincitrici dei bandi passati, eccetera…
Perché si è fatto un bando italiano per l’ importazione cannabis medica?
La ragione è una e una sola: per la carenza di cannabis medica in Italia, ovvero l’insufficiente disponibilità di cannabis medica per i pazienti italiani che ne fanno richiesta.
L’argomento è talmente vasto che ha un suo dettagliatissimo articolo dedicato. La lettura, anche parziale, è consigliata prima di procedere con il presente articolo.
Quanti bandi per l’ importazione di cannabis medica ci sono stati finora in Italia?
Ad oggi 3 e mezzo, anche se dovremmo dire 4:
- nel 2018, bando di importazione per 100 Kg/anno per 1 anno, vinto da Aurora
- nel 2019, bando di importazione per 200 Kg/anno per 2 anni, vinto da Aurora
- nel 2021, assegnazione diretta di 110 Kg, vinto da Little Green Pharma
- l’ultimo nel 2022, bando di importazione per 630 Kg/ anno per 1 anno, in corso
Verranno descritti anno per anno, volendo potete scorrere passando direttamente a quello che vi interessa.
Bando del 2018 per l’ importazione cannabis medica [informazioni storiche, non aggiornate ad oggi]
Il bando, lo ricordiamo, nacque per far fronte alla carenza di cannabis iniziata a Giugno 2017 nel nostro Paese (i dettagli qui).
Il bando si aprì nel Novembre 2017, si concluse nel Gennaio 2019 e a Marzo 2019 arrivarono i primi grammi alle Farmacie di cannabis Canadese
Le ditte partecipanti furono 2:
Dal Febbraio 2018, i Farmacisti Galenisti Italiani di Farmagalenica ebbero a disposizione ulteriore cannabis medica da utilizzare per le preparazioni galeniche: la cannabis Pedanios (marchio Aurora) o Spektrum potrebbe infatti arrivare in Italia se una delle due società riuscirà a vincere il bando (anche se ad oggi non sono ancora state aperte le buste) per l’importazione di 100 Kg nel corso del 2018, che si andranno a sommare ai 250 Kg di importazione dalla Bedrocan BV (Olandese).
Chi vinse il bando per importazione cannabis medica nel 2018?
Siamo lieti di pubblicare in esclusiva, la prima intervista ad Aurora/Pedanios (vincitrice del bando), in fondo a questo articolo.
Dal comunicato stampa del Ministero della Difesa (v. sotto), si evince che la cannabis Pedanios Aurora è l’unica rimasta delle 2 Società presentatesi. Una è stata esclusa, rimane solo Pedanios. Va da se…Update fine Dicembre 2017: contro quanto riportato nel verbale, Spektrum (l’altra ditta del bando) è stata riammessa. Le buste NON sono ancora state aperte (dovevano esserlo il 22 Dicembre), ma lo saranno dopo le festività. Update inizio Gennaio 2018: l’apertura delle buste era prevista per il 10 Gennaio, ma per la valutazione dei ricorsi si slitterà ancora. I tempi si allungano ancora…
Update metà Gennaio 2018: Aurora Pedanios ha vinto tutte e 3 le varietà previste nel bando (leggi comunicato stampa ufficiale).
Pedanios Aurora ha vinto tutti e 3 i lotti previsti dal bando (qui il comunicato stampa ufficiale del Ministero della Difesa) e le varietà aggiudicate sono le seguenti:
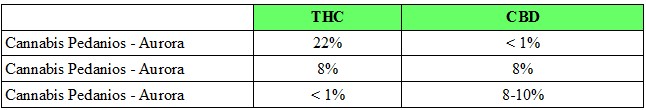
- cannabis ad alto contenuto in THC 22% e < 1% CBD
- cannabis con THC 8% e CBD 8%
- cannabis con basso THC < 1% e alto CBD 8-10%
ovvero 3 varietà da sovrapporre (come contenuto in THC e CBD) a quelle esistenti, cannabis medica olandese e cannabis medica italiana. I dati sono riportati qui di seguito:
Una fondamentale differenza rispetto alle altre varietà di cannabis terapeutica legali e prescrivibili dal Medico in Italia è che la varietà cannabis Pedanios Aurora NON ha nome di marchio (es. Bediol, FM2, ecc…), ma è identificata solo dal contenuto in THC e CBD.
Cosa cambiò nel panorama della cannabis terapeutica italiana con la cannabis Pedanios del 2018?
Si aprirono 2 nuovi scenari:
- il Medico in ricetta può indicare anche solo il titolo in THC della cannabis, senza specificare un nome di marchio (es. Cannabis flos/infiorescenze 22% THC).
- davanti ad una generica ricetta di (es.) Cannabis flos/infiorescenze 22% THC, il farmacista può dispensare (di sua volontà? In base a quello che c’è? Sentito o non sentito il Medico? E lo deve dichiarare che lo ha sentito?) qualsiasi varietà di cannabis sovrapponibile (equivalente) tra quelle reperibili/disponibili. Più avanti verrà chiarito tutto.
Per chiarire meglio il punto 2, si consideri la seguente tabella di confronto:
| Cannabis Medica | Varietà | Olandese | Italiana | Canadese |
|---|---|---|---|---|
| 22% THC <1% CBD | SATIVA | Bedrocan | – | Pedanios |
| 14% THC <1% CBD | INDICA | Bedica | – | – |
| 12% THC <1% CBD | SATIVA | Bedrobinol | – | – |
| 7.5-8% THC 8-12% CBD | SATIVA | Bediol | FM2 | Pedanios (INDICA) |
| < 1% THC 9% CBD | SATIVA | Bedrolite | – | Pedanios (HYBRID) |
In base a questa, il Medico che volesse prescrivere una varietà di cannabis con il 22% in THC, potrebbe scegliere tra Bedrocan e Pedanios. Oppure se volesse prescrivere Bediol, potrebbe “sostituirlo” con FM2 o Pedanios 8/8.
Quando saranno disponibili queste varietà di marijuana canadese?
Secondo stime ufficiale degli addetti ai lavori, si potranno avere i primi lotti disponibili in Italia verso FINE Febbraio 2018. Inizio o fine… non si sa. Si consideri che alla data della pubblicazione del presente articolo, ancora non sono state aperte le buste con le offerte della cannabis Pedanios Aurora.
Questa cannabis Pedanios verrà venduta (come acquirente) al Ministero della Difesa e importata presso lo Stabilimento Chimico Farmaceutico Militare di Firenze affinché la distribuisca alle Farmacie Italiane che ne faranno richiesta.
Le altre varietà di cannabis continueranno a essere importate e vendute sempre come prima (v. articolo).
Cambierà qualcosa a livello prescrittivo?
FORSE. Le modalità prescrittive e i facsimile presenti su questo sito sono state aggiornate A QUESTO ARTICOLO è possibile reperire facsimile di ricette mediche ed indicazioni tecnico normative sulla prescrizione di cannabis Pedanios, BedrocanBV (olandese) e italiana.
Il “forse” è perché se da una parte si vuole rendere più facile l’accesso alla cannabis (ovvero, con una ricetta generica di “Cannabis 22%”, si può avere la varietà olandese o canadese senza rifare la ricetta), dall’altra non è detto che 2 varietà aventi lo stesso contenuto in THC e/o CBD siano considerabili sovrapponibili a priori.
Cambierà qualcosa a livello di prezzo di cannabis con la cannabis Pedanios Aurora?
No, assolutamente. Il prezzo di vendita della cannabis ai pazienti è fisso e stabilito per Decreto Ministeriale ed è immodificabile: 9€/grammo + IVA + costi di produzione del Farmacista. Si veda l’articolo dedicato.
Farmagalenica.it invita pubblicamente sia Spektrum che Pedanios a rilasciare una intervista/dichiarazione su sito.
Per approfondire meglio la situazione della cannabis medica in Italia (perché non si trova più cannabis fino a fine gennaio? la risposta è qui), Farmagalenica è lieta di pubblicare la prima intervista in esclusiva a Aurora/Pedanios a mezzo di Andrea Ferrari, ha intervistato la vincitrice del Bando, a mezzo di Andre Ferrari, direttore vendite per il mercato italiano (vedi ultimo paragrafo della pagina).

Bando del 2019 per importazione cannabis medica [informazioni storiche, non aggiornate ad oggi]
Il bando si aprì nel Giugno 2019 ed è alla data attuale, tutt’ora in corso.
I documenti del bando sono reperibili a questa pagina.
Le ditte partecipanti al bando importazione cannabis medica nel 2019 sono 5:
- WAYLAND ITALIA
- TILRAY PORTUGAL
- MEDICINAL ORGANIC CANNABIS AUSTRALIA
- AURORA DEUTSCHLAND
- CANOPY GROWTH GERMANY
Il 03 Luglio 2019, alla presentazione dell’offerta NESSUNA dei partecipanti ha fornito una documentazione completa e formalmente corretta (fonte:)
Per questo motivo, il bando si è “prolungato” di circa 10 giorni per permettere ai partecipanti di sanare le irregolarità.
Le buste con le offerte non sono ancora state aperte.
Update: vince Aurora, tutti e 3 i lotti del bando. Per i prossimi 2 anni, in Italia avremo le stesse varietà del 2018:
| Cannabis Medica | Varietà | Olandese | Italiana | Canadese |
|---|---|---|---|---|
| 22% THC <1% CBD | SATIVA | Bedrocan | – | Pedanios |
| 14% THC <1% CBD | INDICA | Bedica | – | – |
| 12% THC <1% CBD | SATIVA | Bedrobinol | – | – |
| 7.5-8% THC 8-12% CBD | SATIVA | Bediol | FM2 | Pedanios |
| < 1% THC 12% CBD | SATIVA | Bedrolite | – | Pedanios (HYBRID) |

Intervista esclusiva per Farmagalenica a Pedanios Italia nel 2018
Segue il testo integrale realizzato a inizio 2018, all’indomani della vincita del bando da parte di Aurora
Buongiorno Andrea, chi è e qual è il Suo ruolo presso Aurora/Pedanios?
Sono direttore vendite per il mercato italiano e il mio background è di carattere tecnico-commerciale in ambito internazionale.
Aurora e Pedanios. Quali differenze tra le 2 società?
Pedanios GmbH è la società tedesca che ha partecipato e vinto il bando di gara indetto dal Ministero della Difesa Italiano. Pedanios è la filiale europea di proprietà 100% di Aurora Cannabis Inc. ed è un’azienda certificata GMP in Germania per import, export, immagazzinamento e distribuzione all’ingrosso di cannabis medica. In futuro la nostra filiale potrebbe anche diventare produttore di cannabis medica, in caso di vincita del bando per l’assegnazione di 10 licenze alla produzione di cannabis medica sul suolo tedesco.
La nostra casa madre Aurora Cannabis Inc. è, invece, una società canadese che coltiva cannabis terapeutica con la certificazione GMP per la produzione. Con una capitalizzazione in borsa di quasi 5 miliardi di €, è uno dei due più importanti produttori mondiali. È in fase di avviamento il nostro nuovo sito produttivo Aurora Sky con 80.000 mq di superficie coperta, un impianto di coltivazione e raccolta completamente automatizzato, una logistica integrata (direttamente nel sito di un aeroporto internazionale) e con una capacità produttiva di 100 tonnellate/anno di cannabis di altissima qualità.
Dove viene coltivata la cannabis medica di Aurora?
In Canada, indoor in serre ermetiche. La coltivazione in Canada nel medio periodo sarà destinata, prevalentemente, al mercato nazionale e meno all’export. Difatti a partire dal 18 luglio di quest’anno, il Canada legalizzerà l’utilizzo della cannabis anche per uso ricreativo in tutto il paese rendendo necessario un ulteriore incremento della produzione.
Produrremo nel medesimo sito, seppure in sezioni separate, sia cannabis terapeutica (con certificazione GMP e standard di controllo elevatissimi) che cannabis per uso ricreativo (con standard comunque molto alti).
Per quanto riguarda l’Europa, oltre alla licenza che stiamo cercando di ottenere per la coltivazione in Germania e per la quale abbiamo già identificato un sito strategico, abbiamo costituito una joint-venture in Danimarca chiamata Aurora Nordic Cannabis con la quale stiamo costruendo un impianto con una capacità produttiva annua di 120 tonnellate per servire il mercato scandinavo.
In Australia, altro mercato in forte fermento, abbiamo acquisito grosse quote della Cann Group, prima azienda ad avere in questo paese la licenza per coltivare cannabis. Tramite una serie di acquisizioni strategiche e grazie a una crescita organica sui principali mercati intendiamo consolidare la nostra posizione di leadership mondiale.
Il nostro obbiettivo in ogni paese è di produrre localmente, vicino ai nostri pazienti.
Come dimostrato, infine, dalle nostre attività in settori tecnologici limitrofi, intendiamo affermarci come provider di prodotti e servizi per l’industria della cannabis e non solo come semplici produttori. Alcuni esempi di queste attività collaterali sono la nostra controllata Radient Technologies Inc. proprietaria di vari brevetti per l’estrazione dei principi attivi tramite il processo delle microonde oppure CanvasRx, la nostra azienda che si occupa di educazione e training del personale medico in Canada.
Bando italiano: avete vinto tutti e 3 i lotti richiesti. Un commento a caldo?
Siamo, naturalmente, molto soddisfatti del risultato. Dopo alcuni colpi di scena e due soccorsi istruttori, il bando si è fortunatamente concluso a nostro favore.
Vista l’urgenza delle forniture, il bando è stato indetto mediante procedura accelerata. Abbiamo dovuto correre parecchio per potere fornire in tempo tutta la documentazione ritenuta necessaria da parte delle autorità per garantire la qualità delle aziende e dei prodotti concorrenti e tutelare, quindi, la salute dei pazienti italiani.
I responsabili dell’Agenzia Industrie e Difesa (AID) e dello Stabilimento Chimico Farmaceutico Militare di Firenze hanno organizzato e gestito questo bando con molto professionalità e trasparenza. Come azienda straniera partecipante per la prima volta a un bando di gara europeo in Italia, abbiamo avuto tutto il supporto e la disponibilità da parte dei responsabili del procedimento.
Il nostro più grosso concorrente a livello mondiale, anch’esso partecipante al bando di gara, ha fatto un’offerta molto competitiva e alla fine abbiamo vinto per poco. Questo testimonia la genuinità e l’alta competitività del bando di gara.
Ci siamo aggiudicati il bando a un prezzo di 320.000 € con un ribasso di quasi la metà rispetto alla base d’asta fissata a 570.000 €. I pazienti italiani, quindi, potranno avere presto accesso a prodotti di alta qualità mentre lo Stato potrà ottenere un risparmio economico [per Decreto Ministeriale, il prezzo di vendita al pubblico della cannabis medica è fisso a 9€/g indipendentemente dal prezzo di acquisto, ndr].
Forniremo in prima battuta le 3 varietà Pedanios richieste. Le nostre varietà standard sono 5: 2 con THC alto, 2 con CBD alto, 1 bilanciato.
Quando arriveranno le prime importazioni di cannabis Pedanios in Italia?
Ci sono i tempi di autorizzazione all’esportazione e all’importazione (le cosiddette import/export licences) che dipendono dalle autorità canadesi, tedesche e italiane. Da parte nostra ci impegneremo al massimo per fare arrivare prima possibile i prodotti ai pazienti. Stimiamo che la merce potrebbe arrivare verso fine febbraio.
Una volta importato dallo Stabilimento Chimico Farmaceutico Militare di Firenze, le farmacie potranno ordinarlo utilizzando il normale sistema dei buoni di acquisto.
Il bando riguarda 100 Kg. Esauriti i 100 KG che succederà?
Il bando permette di aumentare queste quantità di alcune decine di KG senza indire una nuova gara. Non sappiamo ancora quali sono le intenzioni e il programma di acquisto del Ministero su successive forniture. È comunque probabile che queste quantità siano sufficienti per alcuni mesi ma non per coprire l’intero fabbisogno dell’anno 2018.

Bando importazione cannabis medica del 2022
Questo bando rappresenta FINALMENTE qualcosa di diverso e concreto (non risolutivo però) nel panorama della cannabis per un motivo:
è il primo bando con un quantitativo “interessante” di infiorescenze importate, ossia 630 Kg
Domande semplici sul bando per l’ importazione cannabis terapeutica di Settembre 2022
Per approfondire l’argomento del bando del Ministero della Difesa (link ufficiale) per l’ importazione cannabis terapeutica, abbiamo chiesto ad un veterano, già noto ai lettori del sito: Andrea Ferrari, advisor per Aurora prima e LGP a tutt’oggi.
Aspetti positivi del bando importazione cannabis terapeutica di Settembre 2022
Criticità del bando importazione cannabis terapeutica di Settembre 2022
Quando arriverà effettivamente la cannabis del bando nelle farmacie italiane?
Per cercare e visualizzare la Farmacie di Farmagalenica in grado di preparare cannabis terapeutica consultare il motore di ricerca cercagalenico.it (si aprirà una nuova pagina).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Importazione cannabis medica, bando italiano e farmacie sembra essere il primo su Farmagalenica.
]]>L'articolo CBD stupefacente in Italia dopo Epidyolex? No,Si,Forse sembra essere il primo su Farmagalenica.
]]>Articolo originale pubblicato a Febbraio 2018.
Aggiornato il 15 Ottobre 2020
Ri-Aggiornato il 22 e 29 Ottobre 2020
Ancora-aggiornato a Giugno 2021
Nuovamente aggiornato a Agosto e Settembre 2023
E ancora: aggiornato ancora a Ottobre 2023 e Febbraio 2024
Neverending story: aggiornato a Luglio 2024
Il 26 Giugno 2018 è stato approvato, come ampiamente previsto e con una precisione svizzera, il farmaco Epidyolex® (non Epidiolex) della GW Pharma (la stessa ditta che commercializza il Sativex®) per il mercato americano (tramite la FDA).
Nel Giugno 2019 è arrivata l’approvazione dell’EMA per l’Europa a cui è seguito tutto quello che leggerete in questo articolo.
Nell’Ottobre 2020 è arrivata la modifica normativa che classifica in Italia l’ Epidyolex come farmaco stupefacente in sez. B (come la cannabis medica), modifica poi sospesa dal Ministro della Salute, Speranza. La sospensione è stata poi revocata il 21 Agosto 2023 con il Decreto del Ministero della salute del 7 agosto 2023. Poi il TAR del Lazio ha sospeso a sua volta questo decreto, cui il MInistero si è appellato al Consiglio di Stato con udienza a Settembre 2024. E nel mentre è arrivato il Decreto 27 Giugno 2024 che ha ripristinato ancora… insomma un casino :D. Leggete e verrà spiegato.
Farmagalenica.it si occupa dell’argomento per la ricaduta che potrà avere avrà questo farmaco, derivato naturale dalla cannabis medica, sul mondo galenico italiano, in particolare per il panorama del CBD e del suo utilizzo, che da Settembre 2023 è diventato “stupefacente”, anzi no, però… però alla fine sì.
La prima parte dell’articolo tratta brevemente di cosa è Epidyolex, se vi interessa la questione del CBD “stupefacente-che-non-lo-è-però” potete saltare direttamente a metà articolo.
Quando arriverà l’ Epidyolex in Italia?
Non c’è ancora una data esatta, ma potrebbe essere prima della fine del 2020, massimo inizio 2021..
Manca solo il rilascio dell’AIC da parte dell’AIFA. Nel corso del 2019 e 2020, comunque, Epidyolex è già stato utilizzato in alcuni centri italiani come cura compassionevole
A Giugno 2021 con pubblicazione in Gazzetta Ufficiale 149 del 24 giugno 2021, l’Epidyolex è entrato in commercio in Italia, come farmaco non stupefacente soggetto a ricetta medica non ripetibile limitativa (neurologo, neuropsichiatra infantile, pediatra).
Che cos’è Epidyolex?
Epidyolex è un farmaco prodotto dalla G. W. Pharma a base di cannabidiolo (CBD) ottenuto naturalmente da fiori di cannabis medica (genetiche proprietarie della G. W. Pharma), le cui indicazioni terapeutiche autorizzate sono il trattamento di 2 forme di epilessia farmacoresistente:
- sindrome di Lennox-Gastaut
- sindrome di Dravet o epilessia mioclonica grave dell’infanzia
Va anche detto che in base alla normativa offlabel (L. 94/98), il farmaco potrà essere utilizzo anche al di fuori delle indicazioni terapeutiche autorizzate se ne ricorrono le condizioni.
Si presenta in forma di sciroppo oleoso (in olio di arachidi raffinato di grado farmaceutico) aromatizzato, con siringa dosatrice in modo da poter aggiustare il dosaggio in base al peso corporeo del bambino.
FONDAMENTALE: Epidyolex è un farmaco ottenuto per estrazione del CBD (in anidride carbonica supercritica) dal fiore della cannabis, quindi NON è UN FARMACO DI SINTESI, ma contiene CBD naturale.
Ma se il CBD non è stupefacente, perché Epidyolex è stupefacente? La risposta più sotto.
Per ulteriori informazioni, si rimanda al sito ufficiale della ditta produttrice, G. W. Pharma.
Quali sono i principali effetti collaterali dell’ Epidyolex ® e come si usa?
Stando alle indicazioni della ditta produttrice, i principali effetti collaterali principali (da comune a molto comune) sono:
- diarrea
- debolezza
- diminuzione dell’appetito
- sonnolenza/stanchezza
- eruzioni cutanee
- sonno disturbato (all’inizio del trattamento)
La posologia prevede la somministrazione di 2 dosi al giorno, calcolate con il dosaggio che va da 5mg/Kg a 20 mg/Kg da dividere, appunto, in 2 (es. paziente di 10Kg, dovrà assumere 25mg di CBD al mattino e 25mg di CBD alla sera).

Quale impatto potrà avere l’entrata in commercio dell’ Epidyolex in Italia per quanto riguarda il mondo del CBD?
Sarà una rivoluzione. Piccola o grande non è possibile saperlo con certezza, ma non servirà una Legge ad hoc: basterà applicare quelle esistenti.
Dr. Marco Ternelli nel Febbraio 2018
La citazione sopra, scritta nel 2018 è stata una azzeccata previsione.
Infatti, nella Gazzetta Ufficiale del 15 ottobre 2020 (scarica qui) che doveva entrare in vigore il 30 Ottobre 2020, sono stati pubblicati tre decreti del Ministero della Salute dell’1 ottobre 2020, che tra l’altro inserisce
Nella tabella dei medicinali, sezione B, del decreto del Presidente della Repubblica 9 ottobre 1990, n. 309,e successive modificazioni, è inserita, secondo l’ordine alfabetico, la seguente categoria di sostanze: composizioni per somministrazione ad uso orale di cannabidiolo ottenuto da estratti di Cannabis.
che al mercato mio padre comprò…
PRIMA DI PROSEGUIRE: con Decreto del Ministro della Salute del 28/10/2020, il decreto è stato SOSPESO (non cancellato) in attesa di ulteriori pareri da ISS e CSS. Quanto segue, quindi NON è ancora in vigore alla data dell’ultimo aggiornamento di questo articolo.Il Decreto del 7 Agosto 2023 è stato pubblicato in gazzetta del 21 Agosto 2023 ed entrerà in vigore entro 30 giorni se non modificato.E ancora: il TAR del Lazio a Gennaio 2024 ha sospeso il Decreto che sospendeva la sospensione, fino a Settembre 2024, in attesa dell’udienza con cui il Ministero della Salute ha ricorso al Consiglio di Stato contro la decisione.
Nuovo colpo di scena: il 6 Luglio è stato pubblicato il Decreto del 27 Giugno 2024 che abroga tutti i precedenti (quindi invalida la sentenza del TAR) e rende stupefacente gli orali di CBD estratto naturale dal 5 Agosto 2024.
Ormai è una comica…
Di fatto, il Decreto che revoca la sospensione entrerà in vigore il 30simo giorno dalla data di pubblicazione cioè il 20 settembre 2023. Da quel giorno succederà quello che state per leggere.
Non più, il Decreto è stato sospeso quindi quello che leggerete è cosa POTREBBE tornare a succedere da Gennaio Settembre 2024.
A Gennaio 2024 infatti, il TAR ha rinviato l’udienza al 16 Settembre 2024.
Ed eccoci: è stato pubblicato, nel luglio 2024 un nuovo decreto che rende stupefacenti i prodotti orali con CBD estratto naturale. Quel che leggere, di seguito, è dunque quello che POTREBBE succedere è successo dal 5 Agosto 2024 (data di entrata in vigore del DM di cui sopra).
Il CBD è diventato una sostanza stupefacente?
NO
Lo si ripete: il cannabidiolo naturale o il cannabidiolo sintetico NON sono stati classificati come sostanze stupefacenti in quanto tali.
Affinchè il CBD in quanto tale fosse stupefacente, nella Tabella dei Medicinali sez. B andava aggiunta questa semplice parola:
cannabidiolo
Questo avrebbe significato che qualsiasi (conoscete il significato della parola qualsiasi giusto?) prodotto esistente contenente CBD (naturale o sintetico) sarebbe stato stupefacente. Ma così non è.
Il Decreto, infatti, parla precisamente di COMPOSIZIONI ossia medicinali (galenici o industriali) ad uso orale che contengono CBD ottenuto da estratti di cannabis.
Detto in maniera discorsiva: non è stupefacente il CBD in quanto tale (in in quanto molecola), ma la COMPOSIZIONE AD USO ORALE che lo contiene SE E SOLO SE il CBD presente è estratto naturalmente.
AD USO ORALE: non è solo “olio”, ma anche “altri estratti”, “capsule”, “tinture”, chewing-gum
È ovvio ma va esplicitato
Ancora un esempio:
- Epidyolex fatto con CBD estratto naturalmente è stupefacente
- Epidyolex fatto con CBD sintetico (non esiste questo Epidyolex, è un esempio concettuale) NON è stupefacente
CBD stupefacente? Solo se a uso orale. Come si spiega?
Quello che è stupefacente dunque non è il CBD (inteso come sostanza dotata di una unica e precisa), ma quello che sta attorno al CBD:
- se CBD estratto naturalmente (es. puro al 99.3%), attorno (quello 0.7%) sicuramente avrà materiale vegetlae, tracce di terpeni e una minima quantità di THC. Questo intorno con THC rende il CBD estratto naturale stupefacente, quando contenuto in prodotti ad uso orale!
- se CBD sintetizzato chimicamente (es. puro al 99.3%), attorno (quello 0.7%) conterrà residui di solventi (e altro coff coff…). Questo intorno senza THC (coff coff…!!) rende il CBD sintetico NON stupefacente.
Se la molecola di CBD fosse stupefacente, non sarebbe possibile questa distinzione naturale-sintetico
Cosa cambia per i prodotti con CBD per uso NON orale?
Ora, che succede a tutti quei prodotti (oli, capsule, uso tecnico, ecc…) che contengono CBD?
In base a quanto sopra, la differenza la fa solo il tipo di CBD usato.
CBD Naturale
Tutte le composizioni (prodotti) contenenti CBD naturale sia ad uso orale che non, ora, sono stupefacenti:
- farmaci
- integratori (non ne esistono attualmente in Italia)
- prodotti uso tecnico
- prodotti ottenuti dalla canapa
Per essere più chiari possibile:
- oli di CBD uso tecnico/mondo grigio al CBD? Farmaci stupefacenti, in quanto ad uso orale
- capsule di CBD nel mondo extra-faramcia? Farmaci stupefacenti, in quanto ad uso orale
- i cristalli uso tecnico/mondo grigio di CBD? Farmaci stupefacenti, in quanto potenzialmente ad uso orale
- infiorescenze di canapa ad uso tecnico? Eh… bella domanda. Contengono CBD e potenzialmente possono essere ingerite ossia ad uso orale. Ma non sono estratti. A parare di chi scrive sono esclusi dal Decreto.
- cosmesi. In teoria non sarebbe dobuto cambiare nulla, non essendo i cosmetici ad uso orale. Una circolare del Ministero della Salute sul Decreto in questione, invece, li VIETA se composti da CBD estrattivo naturale. Boh…
CBD Sintetico
Tutte le composizioni (prodotti) contenenti CBD sintetico sia ad uso orale che non orale, non sono stupefacenti.
Perchè hanno classificato stupefacente le composizioni con CBD naturale e non il CBD molecola?
Il razionale è che durante il processo estrattivo del CBD dalla pianta (Cannabis, che contiene THC) non è possibile escludere completamente la presenza di THC come residuo. Per questo, un farmaco che contiene CBD estratto naturalmente potrebbe contenere una sostanza classificata stupefacente, il THC (tetraidrocannabinolo).
Inoltre, l’OMS nel 2018 ha rimosso il CBD dalle sostanze aventi azione stupefacente e psicotropa.
Si noti che questa distinzione è la stessa operata in Europa sul CBD ad uso cosmetico.

Altre motivazioni, politiche e non (es. la necessità di fornire grazie ai consumatori) le trovate nell’intervista rilasciata dalla Sottosegretaria ad Economia e Finanze.
Che succede ai prodotti NON farmaceutici (es. olio di CBD da canapa) che contengono CBD naturale?
(forse) Nulla, per quanto se ne può dire oggi.
Il Decreto infatti NON ha portato alcuna modifica alle Tabelle I, II, III, IV e V degli stupefacenti (ad uso illecito), ma solo ai medicinali, cioè non ha inserito le composizioni per somministrazione ad uso orale di cannabidiolo ottenuto da estratti di Cannabis come prodotti stupefacenti.
In seguito ai chiarimenti ricevuti a Ottobre 2020 dall’UCS, lo scenario vigente dal 30 Ottobre 2020 sarà il B.
Questo può portare a 2 scenari.
Scenario A (purtroppo non il più seguito)
Il CBD naturale NON è stupefacente, lo sono le composizioni medicinali che lo contengono.
Gli oli/capsule di CBD da canapa/hemp non stupefacente NON sono medicinali
E quindi non essendo medicinali non ricadono nella Tabella dei Medicinali.
E non ricandendo nella Tabella dei Medicinali NON seguono i dettami del nuovo decreto.
Scenario B
In questo caso, si sostiene che solo un farmaco potrebbe contenere CBD naturale ad uso orale ossia deve essere autorizzato dall’AIFA (Agenzia Italiana del Farmaco).
Detto altrimenti: qualsiasi prodotto che contiene CBD naturale ad uso orale non potrà essere prodotto/commercializzato a meno che non sia un medicinale autorizzato dall’AIFA (!). Ergo, può essere prodotto solo da una officina farmaceutica, oltre ad essere stupefacente.
Per riassumere in maniera chiara, per quanto riguarda il CBD naturale di libera vendita fuori dal canale farmacia (quello venduto negli Hemp Shop o negozi di cannabis light o erboristerie), ci sono diverse considerazioni da fare:
- CBD naturale in cristalli da canapa:
probabilmente verràvietato completamente, in quanto materia prima “pura” stupefacente. - oli o estratti di canapa ad uso orale contenenti CBD naturale in cristalli: ne abbiamo appena parlato, vietati in quanto contenenti sostanza stupefacente.
- prodotti ad uso tecnico contenenti CBD: anche questi, vietati in quanto contenenti una sostanza stupefacente.
- cannabis light infiorescenze: grande incognita, anche se, volendo seguire un ragionamento puramente logico, dovrà essere vietata completamente in quanto fonte di CBD, materia prima dotata di attività terapeutica in un farmaco e stupefacente. Ma consideriamo che non è un estratto, quindi a parere di chi scrive non sono toccate dal decreto.
L’articolo verrà aggiornato se ci saranno ulteriori sviluppi.
Cosa cambierà in Farmacia a livello di preparazioni galeniche di cannabis medica o CBD?
Per i pazienti (che già acquistavano in farmacia il CBD con ricetta medica) non cambierà nulla!
Anche qui, ci sono 2 scenari.
Farmaco galenico preparato con CBD sintetico
Non cambia assolutamente nulla.
- il CBD sintetico NON è stupefacente
- il medicinale galenico preparato dal farmacista, essendo ottenuto da CBD sintetico, non è stupefacente
- è richiesta sempre la solita ricetta non ripetibile secondo la Legge 94/98
Non cambia nulla.
Farmaco galenico preparato con CBD naturale [GUIDA PER IL FARMACISTA]
A partire dal 30 Ottobre 2020 5 Agosto 2024 il CBD estratto naturale (E SOLO QUELLO) presente in farmacia andrà caricato e scaricato dal Registro Stupefacenti (es. registro elettronico).
Per fare questo, con data 05/08/2024 il farmacista Galenista:
- peserà e caricherà la quantità di CBD estratto naturale presente in farmacia
- indicherà come motivazione di carico “DM 27 Giugno 2024” riportando la giacenza totale.
Da quel momento, il CBD andrà ordinato dal Farmacista al grossista con Buono acquisto, come tutte le sostanze stupefacenti e scaricato quando viene utilizzato.
I certificati di analisi del CBD rimangono allegati al flacone della materia prima, senza necessità ulteriori.
In questo scenario, QUALSIASI preparazione (anche uso topico o altro) fatta con questo CBD estratto naturale, orale o non orale, andrà scaricata dal registro in quanto farmaco stupefacente in Tabella dei Medicinali sez. B.
[Edit: in realtà lo scarico avverrà sempre e comunque, ma per una crema il prodotto non è ad uso orale, quindi non sarà stupefacente.]
Di seguito, le slide del Dr. Marco Ternelli sulle modifiche normative a adempimenti per il Farmacista per la gestione del CBD estratto naturale in farmacia nelle preparazione galeniche:
CBD e DM Giugno 2024 in Farmacia di MarcoTabella riassuntiva sul CBD galenico e ricette mediche
Per districarsi in questo caos, ecco una pratica tabella contenente tutti i casi possibili con CBD sintetico, naturale, ripetibilità ricetta e varie.
| CBD NATURALE ORALE | CBD NATURALE NON ORALE | CBD SINTETICO ORALE o NON ORALE | |
|---|---|---|---|
| Ricetta con nome e cognome del paziente (es. uso cosmetico) | non ripetibile, valida 30 giorni escluso quello di emissione | (solo inlabel) ripetibile, valida 6 mesi | (solo inlabel) ripetibile, valida 6 mesi |
| Ricetta con codice [alfa]numerico (off-label) | non ripetibile, valida 30 giorni escluso quello di emissione | non ripetibile, valida 30 giorni escluso quello di emissione | non ripetibile, valida 30 giorni escluso quello di emissione |
| Conservazione della ricetta medica | 2 anni dalla data dell’ultima registrazione | almeno 6 mesi dalla spedizione | almeno 6 mesi dalla spedizione |
E per chi assume cannabis terapeutica (es. Bedrocan, Bediol, Bedrolite, ecc…) cosa cambia?
NULLA!
Il provvedimento riguarda il CBD, non la cannabis
E chi comprava oli di CBD da canapa o nei cannabis shop?
Ora l’unico modo legale è acquistarlo in farmacia con ricetta medica.
QUALSIASI MEDICO può fare una ricetta per il CBD; per informazioni sul tipo di ricetta, formalismi, esempi c’è l’articolo apposito.
C’è altro sulla legislazione CBD?
Rimarrà il nodo di cosa succederà quando il Medico vorrà utilizzare cannabis medica con CBD per il trattamento di epilessia: probabilmente nulla di problematico, dato che la cannabis medica NON è CBD, ma un insieme di tante altre sostanze dotate di attività terapeutica (tra cui il CBD e il THC).
Altrettanto sarà possibile per il Farmacista continuare ad utilizzare CBD in GMP per la preparazione di farmaci galenici con ricetta medica, come già avviene tutt’ora, secondo quanto disposto dalla Legge 94/98 (“Di Bella”).
Come si potrà acquistare l’ Epidyolex in Italia per l’epilessia farmacoresistente?
Volendo concludere l’articolo con il farmaco industriale di apertura, trattandosi di un farmaco soggetto a ricetta medica non ripetibile, sarà necessaria la prescrizione di un Medico specialista (neurologo, neuropsichiatra infantile, pediatra).
Inizialmente, il suo uso sarà probabilmente limitato all’ambiente ospedaliero, ma potrà essere acquistato a pagamento anche in Farmacia.
Per visualizzare le Farmacie di Farmagalenica in grado di preparare farmaci galenici con il CBD sintetico, consultare il motore di ricerca Cercagalenico.it (si aprirà una nuova pagina).
Per ogni domanda o dubbio, lasciare un messaggio nei commenti qui sotto.

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo CBD stupefacente in Italia dopo Epidyolex? No,Si,Forse sembra essere il primo su Farmagalenica.
]]>L'articolo Ricetta galenica elettronica via PEC: si può, ma… sembra essere il primo su Farmagalenica.
]]>La spinta a questo articolo viene, come molte cose negli ultimi mesi, dalla situazione di emergenza causata dal COVID-19 (Coronavirus).
DISCLAIMER: le informazioni contenute in questo articolo sono da ritenersi come meri ragionamenti teorici e spunti legislativi su cui riflettere. L’iniziativa di mettere in pratica quanto esposto è personale.
In un momento in cui le persone non possono spostarsi o devono limitare al minimo gli spostamenti, una delle domande più chieste dai pazienti alle Farmacie Galeniche di Farmagalenica (che cioè preparano farmaci galenici) è “Ma posso inviarvi la ricetta via email? È valida?“
Per quanto riguarda la ricetta galenica elettronica, andiamo a scoprire la risposta in questo articolo.
Before we begin: la tesi del Ministero a Farmagalenica: NON SI PUO’
Il 3 Settembre 2021 il Ministero della Salute ha diramato una circolare in cui, citando questo articolo, fornisce una diversa interpretazione e riporta che non è possibile accettare una ricetta medica via PEC con firma digitale di cannabis medica.
E’ possibile scaricare di seguito la circolare:
Vale la pena di notare come tutti i dettami riferiti alla dematerializzazione delle ricette bianche NON siano validi per le ricette galeniche, come indicato dallo stesso Ministero con nota X/2021.
Inoltre, quando il Ministero dice
non garantisce al Farmacista che analogo invio sia stato fatto [dal Medico, ndr.] ad altra farmacia, pertanto [omiss…]
viene spontaneo chiedersi: e quindi? Non avviene forse lo stesso con le ricette bianche cartacee? Quando il medico redige più copie della stessa ricetta medica non ripetibile (a tutti è capitato di vederle) o ogni volta che il Farmacista spedisce una ricetta non ripetibile, che ne sa se il paziente è già stato in un’altra farmacia a ritirare un medesimo medicinale con un’altra ricetta?
O quando dice che per la PEC
non è prevista dalla normativa vigente in materia di digitalizzazione l’impiego della PEC tra soggetti diversi.
c’è qualcuno che possa indicare nei commenti in quale occasione l’uso di PEC fuori dalla Pubblica Amministrazione, es. tra aziende (che so… tra farmacia e azienda per il Buono acquisto stupefacenti) o tra privati non è consentito? Perché quanto il Ministero sostiene, non collima da quello che è spiegato qui.
Più avanti nell’articolo, i punti verranno ripresi e discussi approfonditamente.
Ad ogni modo, l’articolo come sempre indicato nel disclaimer sopra, rimane valido per una digressione normativa ed appigli 
Un “curioso” errore su tutti: niente REV galeniche?
Il Ministero, nella circolare con cui ritiene le PEC non siano valide, scrive che
Per quanto riguarda la dematerializzazione delle ricette veterinarie, sono altresì esclusi dalla dematerializzazione con REV (ricetta elettronica veterinaria) i medicinali contenenti stupefacenti e i medicinali prescrivibili con ricetta magistrale secondo le disposizioni [omiss…]
dove sembra dimenticare che la prescrizione di galenici magistrali veterinari non stupefacenti è regolamentata dal Decreto Ministeriale 8 febbraio 2019 che prevede esplicitamente la prescrizione tramite REV di galenici magistrali, come spiegato qui.
Nel frattempo FEDERFARMA corre ai ripari con una propria circolare dove riporta che
Tale interpretazione, legata alla locuzione usata dalla Direzione generale del Ministero responsabile dell’estensione di tale Nota, non può, tuttavia, essere in alcun modo condivisa dalla scrivente, in quanto un’interpretazione siffatta sarebbe da considerare contra legem. Pertanto, invitiamo le farmacie a continuare ad utilizzare la ricetta elettronica veterinaria (REV) per tutte le prescrizioni medico-veterinarie relative a formule magistrali e officinali.
Circolare FEDERFARMA 12923/495/F7/PE del 09/09/2021
In conclusione:
Le REV galeniche continuano a essere valide! Non in virtù delle circolari (che non hanno rango di legge), ma in virtù del DM 08/02/2019 che le ha istituite.
Il lettore si domanderà: ma se c’è un errore così grossolano su un argomento del genere, è legittimo chiedersi se non ci siano altri errori nelle spiegazioni fornite?
Update: il 18 Ottobre il Ministero rettifica la comunicazione, indicando di sostituire il paragrafo incriminato con il seguente che si allinea alla norma:
Per quanto riguarda la dematerializzazione delle ricette veterinarie, sono altresì esclusi dalla dematerializzazione con REV (ricetta elettronica veterinaria) i medicinali contenenti stupefacenti con AIC e i medicinali prescrivibili con ricetta magistrale contenenti stupefacenti secondo le disposizioni della normativa vigente di cui è possibile trovare puntuale riferimento sul portale ufficiale del Ministero della salute ai seguenti link [omiss]
Circolare 0073403 del 18/10/2021
Da dove nasce la questione della ricetta galenica elettronica
In Italia, la dematerializzazione della ricetta medica è cominciata nel 2014 quando le ricette SSN (quelle “rosse”) sono state trasformate in promemoria cartacei, ossia fogli di carta che non hanno valore formale come ricetta medica, ma che contengono informazioni tecniche (codici ricetta e codice fiscale paziente) per accedere alla ricetta medica elettronica che ha “fisicamente” e “legalmente” sede online (nel SAC, per i più tecnici).
Ad essa sono seguiti nel gennaio 2019 la dematerializzazione della ricetta veterinaria, diventata ricetta elettronica veterinaria (REV) e ricetta elettronica veterinaria galenica (REVG).
A Febbraio 2020 sono diventati elettroniche anche le ricette SSN dei farmaci in DPC (Distribuzione Per Conto, per gli addetti ai lavori), semplicemente includendole come ricette del SSN.
Nel mondo Farmacia, mancano ormai solo 2 grandi categorie da trasformare in ricette elettroniche:
- farmaci stupefacenti, inclusa la galenica
- ricette bianche ad uso umano, inclusa la galenica
In questo tempo è stato chiesto a gran voce di trasformare le ricette c. d. galeniche “bianche” (cioè redatte sul ricettario privato del Medico) in ricette elettroniche per permettere ai pazienti, come già detto, di non uscire, di limitare i contatti, ecc… soprattuto per la ricetta galenica elettronica di cannabis terapeutica.
Ricetta bianca è il nome tradizionale delle prescrizioni su ricettario privato del Medico, che il paziente acquista di tasca propria.

Dovremo attendere molto per avere le ricette bianche e/o di stupefacenti come ricetta elettronica galenica?
No e Sì.
Con l’emergenza COVID-19 “la necessità aguzza l’ingegno”. Si tratta solo di istituire un sistema informatico simile a quello della Ricetta Elettronica Veterinaria (REV) ma applicandola all’umano, che tenga traccia online del farmaco prescritto e la quantità fornita (ed eventualmente residua).
Di fatto, però, la normativa attuale, permette (non vieta) modi alternativi di inviare una ricetta galenica elettronica bianca ad una Farmacia, purché siano rispettate tutte le normative ad oggi vigenti.
Ma non c’è una legge che permetta espressamente l’invio in formato digitale
Ricordate: Ubi lex voluit dixit, ubi noluit tacuit
Questa obiezione trova facile risposta nel principio espresso qui sopra (“Quello che la legge vuole dice, quello che non vuole tace”), molto applicato in campo farmaceutico: se non è vietato espressamente, allora vuol dire che si può fare. Qualche esempio:
- “non si può sconfezionare” dicevano. Poi è stato fatto ricorso fino al Consiglio di Stato il quale ha stabilito che si può sconfezionare perché la norma non lo vieta.
- “le farmacie galeniche territoriali non posso far ripartizioni sterili, solo le ospedaliere” dicevano. Poi è stato fatto ricorso fino al Consiglio di Stato il quale ha stabilito che anche le farmacie territoriali possono ripartire perché la norma non lo vieta.
- “solo gli OTC possono avere pubblicità, non i SOP” dicevano. Poi è stato fatto ricorso fino al Consiglio di Stato il quale ha stabilito che si può fare pubblicità ai SOP perché la norma non lo vieta.
- “non si può fare pubblicità ai farmaci galenici officinali” dicevano. Poi è stato fatto ricorso fino alla Corte di Giustizia Europea la quale ha stabilito che si può fare pubblicità agli officinali perché la norma non lo vieta.
Prima di procedere nella lettura, è opportuno avere chiari alcuni concetti che spesso sono dati per scontati o addirittura neppure si conosce che esistessero.
“Firma digitale” e “firma elettronica”: ci sono differenze?
Si.
Come spiegato bene in questo articolo,
- la firma elettronica non è sufficiente per dare validità ad una ricetta medica
- la firma digitale è quella forte ed è l’unica che può dare valore ad una ricetta medica sostituendosi alla firma autografa.
Per chi volesse approfondire tutte le leggi e l’impianto normativo che ha portato alla firma digitale, e come questa può sostituire una firma di pugno (autografa) nel 100% dei casi, può scaricare il PDF al link sottostante.
Per chi vuole ancora approfondire sulla validità, si rimanda a questa sentenza della Cassazione Sezioni Unite del 2017.
Volendo riassumere in un concetto semplicissimo,
nell’ordinamento giuridico italiano, la firma digitale a crittografia asimmetrica è riconosciuta ed equiparata a tutti gli effetti di legge alla firma autografa su carta.
https://www.arpae.it/dettaglio_generale.asp?id=1577&idlivello=1217
Normativa spicciola sui formalismi della ricetta bianca galenica
Un ulteriore passaggio per ripassare cosa dice esattamente la normativa vigente su obblighi del Medico che redige una ricetta bianca e del Farmacista che la spedisce, prima di entrare nel vivo della ricetta galenica elettronica.
Obblighi del Medico
Abbiamo che
I medici chirurghi ed i veterinari, che prescrivono le specialità sottoposte all’obbligo di cui al comma precedente, debbono indicare chiaramente nelle ricette, da scriversi con mezzo indelebile, il cognome, nome al quale le rilasciano ovvero del proprietario dell’animale ammalato; l’indicazione del modo di somministrazione o di applicazione nei riguardi del mezzo e del tempo; apporre sulla prescrizione stessa la data e la firma. La ricetta dovrà essere conservata dal Farmacista.
Art. 167 del R.D. 27 luglio 1934, n. 1265
Obblighi del Farmacista
Come da sopra,
[omiss..] La ricetta dovrà essere conservata dal Farmacista.
Art. 167 del R.D. 27 luglio 1934, n. 1265
Inoltre:
I Farmacisti hanno l’obbligo di annotare sulle ricette che spediscono, la data della spedizione ed il prezzo praticato;
Art. 37 del R.D. n. 1706/1938
Ancora, per le ricette galeniche è necessario che il Farmacista apponga nome e firma del preparatore.
La documentazione deve riportare
Sez. 5 “Documentazione in Farmacia” delle NBP Farmacopea Ufficiale Italiana XII ed
– [omiss]
– nome e firma del preparatore
ma ciò non deve necessariamente essere sulla ricetta medica, ma anche sul foglio di lavorazione in caso si adottino le NBP integrali.
Dulcis in fundo, nel caso di ricette bianche galeniche contenenti sostanze stupefacenti (es. cannabis terapeutica):
il Farmacista deve apporre timbro della Farmacia se le ricetta contiene sostanze stupefacenti.
Art.
Problemi e soluzioni connessi alla ricetta galenica elettronica
Posto che già a questo punto dell’articolo una buona parte dei lettori avrà formulato mille pensieri tra misto incredulità, sbigottimento, contrariazione, rifiuto, ecc… vediamo quali obiezioni o criticità presenta la ricetta galenica elettronica.
Il Farmacista non può apporre digitalmente timbro, data, prezzo praticato e firma
In pratica, i sostenitori di questa teoria ragionano più o meno così: “visto che il documento è digitale, va trattato solo come digitale: timbro, data, prezzo praticato e firma del Farmacista Galenista devono essere per forza poste digitalmente“. Quindi non si può perché tecnicamente non si può fare.
E chi l’ha detto che non si può fare tecnicamente?
Sulla questione firma del Farmacista, come spiegato nel capito precedente, non è obbligatorio riportarlo sulla ricetta medica. Altro non c’è da dire.
Per il resto sulla questione data, timbro, prezzo praticato da apporre sulla ricetta galenica elettronica esistono 2 opzioni:
- (versione “parato al 100%”) una volta ricevuto e verificata l’integrità della firma digitale del Medico sulla ricetta galenica elettronica, il Farmacista appone il timbro come immagine, aggiunge prezzo praticato come testo nel campo “note” della firma digitale; data e firma saranno apposte con la firma digitale del Farmacista. Fatto.
Questa operazione può essere ripetuta più volte sulla stessa ricetta galenica digitale ripetibile, fino ad esaurimento della ripetibilità. - prendendo spunto dal Ministero della Salute, che con Nota 43238 del 2009, spiega quali sono le normative che regolano la regolamentazione della firma digitale (“elettronica”), indicando addirittura come essa sia valida per il buono acquisto stupefacenti e che possa essere conservato in supporto informatico o cartaceo. Quindi, una volta ricevuto il Buono Acquisto Stupefacenti compilato e firmato digitalmente, il Farmacista lo stampa, lo compila a mano e lo detiene in cartaceo.
Esattamente come farebbe per la ricetta galenica elettronica.
Potete scaricare la nota Ministeriale al link qui sotto:
Una nota ministeriale NON crea legge. Esplica qualcosa che è già legge.
Per questo, è lecito sostenere che il ministero non fa altro che esplicitare qualcosa che già è permesso dalla normativa
Se anche quanto sopra è valido, quando si stampa la ricetta medica firmata digitalmente, essa non ha più valore
No.
La norma indica che il documento informatico siglato dalla firma digitale e tradotto in formato cartaceo manterrà la propria validità qualora risulti invariato in ogni suo aspetto e corrisponda in pieno all’originale digitale (v. spiegazione precedente).
Il Farmacista può modificare il file della ricetta prima di stampare il cartaceo
Falso problema.
È vero che in alcuni casi potrebbe essere modificato un file di una ricetta galenica elettronica (indipendentemente dal formato in cui arriva, .doc, .docx, .odt., .pdf, ecc…), ma ciò equivarrebbe ad una falsificazione di una regolare ricetta bianca cartacea.
Il punto è che “alterare” una ricetta (digitale o cartacea) è un reato. Punto.
Questo è un problema della persona (farmacista) che commette un reato, sia con una ricetta galenica digitale sia con una ricetta cartacea.
La soluzione? Intrinseca: la copia digitale ricevuta per email è integra e, in caso di controllo, si può verificare se la copia cartacea stampata e conservata in Farmacia è identica a quella ricevuta o presenta invece alterazioni.
Questa verifica, si noti, non è possibile su una ricetta cartacea (facilmente falsificabile) detenuta in Farmacia.
Ricordate che le leggi attuali sulle ricette “bianche” risalgono agli anni ’30 e ’60, quando computer, stampanti e tecnologia non esistevano.
Il sunto è: chiunque oggi, nel 2020 e successivi, può falsificare una ricetta bianca con un computer o timbro fatto fare ad hoc, ottenendo una ricetta formalmente corretta e al di sopra di qualsiasi sospetto.
A questo punto bisognerebbe impedire ai medici di redigere ricette bianche perché “potenzialmente falsificabili”. Come detto, falso problema.
La ricetta galenica elettronica, invece, non ha questo problema, essendo sempre presente e immodificabile nella email ricevuta (v. oltre).
La norma XYZ richiede che la ricetta sia in originale
Esempio nel caso di ricette non ripetibili, ricette stupefacenti, alcune ricetta con sostanze doping, eccetera.
Vero. E difatti la ricetta galenica elettronica con firma digitale rappresenta la copia originale e non ripetibile purché siano rispettate determinate condizioni (v. più avanti).
La ricetta galenica elettronica non è possibile renderla ripetibile
Certamente chi pone la questione ragiona più o meno così: “Poiché la ricetta ripetibile è di proprietà del paziente, essa va sempre restituita. Ma essendo digitale, la restituzione del cartaceo stampato non ha valore in quanto non è possibile accettarla una seconda, terza, ecc.. volta non avendo la firma del medico originale”.
La risposta parte da qui: la ripetibilità della prescrizione consente al paziente di ottenere più confezioni/dosi di un medicinale senza dover far rifare la ricetta al Medico. Nel momento in cui il Medico indica “non ripetibile” sulla ricetta galenica elettronica oppure il paziente di sua iniziativa rinuncia alla ripetibilità della ricetta (anche verbalmente), nulla obbliga il Farmacista a imporrare al paziente di dover usare la ricetta una seconda, terza, ecc.. volta.
E se poi il paziente cambia idea? Può richiedere al medico di redigere una nuova ricetta galenica elettronica, esattamente come farebbe per una cartacea che, pur essendo in possesso o meno di una ricetta cartacea ripetibile, può richiedere l’emissione di una nuova ricetta al Medico.
Il paziente non può dare delega al Medico
Qualcuno sostiene quanto segue:
“il decreto del 30/12/2020, in vigore dal 30/01/2021 non permette la delega del paziente al medico per l’invio del promemoria direttamente alla farmacia dallo stesso prescelta
FOFI
Il Decreto in questione è quello più noto per la dematerializzazione delle ricette bianche (che alla data dell’articolo non è ancora avvenuta nonostante il Decreto).
Quanto scritto sopra è FALSO: il Decreto Ministeriale 30/12/2020 NON contiene in nessun punto un divieto alla delega. Anzi, non parla proprio di delega. Probabilmente, l’assunto sopra deriva dal fatto che in una bozza pre approvazione (e abbiamo detto tutto) era contenuta la possibilità per il paziente di delegare il medico ad inviare il promemoria (non la ricetta). Da cui hanno inteso che “visto che non c’è la possibilità di delegare, allora è vietato”.
Se state leggendo fino a qui avete capita come funziona il Diritto italiano, per cui nel Decreto non è contenuto alcun divieto in tal senso, ergo è possibile per il Cittadino italiano delegare chicchessia, salumiere, tabaccaio o Medico ad inviare un documento in sua vece.
Ma andiamo oltre: ammettiamo che dal Decreto si possa desumere un divieto. E’ stato chiesto al Ministero un chiarimento circa l’applicazione del Decreto alle ricette galeniche. Ebbene, il Ministero della Salute risponde così:
Infine, in merito alle preparazioni galeniche, il Dicastero ha chiarito che la dematerializzazione delle ricette per la prescrizione di farmaci non a carico del SSN non si applica ai medicinali preparati in farmacia e, quindi, privi di AIC.
Circolare 12799 del 08.02.2021
Il Farmacista non può sapere se il Medico ha inviato la stessa ricetta ad altre farmacie
E’ un falso problema. Perché? Perché la stessa cosa avviene ogni giorno con le ricette non ripetibili cartacee: ogni volta che il Farmacista spedisce una ricetta non ripetibile (sia essa galenica o industriale, di stupefacente o meno), non ha idea se quel paziente ha già ritirato un’altra ricetta identica in un’altra farmacia (o se andrà a ritirarla).
In altre parole, nulla vieta al Medico (neppure nello stupefacente in sez. B) di fornire ad un paziente 2 o più originali identici della stessa ricetta: sono tutte ricette valide. Magari perché una viene ritirata dal paziente e la seconda è “di scorta”, da utilizzare solo in caso di (es.) necessità.
Idem per la ricetta digitale: il Medico può legittimamente, d’accordo con il paziente, inviare la stessa ricetta a farmacie diverse affinché, (es. altro esempio) non essendo disponibile abbastanza materia prima, una parte di farmaco è acquistata nella farmacia A e la restante parte nella farmacia B: poichè la ricetta è non ripetibile e va trattenuta in Farmacia, servono due ricette identiche e il Farmacista della Farmacia A non saprà (ne gli interessa sapere, nè deve sapere) se esiste una Farmacia B.
Il DM 30 Dicembre 2020 ha legiferato sulla dematerializzazione delle ricette bianche, quindi non ci sono alternative
Il DM 30 dicembre ha legiferato sulla dematerializzazione delle ricette bianche dei farmaci industriali dotati di AIC. Solo quelle.
E come dice il Ministero, sono escluse dall’applicazione del Decreto le prescrizioni di farmaci galenici:
Infine, in merito alle preparazioni galeniche, il Dicastero ha chiarito che la dematerializzazione delle ricette per la prescrizione di farmaci non a carico del SSN non si applica ai medicinali preparati in farmacia e, quindi, privi di AIC.
Circolare FOFI 202100001544/AG del 08.02.2021
Modalità di invio di una ricetta galenica elettronica
Ci sono tanti modi nella testa di chi legge, per intendere “inviare una ricetta galenica elettronica”. Vediamoli tutti (o quasi) e quali sono legittimi.
Invio scansione della ricetta galenica all’email/Whatsapp della Farmacia
Questa è la prima modalità che, per semplicità e immediatezza, viene in mente ai pazienti.
Non ha alcuna validità giuridica, quindi non è legale. Una ricetta inviata via email semplice (non PEC) o Whatsapp è una “copia”; inoltre non ha firma originale (come prevede il R. D. del 1934) ed è quindi priva di alcun valore legale.
Comodo, rapido, ma inutile quindi dimenticatelo.

Invio della scansione della ricetta galenica via PEC della Farmacia
Questa è la seconda alternativa, vedendo nella PEC la via per dare legittimità alla ricetta.
Si intende inviata da un indirizzo PEC (del paziente o del Medico) all’indirizzo PEC della Farmacia.
Ma anche qui, la ricetta via PEC non ha alcuna validità: la PEC certifica il contenuto del testo nel corpo dell’email (come spiegato bene da questo articolo) e non dà alcun valore all’allegato (la ricetta galenica digitale) che, inoltre, è sempre un “copia” della ricetta priva di alcun valore giuridico, in quanto non ha firma in originale (come prevede il R. D. del 1934) o digitale.
La PEC da sola non è in grado di dare validità ad un documento privo di firma digitale.
Invio della scansione della ricetta galenica via PEC della Farmacia e con firma digitale
Si tratta di avere foto/PDF/altro formato della ricetta galenica (quindi un file informatico) su cui il Medico prescrittore (e solo lui) appone la sua firma digitale (non firma elettronica, lo ripetiamo ancora!).
Ci sono dubbi che il documento (ricetta galenica elettronica) abbia validità legale oppure no? No, non ci sono. Perché?
Ricopio quanto spiegato a inizio articolo (i link per approfondire sono indicati in precedenza):
nell’ordinamento giuridico italiano, la firma digitale a crittografia asimmetrica è riconosciuta ed equiparata a tutti gli effetti di legge alla firma autografa su carta.
https://www.arpae.it/dettaglio_generale.asp?id=1577&idlivello=1217
In questo scenario abbiamo quindi una ricetta galenica elettronica firmata digitalmente che ha valore, soddisfando in pieno i requisiti della normativa (lato del Medico prescrittore).
Ma il “bello” viene adesso.
Invio da parte del paziente della ricetta bianca elettronica (con firma digitale) via PEC
NON È VALIDO.
Lo scenario, lo esplicitiamo per completa chiarezza, è quella del Medico che invia con la propria PEC la ricetta galenica elettronica firmata digitalmente alla PEC del paziente il quale, a sua volta, la invia alla Farmacia che vuole.
Il Problema? Che il paziente può inviare la ricetta galenica elettronica a 2, 3, 10, 100 Farmacie diverse senza che una Farmacia sappia che anche altre abbiano avuto la stessa.
Esempio: se fosse una ricetta galenica elettronica di cannabis terapeutica (quindi non ripetibile, utilizzabile per una sopra preparazione), un paziente potrebbe inviarla a 10 Farmacie diverse ottenendo 10 preparazioni, quando per Legge ne avrebbe potuto ottenere solo 1.
Di conseguenza, questa modalità non consente di rispettare tutta la normativa vigente. Non è possibile percorrerla.
Invio da parte del Medico della ricetta bianca elettronica (con firma digitale) via PEC alla Farmacia
È VALIDO*
Versione breve: è l’unica modalità di tutte quelle esaminate che ha valore legale, purché sia sempre e solo il paziente a decidere la Farmacia cui deve essere inviata la ricetta galenica elettronica.
* Versione lunga: in questo scenario il Medico, come nel caso precedente, redige la ricetta galenica elettronica, firma digitalmente il file e lo invia direttamente ad una Farmacia scelta dal paziente. In questo modo, solo UNA Farmacia riceve UNA copia della ricetta medica. Se il Medico inviasse la stessa ricetta a Farmacie diverse, essendo lui il Medico prescrittore, equivarrebbe ad emettere la stessa ricetta più volte (cosa che può avvenire con il cartaceo).
A questo punto rimane la questione più spinosa nel mondo Farmacia, ossia la libera scelta del paziente della Farmacia.
È riconosciuto ad ogni cittadino, anche se assistito in regime mutualistico, il diritto di libera scelta della farmacia
Art. 15 della Legge 475/1968
Inoltre, il Codice Deontologico del Farmacista (versione 2018) recita che
Al farmacista è vietato porre in essere iniziative o comportamenti che limitino o impediscano il diritto di libera scelta della farmacia da parte dei cittadini.
Art. 14 “Libera scelta della farmacia” del Codice Deontologico del Farmacista
Come si può rispettare tutto questo senza incappare, addirittura, nell’accusa di comparaggio?
Con una dichiarazione scritta che il Paziente rilascia al Medico sulla volontà di volersi servire di una specifica Farmacia e che, sempre il Paziente, chiede al Medico di inviare la PEC a quella specifica Farmacia.
Tali dichiarazioni sono le stesse richieste da tutte quelle società di ritiro ricette o consegna farmaci per conto del paziente, cui il Paziente richiede per iscritto da quale Medico andare a ritirare le ricette e in quale Farmacia portare tali ricette per essere spedite.
È assolutamente consigliato, ma non obbligatorio, che il Medico dichiari, nel corpo della email PEC, che ha ottenuto il consenso all’invio della ricetta galenica elettronica alla Farmacia. In questo modo il Farmacista ha la massima tranquillità che il Medico non si è “dimenticato” di raccogliere il consenso.
Della liceità della cosa è anche l’Avv. Paolo Leopardi (che, certamente per lapsus, dimentica che già sono state dematerializzate le ricette stupefacenti in fascia A ossia a carico del SSN) che espone quanto segue:
Ci sono casi di ispezioni da parte di AUSL, NAS in cui tale modalità viene accettata?
Eccome, assolutamente sì: la normativa è questa.
Certamente esisteranno realtà in cui l’unica soluzioni, potrebbe essere arrivare al CdS.
Questo è tutto. Data la perniciosità dell’articolo, vale la pena citare ancora il disclaimer e invitarvi a scrivere nei commenti per ogni dubbio, domanda, ecc…
Ci sono software già predisposti per questa possibilità?
Si, in Italia esiste un software chiamato Synthesis, che permette al medico di redigere una ricetta medica di un galenico (di qualsiasi tipo, da soluzioni di minoxidil alla cannabis terapeutica), inviare la ricetta digitale nel cloud e, al Farmacista, di recuperarla e avviare la produzione del galenico.
DISCLAIMER: le informazioni contenute in questo articolo sono da ritenersi come meri ragionamenti teorici e spunti legislativi su cui riflettere. L’iniziativa di mettere in pratica quanto esposto è personale

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Ricetta galenica elettronica via PEC: si può, ma… sembra essere il primo su Farmagalenica.
]]>L'articolo Preparare olio di cannabis standardizzato, farmaco galenico sembra essere il primo su Farmagalenica.
]]>La cannabis medica o cannabis terapeutica è legale in Italia dal 2013 e da allora, viene prescritta da alcuni Medici e venduta in alcune Farmacie in varie forme farmaceutiche:
- cartine per decozione in tisana
- cartine per vaporizzazione mediante vaporizzatori
- capsule apribili per decozione in tisana di cannabis micronizzata
capsule decarbossilate ad uso orale - estratto in olio di oliva di cannabis (Cannabis Olive Oil)
- tinture
- estratti in alcool etilico di cannabis: resina (Rick Simpson’s Oil o FECO)
- estratti glicolici/glicerici
- estratti per sigarette elettroniche (eCig)
- cannabis in gel transdermico (PLO)
- cannabis in crema
- pillole al cacao (“cioccolatini”) alla cannabis
La forma farmaceutica probabilmente più prescritta e gradita ai pazienti/Medici è l’olio di cannabis terapeutica
Caratteristica intrinseca dell’olio di cannabis terapeutico preparato in Farmacia è la sua variabilità nella concentrazione di THC e CBD e le ripercussioni negative che questo può avere sul risultato terapeutico (come dimostrano diversi studi scientifici come questo e questo) le cui motivazioni verranno discusse tra poco.
Farmagalenica ospita oggi questa intervista del Dr. Marco Ternelli, “inventore” di una nuova metodica per preparare olio di cannabis standardizzato galenico in Farmacia, ossia
un olio la cui concentrazione in THC o CBD è sempre fissa ad ogni produzione, indipendentemente dalla concentrazione del fiore utilizzato.
Buongiorno Dottore, come e quando è nato l’olio di cannabis in farmacia?
Nei primi mesi del 2014.
Al tempo, eravamo poche decine di Farmacie in tutta Italia a preparare cannabis medica, e si realizzavano solo cartine/bustine per decotto (tisana alla cannabis) o vaporizzazione.
Dopo un anno che preparavo cannabis terapeutica, mi resi conti dei limiti enormi che aveva questa forma farmaceutica:
- decotto: prescritta ai dosaggi “omeopatici” (30-50-90 mg) non funzionava (i dettagli qui)
- vaporizzazione: in teoria, la miglior via di somministrazione. In pratica, non accettata dalla quasi totalità dei pazienti per “background culturale” e per il costo aggiuntivo del vaporizzatore.
Fu così che cercando, mi imbattei in un documento da poco pubblicato, di un certo Luigi Romano e Arno Hazekamp  che dava le prime indicazioni su come realizzare un olio di cannabis. Cominciai a far circolare e spiegare cone esempi come compilare le ricette mediche di marijuana terapeutica, in collaborazione con ACEF (all’epoca l’unico fornitore autorizzato alla distribuzione di cannabis flos) che diffuse questa conoscenza per l’Italia.
che dava le prime indicazioni su come realizzare un olio di cannabis. Cominciai a far circolare e spiegare cone esempi come compilare le ricette mediche di marijuana terapeutica, in collaborazione con ACEF (all’epoca l’unico fornitore autorizzato alla distribuzione di cannabis flos) che diffuse questa conoscenza per l’Italia.
Successivamente diversi ricercatori italiani e non, hanno sviluppato metodiche diverse sulla preparazione di olio di cannabis, più che altro per dimostrare metodiche di analisi o composizione in terpeni: la cosa che le accomuna (ed è il perché siamo qui oggi) è che non si considera la concentrazione finale di THC o CBD a priori, ma la si va a determinare a preparazione ultimata, ergo quel che c’è, c’è.
In pratica, il Medico non sa mai a priori (quando prescrive il farmaco) quale sarà la concentrazione di THC o CBD nell’olio, aspetta che il Farmacista faccia la titolazione dell’olio e fornisca questo risultato, ogni volta diverso e, in base a quello, ricalcoli la posologia per il paziente.
Quindi fino a oggi l’olio di cannabis nelle Farmaci eNON è standardizzato?
Quando si acquista un olio di cannabis in farmacia, si acquista un farmaco che il Farmacista galenista ha preparato utilizzando (nel 99% dei casi) le seguenti materie prime:
- fiori (infiorescenze) di cannabis farmaceutica
- olio di oliva
Ogni Farmacia o meglio ogni farmacista, in base alla metodica utilizzata (fai secondo arte o indicata dal medico in ricetta) otterrà un olio di cannabis con certe caratteristiche, in particolare con una certa concentrazione di THC, THCA, CBD, CBDA e CBN (i principali cannabinoidi di interesse terapeutico).
A questo, si aggiunge un fatto importante: la variabilità di concentrazione nel fiore di cannabis. Si, perché da una parte un fiore è standardizzato d un certo valore di THC o CBD (es. il Bedrocan è 22% THC, il Bedrolite 9% CBD), ma dall’altro, variazioni da lotto a lotto sono sempre presenti.
Ad es. il Bedrocan può essere 18% una volta e 24% l’altra. Il Bedrolite 7.9% oppure 8.5% e così via.
Unendo tutte queste variabili (fiore + metodiche + capacità/conoscenza del Farmacista) si ottiene, di fatto, un olio di cannabis con concentrazione sempre diversa da lotto a lotto (e da Farmacia a Farmacia).
In pratica, tutte le metodiche finora adottate in Farmacia (qui l’elenco) per preparare olio di cannabis, partono da un assunto di base:
- prendere una certa quantità di fiori e solvente (es. olio di oliva)
- miscelare con una certa metodica
- analizzare il risultato mediante titolazione HPLC o GC
- comunicare la concentrazione di THC e CBD al Medico/Paziente

Perché ha deciso di sviluppare una ulteriore metodica?
Ho sempre avuto passione per la Galenica, sempre: per me il Farmacista è Galenica. Punto.
Con la cannabis terapeutica ho avuto modo di poter realizzare e creare qualcosa di nuovo dal punto di vista “galenico-tecnologico”. Dal 2013 ho avuto modo di sviluppare, proporre (a volte insegnare) ai colleghi italiani diverse forme farmaceutiche della cannabis terapeutica galenica, creando o collaborando a creare (alcune ancora disponibili su Preparazionigaleniche.it):
- capsule di cannabis micronizzata per tisana
- capsule di cannabis micronizzata per uso orale
- olio di cannabis con metodica R&H e altre varie metodiche
- metodica SIFAP
Di fatto, col passare del tempo, mi sono reso conto che le metodiche utilizzate in Farmacia finora avevano tutte lo stesso problema: principalmente una elevata variabilità di contenuto in THC e CBD, ma anche una elevata perdita in terpeni a causa delle alte (eccessive) temperature di lavorazione. Queste variabilità richiedono un ricalcolo da parte del medico/paziente, il che può portare (come indicano gli Autori degli studi citati a inizio articolo) a
- errori di dosaggio
- errori terapeutici
- confusione nel paziente (ad es. come gli si spiega che, in base alla metodica, 8 gocce di olio possono contenere molto più THC o CBD di 20 gocce?)
Oltre a questo però, c’era la necessità di trovare un olio che contenesse tutto il profilo cannabinoidico (non solo THC, ma anche THCA; non solo CBD, ma anche CBDA) oltre che a più terpeni possibile e che avesse il minor numero di metaboliti di degradazione che si generano durante le fasi di riscaldamento.
L’olio di cannabis standardizzato galenico NON è un “estratto raffinato di THC”, ma un farmaco che contiene quante più sostanze possibile della cannabis.
Da qui lo sviluppo della metodica Ternelli (nome non definitivo ad oggi) per preparare olio di cannabis standardizzato galenico.

Quali sono le concentrazioni di un olio di cannabis standardizzato in Farmacia?
Le concentrazioni di un olio di cannabis standardizzato, potenzialmente potrebbero essere qualsiasi: si tratta di definire un certo valore X di THC o CBD (o altro cannabinoide) e fare in modo che ad ogni produzione nel Laboratorio Galenico, si ottenga sempre quel valore X.
Qui però si parla di un farmaco, qualcosa che i Medici e i pazienti dovranno conoscere univocamente e che bisognerà far conoscere; considerando
- la mia personale esperienza di oltre 6 anni di preparazione olio di cannabis
- gli studi scientifici disponibili sui cannabinoidi neutri e acidi
- la prassi medica
- la variazione massime e minime delle concentrazioni di THC e CBD nei fiori di cannabis farmaceutica
- semplicità nel ricordare una concentrazione e effettuare calcoli matematici precisi
- il voler fornire un farmaco scalabile finemente e quindi facilmente personalizzabile
- l’esperienza olandese in cui ho appreso di come alcune Farmacie già producessero olio di cannabis standardizzato
ho individuato e proposta nella metodica i seguenti valori “standard”, sempre riproducibili, anche nel caso di basso titolo di cannabinoidi nel fiore:
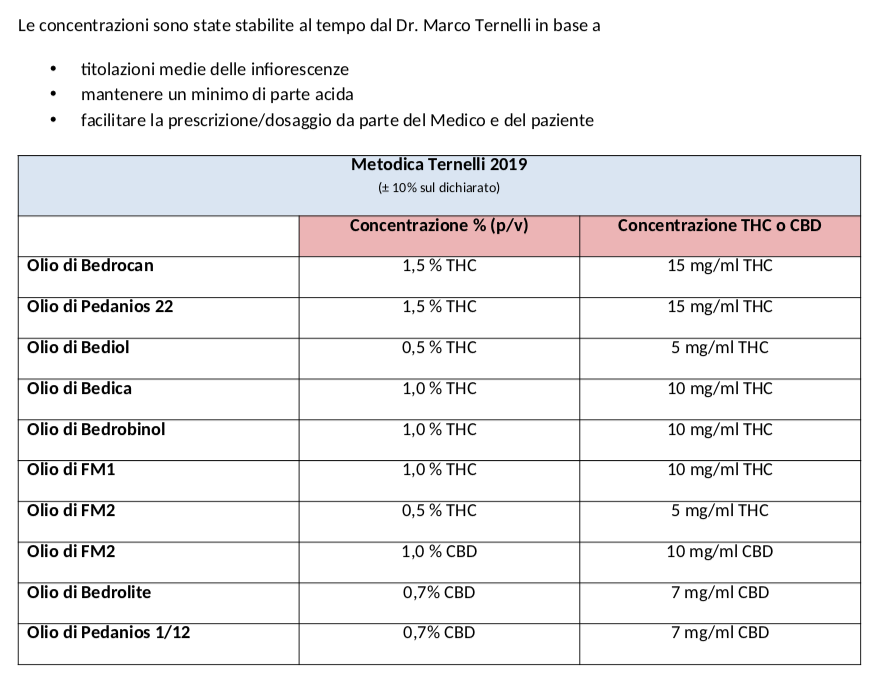
Qualche esempio.
Un olio di Bedrocan o Pedanios con metodica Ternelli conterrà sempre l’1.5% di THC cioè 15 mg/ml con una variazione media possibile tra i 14 e i 16 mg/ml.
Un olio di Bedica o Bedrobinol o Bedica con metodica Ternelli conterrà sempre l’1.0% di THC cioè 10 mg/ml con una variazione media possibile tra i 9 e i 11 mg/ml.
Cambierà qualcosa nel come una ricetta di cannabis andrà redatta?
No, parte del lavoro di elaborazione dei dati comprende anche una valutazione dal punto legislativo per trovare il modo più corretto per il medico di richiedere una preparazione olio di cannabis standardizzato galenico al Farmacista.
Premetto innanzitutto che il Medico potrà, ovviamente, prescrivere un olio di cannabis con qualsiasi altra metodica voglia.
Di fatto, nella metodica Ternelli per l’ olio cannabis standardizzato galenico, il rapporto tra i grammi di cannabis flos e millilitri di olio di oliva è rimasto identico a quello che i Medici prescrivono dal 2014 a oggi cioè 1 : 10 (esempio 5 grammi di cannabis in 50 ml di olio di oliva).
Sarà però necessario per il Medico indicare in ricetta la concentrazione esatta di THC o CBD che vuole ottenere nell’olio finale (es. 0,5% o 5 mg/ml) q. b. (quanto basta) a 50 millilitri.
Quali i vantaggi e svantaggi di un olio di cannabis standardizzato?
Di seguito le caratteristiche positive e negative relative ad un olio alla metodica Ternelli 2020.
Vantaggi
Contenuto stabile di cannabinoidi = riproducibilità terapeutica
È il senso dell’articolo: un farmaco galenico standard, esattamente come qualsiasi altro farmaco galenico. Se il medico chiede capsule da 24 mg di furosemide (un diuretico), il Farmacista Galenista prepara 24 mg per capsula, non fa (esempio) capsule da 12mg, comunica il dosaggio al medico e questi raddoppia il numero di capsule per ottenere il dosaggio desiderato.
Se il medico chiede 1% di THC nell’olio, perché il Farmacista Galenista non dovrebbe fare altrettanto?
Maggior presenza di terpeni
Buona palatabilità / sapore
Per le basse temperature a cui avvengono i processi di lavorazione dell’olio di cannabis standardizzato, l’olio non ha sapore di cotto o bruciato o tostato o acido, ma “sa di cannabis”.
Anche questo significa maggiore compliance da parte del paziente.
Miglior stabilità
All’olio formulato con questa metodica sono state assegnate 2 scadenze diverse, per un massimo di 6 mesi durante i quali la concentrazione dei cannabinoidi non decade.
Ovviamente sono necessari accorgimenti tecnici che saranno descritti nella metodica.
Facilità d’uso
Avendo un olio che ha sempre la stessa concentrazione di THC e CBD, diviene più facile per il paziente ricordarsi le gocce che deve assumere senza alcun cambiamento nella posologia o ricalcolo del dosaggio quando acquista un nuovo flacone.
Riduzione di errori di somministrazione e ADR
Si può associare univocamente il contenuto di THC o CBD ad una certa quantità di olio (es. gocce o millilitri): il Medico sarà agevolato nel calcolare i dosaggi (potendo imparare a memoria i dosaggi standard e sapendo saranno sempre quelli), mentre il paziente non si confonderà nel dover assumere gocce diverse per mantenere sempre lo stesso dosaggio di THC o CBD.
Presenza di cannabinoidi acidi = full spectrum
Svantaggi
Tempi lunghi di realizzazione
Mentre le altre metodiche hanno una durata massima di 2 o 3 ore per la realizzazione, la metodica Ternelli richiede minino 48 ore (2 giorni). Ma ne vale la pena. 
Strumentazione complesse e costose
Dimenticate i 300€ dell’agitatore elettromagnetico. Per tutta l’attrezzatura necessaria per la metodica si parla di un importo minimo variabile da 30.000 a 50.000€ (stima).
Quantitativo minimo in volume da preparare
Posto che teoricamente la metodica può essere applicata a qualsiasi volume, anche minimo (es. 50 ml), per le macchine utilizzate, la resa e il tipo di lavorazione, la metodica è applicabile quando il Farmacista deve preparare almeno 250 – 300 ml di olio di cannabis standardizzato galenico.
In caso di errori, può essere impossibile standardizzare una certa preparazione galenica
Poiché il Farmacista non può utilizzare liberamente la quantità cannabis che vuole, diciamo che “non può permettersi di sbagliare”, specie quando deve ottenere alte concentrazione di un cannabinoide. Se nel seguire la metodica sbaglia qualche passaggio importante, è chiaro che probabilmente non riuscirà ad arrivare al valore standardizzato. In quel caso? O considera non vendibile il preparato o lo destinerà ad altri.
Ci può dire cosa serve per realizzare la metodica Ternelli per preparare olio di cannabis standardizzato galenico?
Purtroppo non mi è possibile ancora fornire informazioni complete su come realizzare la metodica, sia perché ancora in fase di elaborazione e pubblicazione, sia per potenziali brevetti in alcuni passaggi. In futuro, sarà certamente possibile.
Volendo però dare un’idea indicativa della strumentazione assolutamente necessaria da avere in Farmacia, posso citare (non esaustivamente):
- HPLC
- sonicatore ad ultrasuoni (non un bagno ad ultrasuoni)
- rotavapor (evaporatore rotante)
- agitatore ad asta
- forno digitale
- pompa da vuoto
In questo modo, non sarebbero poche le farmacie in grado di realizzare questo olio di cannabis standardizzato galenico?
Si o comunque un numero inferiore a quello di adesso.
Partiamo dagli studi scientifici che ho citato in precedenza: sollevano un problema strutturale della galenica, ossia l’individualità e variabilità del Farmacista nel fare una preparazione con metodiche “classiche”.
Attorno alla Galenica in farmacia si è sempre sviluppato il motto “tutti possono fare tutto, sempre e comunque”, quando poi nella realtà non è così. Tutti possono tutto = frammentazione e abbassamento della qualità, e l’olio di cannabis ne è la prova lampante (ma non l’unica).
In Galenica, tutti possono fare tutto? No, anche se a molti piace ancora pensarlo.
Permettetemi un esempio per rendere l’idea, vale a dire i colliri/iniettabili realizzati in farmacia: tu Farmacista vuoi fare farmaci sterili?
Servono spazi, una camera bianca (quindi investimenti), personale qualificato e conoscenze.
Però potremmo anche ragionare in maniera diversa e decidere di rimuovere questi limiti per consentire a tutte le farmacie di preparare colliri, anche chi non ha spazi, chi non ha struttura disponibile. Calerebbe la qualità (= colliri non sterili), ma avremmo più farmacie che possono “fare” colliri.
Credo sia palese che il secondo modo di pensare sia un disastro e infatti, per fortuna, non è così.
Inoltre, ripeto che un Medico potrà sempre indicare altre metodiche o lasciare libertà assoluta al Farmacista indicando f. s. a. in ricetta.

Alcuni dicono che un olio cannabis standardizzato non sia davvero realizzabile in Farmacia
Sicuramente c’è chi criticherà, ma la vita è troppo breve, intensa e bella per preoccuparsi di quel che pensano gli altri, specie se dicono che l’uva è acerba.
L’importante è fare bene e fare del bene, con passione e divertendosi nel proprio lavoro.
Gli oli standardizzati in Farmacia come galenico sono già preparati in Olanda da anni (fu là che ne sentii parlare per la prima volta). È tempo che vengano sviluppati anche nelle Farmacie italiane.
E, pensiero finale, non è che la metodica Ternelli sia l’unico modo di ottenere un olio di cannabis galenico standardizzato, ma di fatto è la prima proposta e risposta concreta a un problema ormai presente da tempo.
Chi dice che è impossibile non dovrebbe disturbare chi ce la sta facendo.
Elbert Hubbard (?), certamente non Albert Einstein

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Preparare olio di cannabis standardizzato, farmaco galenico sembra essere il primo su Farmagalenica.
]]>L'articolo Cosmetici alla canapa in Europa e Italia, normativa e spunti sembra essere il primo su Farmagalenica.
]]>- cannabis
- canapa
- estratti di canapa
- cosmetici CBD
- oli essenziali di canapa
e così via.
Lo scenario classico è l’agricoltore che ha un campo di canapa e vuole venderla (o vendere un semilavorato ottenuto dalla sua coltivazione) ad un laboratorio cosmetico affinché ne faccia cosmetici alla canapa.
Esattamente come nell’uso della canapa/cannabis nel consumo umano in cui vige una grande confusione, anche per l’uso della canapa nei cosmetici ci troviamo nella stessa situazione, specialmente su cosa è lecito e cosa non lo è.
In questo articolo, faremo chiarezza su quali parti e derivati della cannabis/canapa possono essere utilizzati per preparare un cosmetico (creme, shampo, sapono, sieri, ecc…).
Nota: da Febbraio 2021 la normativa è cambiata drasticamente rispetto a prima, l’articolo è stato perciò diviso in 2 parti (prima e dopo). Per le vicende del CBD “stupefacente” del “Decreto Speranza”, si rimanda all’articolo dedicato.
Cannabis e canapa
Prima di procedere e per scongiurare incomprensioni ulteriori, serve un minimo di chiarimento sui termini usati, vale a dire
- cannabis sativa L.: è il nome botanico latino e scientifico della pianta, indipendentemente che sia uso ludico, medico, tecnico, alimentare, industriale che sia. In questo articolo, però, il termine cannabis lo si userà per riferirsi alla cannabis stupefacente (con THC).
- canapa: conosciuta anche come HEMP, è il termine con il quale ci si riferisce a Cannabis Sativa L. con contenuto di THC < 0,2% nel fiore e quindi non è considerata stupefacente. La canapa legale è destinata all’uso industriale, tecnico, alimentare, tessile, cosmetico ecc… Il limite di THC nelle infiorescenze (nei fiori) è tollerato fino allo 0.6% nelle analisi eseguite sulla coltivazione.
Ulteriori approfondimenti sono in questo articolo dedicato sulla canapa ad uso umano, in cui si spiegano ancora meglio e più dettagliatamente le differenze.

Cannabis nei cosmetici: (breve) iter di produzione e legislazione
Non vogliamo annoiarvi, ma anche questo è un passaggio obbligatorio da conoscere per capire (tra poco) perché SI alcune cose e perché NO altre quando si parla di cannabis nei cosmetici.
Quando si vuole creare e immettere in commercio un cosmetico (qualsiasi, non necessariamente con cannabis) l’iter in estrema sintesi è:
- avere un laboratorio cosmetico idoneo
- creare la formula
- effettuare i test obbligatori sulla stabilità del prodotto
- redazione del PIF (Product Information File)
- comunicazione telematica al CPNP (Cosmetic Product Notification Portal)
- cominciare a commercializzare il prodotto
L’ultimo punto vuol dire che una volta inviato (elettronicamente) la comunicazione al CPNP, dopo appena mezz’ora è possibile commercializzare il prodotto cosmetico.
È nel punto 2 che avviene la scelta e utilizzo delle sostanze e materie prime, tra cui (volendo) canapa e derivati.
La normativa Europea dei cosmetici, valida anche per l’Italia è il Regolamento CE 1223/2009
Controlli sui cosmetici alla canapa e non solo
Seguita la procedura di cui sopra, le domande che sorgono sono:
- chi garantisce a priori che la composizione del cosmetico venduta sia effettivamente quella registrata?
- chi garantisce a priori che le sostanze usate nei cosmetici alla canapa siano certificate ad uso cosmetico (eh si, serve quello)?
- chi garantisce a priori che non ci sia THC nel cosmetico alla canapa?
Queste domande hanno una risposta divisa in 2 parti:
- nessuna forza dell’ordine/sanitaria controlla a priori! Tutti i controlli sui cosmetici sono demandati a posteriori mediante controlli a campione sul prodotto già in vendita o dopo segnalazione di reazione avversa da parte del consumatore
- il fabbricante è responsabile dei dati dichiarati, qualità delle materie prime usate, corrispondenza al certificato di analisi, ecc…
Fatta questa introduzione (speriamo utile), andiamo al nocciolo.

Quali sono le parti e derivati della canapa utilizzabili LEGALMENTE nei cosmetici alla canapa?
Versione breve
Sono le seguenti:
- CBD sintetico
- [da febbraio 2021] CBD naturale (da estratti, tinture o resine)
- estratti da foglie
- estratti ottenuti da semi di canapa
- olio ottenuto da semi di canapa
- steli polverizzati
NON sono utilizzabili nei cosmetici alla canapa:
- oli essenziali
- tutti gli estratti/resine/tinture ottenuti da infiorescenze/gemme
- parti dirette di foglie o stemmi
Coraggio, continuate a leggere per capire come e perché 
Versione lunga (con dettagli)
Tutte le sostanze utilizzabili nei cosmetici in Europa sono contenute in un grande database chiamato COSING (Cosmetic Ingredient Database) che è composto da
- Regolamento Cosmetico Regulation (EC) No 1223/2009 del Parlamento e del Consiglio Europeo
- Direttiva 76/768/EEC (Direttiva cosmetica) e successive modifiche
- Elenco degli Ingredienti Cosmetici modificato dalla Decisione 2006/257/EC che stabilisce una nomenclatura comune di tutti gli ingredienti cosmetici, da indicare sulle etichette dei cosmetici venduti in Europa
- opinioni sulle sostanze cosmetiche da parte del Scientific Committee for Consumer Safety (elenco delle opinioni del SCCS).
Per quanto riguarda la canapa (hemp), in questo database Europeo e quindi valido per qualsiasi cosmetici alla canapa, sono riportate 17 20 40 diverse registrazioni alla data del presente articolo (Febbraio 2021), in particolare le seguenti (nome INCI):
- CANNABIDIOL (cannabidiolo)
- CANNABIS SATIVA SEED OIL (olio di semi di canapa)
- CANNABIS SATIVA SEED EXTRACT (estratto dai semi di canapa)
Cannabis Sativa Seed Oil
Il più semplice, l’olio di seme o olio di canapa, inteso come l’olio ottenuto dalla spremitura del seme.
Avete presente i cosmetici all’olio di oliva o con l’olio di mandorle dolci o olio di enotera? Ecco, stessa cosa, cosmetici con l’olio di canapa. Niente CBD (se non tracce irrilevanti), niente cannabinoidi, …
Posto che si utilizza anche a livello alimentare, a livello cosmetico, l’olio di semi di canapa ha proprietà
- emollienti
- protettive per la pelle
Volete saperne di più sull’olio di canapa? Leggete l’articolo dedicato.
Cannabis Sativa Seed Extract
Anche qui, parliamo di qualcosa di noto: estratti derivanti dal seme di canapa.
Il seme di canapa ufficialmente non contiene THC (se non tracce per contaminazione) e ha bassissimi livelli di CBD.
A livello cosmetico si utilizza ufficialmente come emolliente.
Cannabidiol (CBD)

È la richiesta che va per la maggiore, la “crema al CBD” o “il siero alla cannabis con CBD”.
Situazione PRIMA di Febbraio 2021
Qui le cose si complicano, o meglio, è necessario spiegare bene. Difatti, nel Cosing il CBD viene descritto in 2 modi diversi:
- derived from extract or resin or tincture of cannabis (derivato da estratto o resina o tintura di cannabis)
- shyntetically produced (prodotto sinteticamente)
Per entrambi, poi, è presente un riferimento all’Annex II/306. Calma! 
Annex II/306
L’Annex II (annex secondo, non annex due) è quella parte del Regolamento sui cosmetici Europei relativo alle sostanze vietate. Il numero 306 riferito alla cannabis, indica (hahaha… “indica”… ) che la cannabis si trova nella posizione 306.
Il fatto che una sostanza sia presente nell’Annex II, significa che non può essere usata nella preparazione di un cosmetico.
1. CBD derivato da estratto o resina o tintura di cannabis
Questo è il CBD che nel 99,9% dei casi viene richiesto da chi vuole produrre un cosmetico alla cannabis: il CBD “naturale” perché ottenuto dalle infiorescenze di cannabis (che sono naturali, giusto?).
Ma, nelle annotazioni sul CBD, il Cosing riporta che (traduzione a cura dell’Autore):
il cannabidiolo come tale, indipendentemente dalla sua origine, non è contenuto nelle sostanze stupefacenti della Convenzione Unica sulle sostanze Narcotiche del 1961. Ad ogni modo, il suo uso deve essere vietato nei prodotti cosmetici (II/306) se preparato partendo da estratti o tinture o resine di cannabis, in accordo con la Convezione Unica.
Cosing
Tenere presente inoltre che la legislazione di ogni Stato Membro sulle sostanze stupefacenti che potrebbe applicarsi
Il che significa che il CBD sintetico in quanto tale può essere usato, mentre in forma di resine, tinture o estratti titolati in CBD (indipendentemente dal tenore di THC ovvero anche se < 0.2% o anche < 0.1%) NON può essere utilizzato nella produzione di cosmetici alla canapa.
2. CBD prodotto sinteticamente
Molti rabbrividiscono e storcono il naso alla parola “sintetico” associata alla cannabis, ritenendo che associando tale termine associato alla parola “cannabis” sia un reato! 
Di fatto, dal punto di vista chimico, il CBD sintetico è identico al CBD naturale, quel che cambia è “l’intorno”, ossia le altre sostanze presenti. Spieghiamo.
Immaginiamo un cristallo naturale di CBD ottenuto dalle infiorescenze di canapa, puro al 99.2% e un cristallo sintetico di CBD puro al 99.2%.
Significa che in entrambi casi il 99.2% è rappresentato dal CBD, chimicamente identico tra i 2. La differenza sta in quel 0,8%.
Nel caso del CBD naturale, lo 0,8% potrà essere composto da terpeni, altri cannabinoidi (anche THC, a tenore variabile), alcaloidi.
Nel caso del CBD sintetico, lo 0,8% saranno per lo più solventi residui e metaboliti secondari (anche THC, anche se in tracce).
Tutto ciò detto, anche per il CBD sintetico, il Cosing riporta la stessa frase citata sopra per il CBD naturale, ma in questo caso non si tratta né di resina, né di estratto, né di tintura.
Situazione DOPO Febbraio 2021
Sperando abbiate letto come era prima, le poche seguenti righe faranno capire rapidamente: il COSING è stato aggiornato ed è stata rimossa la limitazione dell’Annex II/306 sul CBD naturale ottenuto da estrazione (da fiori, foglie o altro).
Si può vedere dalla foto seguente come la colonna dell’Annex II/306 (il divieto) ora sia vuota.
Di conseguenza CBD sintetico o anche il CBD naturale può essere impiegato nella preparazione di cosmetici alla canapa. Tale possibilità è ancora possibile alla data di Febbraio 2024.
Cannabis nei cosmetici e THC: ci sono limiti?
Il THC (tetraidrocannabinolo) è una sostanza classificata come stupefacente e perseguita da leggi internazionali. La sua presenza nel FIORE è solitamente richiesta sia < 0.2%.
Ma per quanto detto dell’Annex II/306, tutte le materie prime ad uso cosmetico della cannabis nei cosmetici devono essere completamente prive di THC, che non deve essere presente neppure in tracce.
In pratica, un certificato di analisi di una materia prima ad uso cosmetico deve riportare ND (Not Detected).
A voi le considerazioni.
E gli oli essenziali? I terpeni? Le foglie? Le gemme?
A parte i terpeni e gli estratti da foglie (per un motivo che vedremo a breve), non si può usare nient’altro, in base alla normativa attuale sui cosmetici alla canapa.
Il motivo è presto detto:
- alcuni non sono riportati nel Cosing. E se non ci sono, NON si possono usare.
- altri derivati, sono ottenuti da estrazione da fiori e/o foglie, quindi inclusi nell’Annex II = divieto.
Perchè i terpeni si possono usare nei cosmetici alla cannabis?
Perché i terpeni NON sono costituenti unici della cannabis, ma a livello botanico sono presenti in tanti altri vegetali (es. agrumi, luppolo, ecc…) ossia si possono ottenere (estraendoli) da piante che nulla hanno a che vedere con la cannabis e le sue limitazioni.
E, ovviamente, queste sostanze sono riportate nel Cosing.
L’importante, è che siano sempre certificati ad uso cosmetico.
Riassunto finale sul cosa si può e non si può fare
Per evitare di ripetere cose già dette, proponiamo questa tabella riepilogativa su quali parti e derivati della canapa possono essere utilizzate per preparare cosmetici alla canapa.
| SI PUO’ USARE? | |
| CBD sintetico | SI |
| CBD naturale senza THC | SI |
| CBD naturale con tracce di THC | NO |
| CBG sintetico | SI |
| CBG naturale | SI |
| altri cannabinoidi sintetici (es. CBN) | SI |
| altri cannabinoidi naturali (es. CBN) | NO |
| infiorescenze o derivati da infiorescenze (estratti, tinture, …) | NO |
| steli e derivati degli steli | SI |
| semi e derivati (olio da seme, farina, ecc..) | SI |
| oli essenziali | NO |
| foglie (estratto senza THC) | SI |
| foglie (TUTTO il resto, esclusi estratti) | NO |
E ricordiamo che il nostro laboratorio cosmetico Farmacosmetica prepara e vende da tempo cosmetici alla canapa, secondo tutto quello spiegato in questo articolo.

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Cosmetici alla canapa in Europa e Italia, normativa e spunti sembra essere il primo su Farmagalenica.
]]>L'articolo Ricetta elettronica veterinaria galenica: istruzioni e stupefacenti sembra essere il primo su Farmagalenica.
]]>Si tratta della “morte” della ricetta veterinaria cartacea per come la conosciamo: niente più firma del medico, timbro, ricetta in triplice copia colorata (blu, rosa, gialla, ecc…). SOLO una ricetta online, identificata da un codice e un pin.
Ci sono state difficoltà iniziali su aspetti tecnici, legislativi, farmaceutici e pratici. In questo articolo vediamo di risolverli il più possibile, sia dalla parte del Medico Veterinario che del Farmacista… e perché no? Dal parte del proprietario dell’animale, che vedrà consegnarsi qualcosa di completamente diverso rispetto a quello cui era abituato prima.
In fondo alla pagina, infine, sono riportate le Domande più frequenti con Problemi & Soluzioni pratiche.
Perché è nata la ricetta elettronica veterinaria galenica?
Per contrastare l’antibiotico resistenza. Questa la prima e vera motivazione.
Di fatto, serve a dare una tracciabilità completa di dove è stato venduto il farmaco, a chi, quando, come, ecc… per evitare abusi prescrittivi, usi impropri ed illegali.
Normativa della ricetta elettronica veterinaria galenica (e non)
La ricetta elettronica veterinaria galenica segue la stessa legislazione della ricetta veterinaria non elettronica.
Le norme che regolano la ricetta elettronica veterinaria galenica sono
- Decreto Legislativo 193/2006
- Decreto Ministeriale 8 febbraio 2019 – Modalità applicative delle disposizioni in materia di tracciabilità dei medicinali veterinari e dei mangimi medicati pubblicato sulla G. U. 89 del 15 Aprile 2019
- Decreto Legislativo 5 agosto 2022, n. 136 pubblicato sulla G.U. del 12 settembre 2022.
Di fatto, significa che NON avranno più valore le ricette fatte “a mano” o su “carta intestata” dal Veterinario, ma solo quelle emesse attraverso un sistema informatico online al quale il Farmacista si collega per visualizzare la prescrizione.
Il Veterinario potrà compilare ed emettere la ricetta tramite:
- computer fisso o portatile
- tablet
- app per smartphone
e generare un “promemoria” da dare al proprietario dell’animale, cioè un foglio di carta senza alcun valore che però contiene i dati che il Farmacista utilizzerà per accedere al sistema online e recuperare la ricetta.
Per quali farmaci si utilizza la ricetta elettronica veterinaria galenica?
Fino al 27 settembre 2022, essa valeva per tutti i farmaci, ad eccezione dei farmaci stupefacenti , sia di origine industriale sia galenici (preparati dal Farmacista).
La REVG quindi si userà:
- per le ricette veterinarie ripetibili
- per le ricette veterinarie non ripetibili
- per le ricette veterinarie non ripetibili in triplice copia
- per le ricette veterinarie di approvvigionamento scorta personale o per impianto
Dal 27 settembre 2022 (incluso) la ricetta elettronica veterinaria galenica varrà per tutti i farmaci inclusi i farmaci stupefacenti industriali e galenici (sono esclusi solo quelli in sez. A, come morfina iniettabile o ketamina).
È quindi possibile prescrivere cannabis medica direttamente in REV senza bisogno di stampare nulla.
Dal 27 settembre 2022, con inclusione dei farmaci stupefacenti sez. B, C, D, E, una ricetta cartacea veterinaria datata nel 2019 NON avrà alcun valore.
Salvo malfunzionamento del sistema informatico
Serve la REV per gli stupefacenti (es. cannabis medica)?
SI!
Dopo il 27 settembre 2022
Il Decreto è chiarissimo nell’escluderli.
Se ciò non bastasse, con l’aggiornamento delle Tabelle della Farmacopea con il DM 18 Giugno 2020 è stato esplicitamente (ri)chiarito che
OBSOLETA da Settembre 2022: Tabelle 4 e 5 della FU XI Edizione Italiana
Non è ammessa la prescrizione di medicinali contenenti sostanze stupefacenti tramite REV.
In altre parole: per poter dispensare un farmaco o galenico stupefacente, basteranno il codice ricetta e il PIN (esattamente come tutti i farmaci non stupefacenti), senza più bisogno di avere copia cartacea timbrata e firmata dal Medico Veterinario.

Differenze tra la ricetta elettronica veterinaria galenica e non elettronica
Posto che la normativa e quindi i formalismi della ricetta elettronica veterinaria galenica sono gli stessi delle “vecchie” ricette, nulla cambia per durata della ricetta, modalità di compilazione, dati da indicare, ecc…
Anzichè indicarli a biro o su carta stampata al computer, saranno inseriti direttamente nel sistema centrale di Farmacosorveglianza.

Veterinario: come fare una ricetta elettronica veterinaria galenica
Di seguito i principali passaggi, per chi comincia da 0.
1. Registrarsi online come Veterinario e ottenere credenziali
Collegarsi al sito www.ricettaveterinariaelettronica.it, in particolare su www.ricettaveterinariaelettronica.it/richiesta-account.html portale del Ministero

Cliccare sull’icone blu indicata dalla freccia. Si aprirà una pagina come questa:
in cui il Veterinario dovrà compilare ed inserire tutti i dati richiesti, unitamente ad un documento di identità.
Dopo qualche giorno, quando tutte le verifiche del caso saranno state eseguite, il Veterinario riceverà user id e password via email.
2. Compilare ed emettere una ricetta veterinaria elettronica galenica
A questo punto, sarà necessario collegarsi al sito www.vetinfo.it
e cliccare su “Accedi all’Area Riservata”. Si aprirà la seguente pagina:

dove sarà necessario cliccare su “Farmacosorveglianza” (v. freccia rossa). A questo punto si proseguirà cliccando su “Menù”:
Verrà aperta una schermata simile a questa:
in cui il Veterinario dovrà selezionare tra:
- Nuova Ricetta per Prescrizione Veterinaria
- Nuova Ricetta per animali DPA con allevamento non censiti in BDN (Banca Dati Nazionale) e per Equidi DPA: si tratta in pratica, della vecchia Ricetta Non Ripetibile in Triplice Copia
- Nuova Ricetta per Prescrizione Veterinaria PET ed Equidi NDPA
A seconda della scelta, la finestra che si aprirà avrà contenuti diversi che, se indicati con un asterisco rosso, dovranno essere compilati obbligatoriamente pena l’impossibilità di continuare nel sito.
Dopo aver cliccato su “Inserisci”, la successiva schermata richiederà (importante!) di selezione “Galenico”dal menù “Tipologia”:
A quel punto si compila la prescrizione, in particolare il campo libero “” dove il veterinario deve riportare la richiesta del farmaco galenico veterinario, esattamente come si sarebbe fatto per la ricetta cartacea:
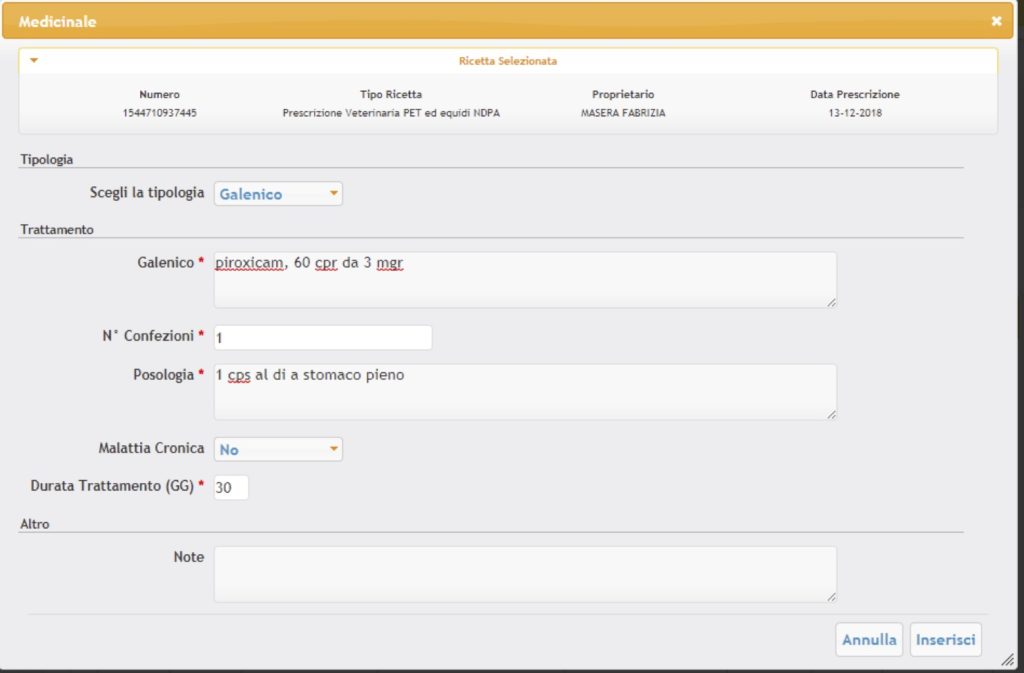
Cliccando su “Inserisci”, il Veterinario avrà creato la ricetta online.
Farmacista: come spedire una ricetta elettronica veterinaria galenica
Il Farmacista di fatto riceve la ricetta elettronica veterinaria (che vuol dire ALMENO il numero ricetta e pin) in uno dei seguenti modi:
- promemoria cartaceo consegnato a mano dal paziente
- numero e pin dettati a voce dal paziente
- foto su smartphone
- FAX
- email da parte del paziente
Sono TUTTI metodi validi per accedere alla ricetta medico veterinaria elettronica, che si ripete, avviene mediante:
- o numero ricetta e PIN
- o codice fiscale (del proprietario dell’animale) e PIN
Fatto questo, l’iter da che il Farmacista deve seguire per dispensare un farmaco galenico veterinario è
- compilare il foglio di lavoro in laboratorio
- loggarsi sul sito www.vetinfo.it
- effettuare la vendita sul portale
- effettuare la vendita al cliente sul gestionale della Farmacia
- (opzionale) allegare promemoria della ricetta elettronica al foglio di lavorazione; in alternativa, la stampa della stessa, dalla pagina del portale Vetinfo.
In futuro, i punti 2 e 3 non saranno più necessari, in quanto i gestionali saranno perfettamente in grado di integrarsi ed inviare automaticamente i dati al sistema online.
Caso molto particolare: lo sconfezionamento
Caso A: richiesta diretta di sconfezionamento da parte del Veterinario
Situazione: il veterinario vuole che il Farmacista prenda un farmaco industriale, uso umano o veterinario, (es. Norvasc® 5 mg compresse) e lo modifichi (es. ripartire la dose di 1/6).
Quante ricette deve fare?
Due? Una per il farmaco uso umano e una per la preparazione galenica?
Una? Una ricetta elettronica galenica veterinaria in cui il veterinario indichi il nome del farmaco uso umano e cosa farne?
La risposta giusta: UNA sola ricetta elettronica veterinaria galenica.
Dovrà compilare la ricetta impostandola come “Galenico”, indicando il nome del farmaco industriale (Norvasc® 5 mg compresse) e la preparazione galenica da farsi (es. dosaggio diverso, forma farmaceutica diversa, ecc…).
Per la tracciabilità, infatti, il farmaco industriale NON verrà dato al paziente affinché lo somministri all’animale, ma aperto e lavorato dal Farmacista per eseguire la preparazione galenica veterinaria.
Inoltre, la tracciabilità è comunque garantita, perché anche se il farmacista registra nella ricetta elettronica veterinaria solo i dati del farmaco galenico, nel foglio di lavorazione che rimane al Farmacista viene riportato obbligatoriamente il numero di lotto e scadenza
Caso B: richiesta di preparazione galenica con principio attivo
È il caso in cui il medico veterinario prescriva una preparazione galenica a base di un principio attivo (es. litio carbonato) in capsule per un gatto.
Nel caso in cui (SOLO in questo caso!!) per tale preparazione non esista la materia prima disponibile, il Farmacista per poter preparare tale farmaco galenico veterinario, dovrà sconfezionare il farmaco industriale che contiene tale principio attivo (es. CarboLithium® compresse).
Può farlo? O il Veterinario deve fare (avrebbe dovuto fare) una ricetta separata anche per il CarboLithium® compresse?
Si, può farlo. E no, il Veterinario non deve fare nessuna altra ricetta.
La Tariffa dei medicinali prevede che il Farmacista possa autonomamente (“qualora sia necessario“) sconfezionare il farmaco industriale per ottenere il principio attivo che serve.
Inoltre, la tracciabilità è comunque garantita, perché anche se il farmacista registra nella ricetta elettronica veterinaria solo i dati del farmaco galenico, nel foglio di lavorazione che rimane al Farmacista viene riportato obbligatoriamente il numero di lotto e scadenza.
Quando il Veterinario vuole far ripartire galenicamente un farmaco uso umano, NON è necessario emettere 2 ricette distinte

Vantaggi e svantaggi della ricetta elettronica veterinaria galenica
Vediamo insieme gioie (tante) e dolori (pochi) della nuova ricetta elettronica rispetto a quella “tradizionale” cartacea.
Vantaggi
- Veloce, compilabile via computer o smartphone o tablet
- Inviabile via email o Whatsapp al proprietario dell’animale
- Permette l’abilizione di moduli
- Evita errori formali, lapsus medici, formalismi assenti
- Evita falsificazioni o manipolazioni della ricetta
- Abolisce gli obblighi di invio alle AUSL, che avvengono invece automaticamente
- Permette tracciabilità del Farmaco veterinario galenico e non
Svantaggi
- Legata al funzionamento della piattaforma online
- Nessuna possibilità di “accomodare” la scadenza (alla mezzanotte del giorno dopo la scadenza, non c’è modo di utilizzarla)
- Se non si utilizza la ricetta elettronica veterinaria… “si è al di fuori del sistema”

Domande varie sulla ricetta elettronica veterinaria galenica
Certamente: sono valide in quanto emesse quando la normativa della ricetta elettronica veterinaria non era ancora in vigore. Ovviamente non sono presenti sul sistema elettronico, per cui vanno spedite dal Farmacista normalmente, apponenti timbro e prezzo praticato.
Dopo i primi mesi del 2019, tutte le vecchie ricette ripetibili veterinarie “vecchie” cesseranno di avere validità e rimarranno quindi solo le elettroniche.
La registrazione della vendita deve avvenire in tempo reale o comunque entro la giornata. In caso di malfunzionamento, va effettuata entro 24 ore dal ripristino del funzionamento: il farmacista, al momento della dispensazione, annota nome farmaco, AIC, numero confezioni dispensate, lotto e scadenza che inserirà poi in un momento/giorno successivo indicando come data di dispensazione il giorno in cui il sistema non ha funzionato.
Nota: il farmacista può accedere manualmente al sito www.vetinfo.it.
PRIMA deve provare ad accedere con i 2 siti sopra indicati.
POI dovrebbe provare con la APP da smartphone/tablet (si, è sistema ancora diverso a indipendente dai siti web)
INFINE, redige una ricetta bianca (come faceva prima della REVG). Sarà il Farmacista a dover compilare una sezione del sito segnalando la dispensazione in urgenza con ricetta bianca.
Nota: ad oggi, tale sezione sul sito Vetinfo.it non è ancora presente (nc…).
Si, essendo la cannabis medica uno stupefacente in sez. B, dal 27 Settembre 2022 serve la ricetta elettronica veterinaria galenica (REVG).
Pure il CBD (cannabidiolo), che non è stupefacente, può essere prescritto SOLO con ricetta elettronica Veterinaria galenica.
Si, assolutamente. A maggior ragione dato che il potassio bromuro NON è stupefacente (indipendentemente dall’attività che esplica) non essendo classificato in nessuna delle 5 sezioni (A, B, C, D, E) della Tabella dei Medicinali.
Pertanto, si prescrive con una REVG.
Quali sono le farmacie galeniche di Farmagalenica che preparano farmaci veterinari Galenici? Cercale sul motore di ricerca Cercagalenico.it (si aprirà una nuova pagina).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Ricetta elettronica veterinaria galenica: istruzioni e stupefacenti sembra essere il primo su Farmagalenica.
]]>L'articolo Cannabis per cane e gatto e CBD uso veterinario in Farmacia sembra essere il primo su Farmagalenica.
]]>In questo articolo andremo quindi a vedere come è possibile ottenere in Italia cannabis per cane e gatto, ma non solo (potenzialmente qualsiasi animale), come va prescritta, quali sono gli usi, dove acquistarla, avvertenze e costi.
Non solo, ma si parlerà anche del CBD uso veterinario (cannabidiolo uso veterinario), cannabinoide non psicotropo che mostra sempre più interesse anche su affezioni per animali.
Nota: non stiamo parlando di una cannabis utilizzabile solo da cani e gatti, ma della cannabis farmaceutica che, anzichè essere prescritta ad un essere umano, è prescritta ad un animale.
Alcune informazioni essenziali sulla cannabis terapeutica in Italia
Sulla cannabis terapeutica, Farmagalenica ha già scritto molti articoli negli anni passati, essendo stato uno dei primi blog ad occuparsene dal 2013.
Se quindi volete approfondire lo scenario italiano della cannabis terapeutica consigliamo la lettura di questi articoli:
- varietà di cannabis prescrivibili in Italia e forme farmaceutiche
- l’olio di cannabis
- la cannabis italiana
- la cannabis light
- domande frequenti (FAQ) sulla cannabis terapeutica
Infine, per un migliore e completo approfondimento, è consigliata la lettura del seguente PDF redatto dal Dr. Marco Ternelli, una guida completa all’uso della cannabis medica in Italia:
È davvero possibile prescrivere cannabis per cane e gatto?
Senza voler “annoiare” con i dettagli della normativa, per i più tecnici e curiosi, la normativa che permette al Veterinario la prescrizione di cannabis terapeutica è l’art. 10, c. 1 del Dlgs 193/2006, ossia la cosiddetta cascata prescrittiva.
L’ultimo punto di tale articolo recita infatti che, in mancanza di un farmaco industriale disponibile per l’animale, il Veterinario può prescrivere
in mancanza dei medicinali di cui alla lettera b), con un medicinale veterinario preparato estemporaneamente da un farmacista in farmacia a tale fine, conformemente alle indicazioni contenute in una prescrizione veterinaria.
art. 10 c. 1 l. c Dlgs 193/2006
Attenzione: tale parte si rivolge solo agli animali nDPA cioè non destinati all’alimentazione umana (cani, gatti, tartarughe, pesci, equidi non da alimentazione, ecc…), ma NON è consentito per ora, la prescrizione di cannabis uso veterinario o CBD ad uso veterinario ad animali DPA produttori di alimenti(ovini, suini, bovini, ecc…) poiché non si trova compresa negli allegati I, II, e III del regolamento (CEE) n. 2377/90 (art. 11, c. 2 del Dlgs 193/2006). Su tale argomento è intervenuto anche il Ministero della Salute con nota 0012770-14/05/2019 che ne ribadisce il divieto.

L’articolo ora si divide in 2 sezioni distinte:
- cannabis uso veterinario
- CBD uso veterinario
CANNABIS USO VETERINARIO
Come è compilata una ricetta di cannabis per cane e gatto uso veterinario?
Informazioni per il Medico Veterinario
Alcune premesse importanti sulla ricetta di cannabis uso veterinario:
- la ricetta medica cannabis a pagamento può essere redatta da QUALSIASI Medico iscritto all’Ordine dei Veterinari
- all’interno di ogni facsimile e esempio di ricetta, sono riportate anche le istruzioni per la compilazione corretta
- non ci sono limiti quantitativi o di durata della terapia: può essere prescritto qualsiasi quantitativo per una durata qualsiasi (es. 2 mesi, 6 mesi, ecc…): questo perché la cannabis è un farmaco stupefacente in sez. B e non in sez. A.
- a differenza della prescrizione ad uso umano, le ricette di cannabis uso veterinario NON seguono la Legge 94/98 (Legge “Di Bella”), essendo essa riferita alle preparazioni ad esclusivo uso umano.
Quando il medico Veterinario vuole prescrivere cannabis uso veterinario deve:
- acquisire il consenso informato del paziente: NON obbligatorio per la normativa in se (ricordiamo che la Legge 94/98 non è valida in campo veterinario). Informazioni sul consenso informato sono qui, mentre un facsimile può essere scaricato da qui.
- redigere la ricetta medica cannabis sulle base delle indicazioni Ministeriali, utilizzando per semplicità i facsimile e gli esempi disponibili in questo articolo.
- Per ulteriori informazioni, fare riferimento alla seguente pagina sul sito del Ministero della Salute.
Formalismi della ricetta di cannabis uso veterinario
La ricetta medica di cannabis uso veterinario deve riportare tutti i seguenti formalismi:
- nome e cognome del proprietario dell’animale
- indirizzo completo del proprietario dell’animale
- specie dell’animale (es. cane, gatto, ecc…)
- data di redazione della ricetta medica di cannabis uso veterinario
- timbro (o carta intestata) e firma del medico Veterinario
- prescrizione della sostanza incluso il titolo, tra i vari disponibili (es. Cannabis flos 22% THC – 50 mg). L’indicazione del marchio di cannabis AD OGGI (Bedrocan, Bediol, Bedica, FM2, Pedanios, eccetera) è obbligatoria quando non è possibile identificare con certezza una varietà (es. Bediol o FM2); è facoltativa invece, quando non vi è alcun dubbio circa la varietà di cannabis prescritta dal Medico (es. Cannabis 14% si riferisce solo al Bedica).
- forma farmaceutica: cartine / filtri / bustine / soluzione oleosa / capsule apribili per tisana / tintura / collirio / eccetera
- il numero di dosi (es. 10 cartine) o la quantità (es. 50 ml)
- posologia (è obbligatoria in quanto trattasi di prescrizione in deroga ad animale da compagnia, es. cane o gatto).
È fortemente consigliato, solo ed esclusivamente nel caso di prescrizione di estratti (olio, resine, creme, ecc…) che il medico riporti la posologia in mg di THC o mg di CBD, NON in gocce o ml, lasciando al Farmacista il compito di convertire la dose di THC o CBD nel corrispondente numero di gocce o ml in base al reale contenuto dell’estratto. motivazione della prescrizione o “esigenza di trattamento” (DM 9 novembre 2015), NON ci vuole alcune “motivazione della prescrizione” non essendo la ricetta uso veterinario soggetta alla Legge 94/98 (Legge “Di Bella”).
La ricetta di cannabis ad uso veterinario DEVE essere cartacea in quanto stupefacente, NON REV.
Tabella 5 della FU ITALIANA XII edizione
E il Farmacista? Che fa il Farmacista?
Ogni ricetta medica cannabis ha una validità temporale di 30 giorni escluso quello di redazione e il Farmacista ha l’obbligo (DM 9 novembre 2015) di consegnarne una copia timbrata, datata e firmata dal Farmacista.
Nota: a differenza di quanto deve fare per le ricette ad uso umano, il Farmacista NON deve inviare copia della ricetta medica cannabis all’AUSL, poiché non segue la Legge 94/98 (Legge “Di Bella”).

Quali forme farmaceutiche sono prescritte nella cannabis uso veterinario?
Va detto che la cannabis può essere prescritta in tantissime forme farmaceutiche (leggere questo articolo), ma la più prescritta dai Medici Veterinari in assoluto è l’olio di cannabis:
- pronto all’uso (la cannabis è già decarbossilata dal Farmacista nel Laboratorio Galenico della Farmacia)
- facile da somministrare (gocce)
- accettato dall’animale (l’olio può piacere o comunque si maschera facilmente negli alimenti)
- precisione del dosaggio, in base al numero di gocce: dato che i pesi degli animali da compagnia possono essere anche di pochi Kg, è importante avere un farmaco che sia estremamente scalabile.
In pratica, l’olio di cannabis uso veterinario è un farmaco pronto all’uso: il proprietario dell’animale esce dalla Farmacia con il farmaco in mano e può immediatamente e facilmente somministrarlo all’animale, che lo accetterà sia come sapore che forma di somministrazione.
È impensabile di somministrare cannabis per cane e gatto tramite vaporizzazione o tisana!
Come utilizzare l’olio di cannabis uso veterinario?
La classica prescrizione è solitamente è in rapporto 1:10 tra grammi di cannabis infiorescenza e millilitri di olio.
Dr. Marco Ternelli
Ad esempio, nella prescrizione di cannabis per cane e gatto, si possono avere prescrizioni tipo
- 2 grammi di cannabis in 20 ml di olio (circa 560 gocce)
- 3 grammi di cannabis in 30 ml di olio (circa 840 gocce)
- 5 grammi di cannabis in 50ml di olio (circa 1400 gocce)
Il rapporto è sempre 1:10 in tutti gli esempi; cambia solo il numero di gocce totali. Ma nulla vieta al Medico Veterinario di prescrivere in un rapporto diverso, esempio 5 grammi in 100 ml (anzichè 50ml) ottenendo, in questo caso, un olio maggiormente diluito.
Per quali indicazioni viene utilizzata la cannabis per cane e gatto?
La cannabis uso veterinario per piccoli animali viene prescritta (fonte: EBM) solitamente per
- artrosi
- deficit cognitivi in animali anziani
- ictus
- malattie neurologiche
- nevriti
- ansia/stress
- diabete
- epilessia
- tumori
- dermatiti
- patologie tratto gastrointestinale
- osteoporosi
- malattie autoimmuni
- epilessia
oltre a qualsiasi altra indicazione “al fine di evitare all’animale evidenti stati di sofferenza” (art. 10 c. 1 l. c Dlgs 193/2006).
Quali tipo di cannabis (varietà) sono prescritte maggiormente nella cannabis uso veterinario?
Certamente il Bedrolite/Aurora (< 1% THC e 9% CBD) sono le varietà maggiormente prescritte dai Veterinari (fonte: ricette mediche trienno 2015-2018 presso Farmacia T.) che desiderano ottenere preparazioni galeniche ricche di CBD; segue subito dopo il Bediol/FM2 nel caso si voglia un olio di cannabis uso veterinario che contenga sia THC sia CBD.
Ovviamente, il Veterinario è libero di prescrivere qualsiasi varietà ritenga adatta al caso in questione.
Qual è la posologia per l’olio di cannabis per cane e gatto o comunque ad uso veterinario?
3 regole d’oro fondamentali:
- il Medico Veterinario è l’unico che può definire qual è la corretta posologia e dosaggio di cannabinoidi.
- si inizia SEMPRE e solo con 1 goccia, prima ancora di definire un dosaggio di THC o CBD a cui arrivare
- start low, go slow (iniziare bassi, incrementare lentamente)
Detto questo, la classica posologia che molti Veterinari utilizzano è di somministrare l’olio di cannabis 2 volte al giorno (ogni 12 ore), anche se ci sono casi di 3 somministrazioni giornaliere (fonte). Possibilmente a stomaco vuoto e quindi lontano dai pasti.
Per il numero di gocce, si inizia sempre da 1 goccia per somministrazione, incrementando ogni giorno o, se l’animale mostra effetti collaterali, ogni 2 o 3 giorni.
Si prosegue fino a raggiungimento di un risultato terapeutico soddisfacente.
Consigli per la somministrazione di olio di cannabis ad uso veterinario
Le Farmacie Galeniche forniscono l’olio di cannabis in un flacone con contagocce. Si tratta di gocce oleose che, come già scritto, possono essere costituite da un qualsiasi olio alimentare si desideri: oliva, soia, arachidi, mais, MCT, ecc…
Sebbene la via più in uso negli essere umani sia la via sublinguale, negli animali questo può essere difficoltoso (pensata al gatto…). Il consiglio è di porre le gocce in pochissimo cibo e fare ingoiare/mangiare il tutto all’animale: evitare di disperdere le gocce in molto cibo, altrimenti il rischio è che l’animale tralasci del cibo, insieme al farmaco in esso contenuto.
Dosaggi del THC nei piccoli animali
Per concludere questa sezione, alcune indicazioni esperienziali sull’uso del THC da cannabis terapeutica ad uso veterinario sono i seguenti:
- 0,1 – 0,25 mg/kg di THC al giorno, da suddividere in 2 o più somministrazioni
- aumentare la dose in media ogni 3 giorni
- non incrementare più di 0,25/0,5mg/kg per volta
CBD USO VETERINARIO
Come è compilata una ricetta di CBD uso veterinario?
Informazioni per il Medico Veterinario
Alcune premesse importanti sulla ricetta medico veterinaria di CBD uso veterinario:
- il CBD non è ad oggi un principio attivo stupefacente e psicotropo
- per questo va redatta con la Ricetta Elettronica Veterinaria Galenica (REV o REVG)
- la ricetta medica di CBD uso veterinario può essere redatta da QUALSIASI Medico iscritto all’Ordine dei Veterinari
Formalismi della ricetta di cannabis uso veterinario
La ricetta medica di CBD uso veterinario deve riportare tutti i seguenti formalismi (che la REV, per la maggior parte, inserisce automaticamente):
- nome e cognome del proprietario dell’animale
- indirizzo completo del proprietario dell’animale
- specie dell’animale (es. cane, gatto, ecc…)
- data di redazione della ricetta medica di cannabis uso veterinario
- timbro (o carta intestata) e firma del medico Veterinario
- prescrizione della quantità di CBD (cannabidiolo) in mg o % a seconda del tipo di preparazione.
- forma farmaceutica: cartine / filtri / bustine / soluzione oleosa / capsule apribili per tisana / tintura / collirio / eccetera
- il numero di dosi (es. 10 capsule) o la quantità (es. 50 ml)
- posologia (è obbligatoria in quanto trattasi di prescrizione in deroga ad animale da compagnia, es. cane o gatto).
Dosaggi del CBD uso veterinario
Posto che il CBD (cannabidiolo) funziona in maniera diversa a seconda della sensibilità e tolleranza dell’animale, alcune indicazioni esperienziali e da letteratura sui dosaggi (si ripete: indicativi) del CBD uso veterinario per cane e gatto possono essere le seguenti.
Cane
- 0 – 9 kg: 2,5 mg a salire due volte al giorno
- 9 – 20 kg: 5 mg a salire due volte al giorno
- 20 – 35 kg: 10 mg a salire due volte al giorno
- 35 – 50 kg: 15 mg a salire due volte al giorno
- oltre 50 kg: 20 mg a salire due volte al giorno
Gatto
- 1,0 mg a salire una volta al giorno
Dove lavorano i Veterinari che prescrivono ricette di cannabis uso veterinario o CBD uso veterinario?
Prima di tutto occorre ricordare che qualsiasi Veterinario può redigere una ricetta cannabis medica uso veterinario, ma non è obbligato poiché un Medico Veterinario può prescrivere un farmaco solo se, in scienza e coscienza, ritiene sia necessario al trattamento della patologia del paziente.
Ricorda: un Medico non è mai obbligato a prescrivere un farmaco, cannabis o non cannabis.
Non è possibile, per motivi legali, indicare in questo articolo dove e quali Veterinari prescrivono la cannabis medica in Italia. Possiamo però segnalare:
- contattare delle Farmacie che fanno galenica e chiedere, singolarmente, se hanno dei nominativi di Medici o conoscono centri specialistici in cui viene utilizzata la cannabis medica
- usare Google, Duckduckgo, Bing, Yahoo come motori di ricerca per trovare medici che prescrivono cannabis terapeutica
- registrarsi su www.letsweed.com e vedere se sono reperibili nominativi di Medici
- chiedere su Facebook e altri social ad altri pazienti
Infine, ricordiamo che per conoscere quali sono le Farmacie di Farmagalenica in grado di vendere prodotti a base di Cannabis Sativa L., consultare il motore di ricerca cercagalenico.it (si aprirà una nuova pagina).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Cannabis per cane e gatto e CBD uso veterinario in Farmacia sembra essere il primo su Farmagalenica.
]]>L'articolo Cannabis medica FM2 FM1: guida completa sembra essere il primo su Farmagalenica.
]]>
Articolo aggiornato profondamente rispetto alla versione originale.
Da quanto la cannabis è diventata legale ad uso terapeutico nel 2013, uno degli ostacoli più grandi lamentati dai pazienti e associazioni è stato il prezzo: chi diceva che si pagava 35€ al grammo, chi 40€, chi 50€, chi 80€, eccetera.
Posto che agli inizi 2013 (appena diventata legale ad uso terapeutico), la cannabis aveva davvero un prezzo di 35€/grammo (mai 40€), ad oggi importi del genere sono legati o a (voluta) disinformazione o situazioni episodiche disdicevoli. Il Farmacista NON può scegliere liberamente a quale prezzo vendere un farmaco galenico (qualsiasi, non solo i farmaci a base di cannabis), ma deve sottostare a una Tariffa Nazionale dei Medicinali che ne impone la vendita a 9€/grammo + costi di preparazione + IVA 10%.
Chiarito il concetto che “1 grammo di cannabis” non vuol dire nulla (si legga l’articolo dedicato), vediamo a metà 2018 quali varietà di cananbis sono legali in Italia:
- cannabis Olandese (Bedrocan, Bediol, Bedrobinol, Bedica, Bedrolite).
- cannabis Canadese Pedanios (Pedanios 22/1, Pedanios 8/8, Pedanios 1/9).
- la “cannabis di stato” o “cannabis italiana” o “cannabis dei militari” o “cannabis FM2” (titolata al 5-8% THC e 7-12%CBD), prodotta a Firenze dall’Istituto Farmaceutico Militare è acquistabile in farmacia da Gennaio 2017.
- la “cannabis di stato” o “cannabis italiana” o “cannabis dei militari” o “cannabis FM1″ (titolata al 13-20% THC e <1%CBD), prodotta a Firenze dall’Istituto Farmaceutico Militare sarà acquistabile in farmacia a partire da Luglio 2018.
Cannabis FM1? Ma non si era sempre parlato di Cannabis FM19?
Corretto. La FM19 era stata così chiamata al tempo (2014), per affiancarla a quello che era il Bedrocan 19% (poi divenuto Bedrocan 22%).
La cannabis FM19 fu la prima ad essere coltivata e le cronache racconti di problemi nella produzione per i quali fu necessario distruggere i raccolti a passare alla coltivazione della cannabis FM2.
A Luglio 2018, la FM19 ritorna “trasformata” in FM1 (riferendosi ad 1 principio attivo, il THC) con un tenore di THC medio alto (v. oltre).
Qual è il prezzo cannabis nelle Farmacie galeniche italiane?
OLANDESE: la cannabis olandese viene acquistata dalle Farmacie Italiane ad un prezzo che varia dagli 8€ ai 10€ + IVA 22% al grammo (ossia dai 9.76€ ai 12.2€ IVA INCLUSA).
In base alla Tariffa Nazionale dei Medicinali è di 9€/grammo + IVA 10% (+ costi di preparazione e supplementi).
ITALIANA: il prezzo cannabis è unico e preciso: viene stabilito (Nota del Ministero QUI) che il prezzo di vendita dello Stabilimento Farmaceutico Militare di Firenze a Farmacie, AUSL e Ospedali è di 6.88€ + IVA 22% = 8.39€ (+ 15/20/25€ fissi di spese di spedizione). NON è il prezzo di vendita al PUBBLICO, ATTENZIONE! Continuare a leggere!.
Diversamente da quanto si diceva in interviste passate, infatti, sarà lo Stabilimento Farmaceutico Militare di Firenze a vendere direttamente, SENZA passare da intermediari. Questo incide sul prezzo finale? Si.
Ora, la cannabis FM2 terapeutica è venduta direttamente come materia prima dallo Stabilimento Farmaceutico Militare alla Farmacia. Questo vuol dire che dopo l’approvazione del DM del 23 Marzo 2017, dal 18 Giugno 2017 la cannabis infiorescenze è stata inserita nell’Allegato A della Tariffa Nazione dei Medicinali e verrà venduta al prezzo di 9€/grammo (9€ + IVA 10%).
Quali sono i costi sostenuti dalle AUSL o Ospedali per l’importazione diretta della cannabis olandese?
Normalmente sono tra i 5-6€/grammo + IVA 22%.
Si chiarisce ancora: sono i costi per l’acquisto diretto da parte di AUSL e Ospedali, non da parte di pazienti o farmacie.
Che aspetto ha la cannabis FM2 terapeutica italiana dell’Istituto Farmaceutico Militare?
La cannabis FM2 viene definita dal Ministero come
“costituita da infiorescenze femminili non fecondate, essiccate e macinate con granulometria inferiore a 4 mm”
L’aspetto è il seguente:

Viene fornita in barattoli bianchi da 5 grammi che NON possono mai essere dispensati direttamente al paziente, ma vengono impiegati dal Farmacista per la preparazione di farmaci galenici.
La concentrazione di principi attivi è:
- THC: range che va dal 5% al 8%
- CBD: range che va dal 6.5% al 12%
Si presta quindi ad essere un similare (!) di varietà come il Bediol (olandese) o Pedanios 8/8 (Canadese).
Che aspetto ha la cannabis FM1 terapeutica italiana dell’Istituto Farmaceutico Militare?
La cannabis FM1 viene definita come infiorescenze, macinati, quindi NON sono fiori interi.
L’aspetto è il seguente:
Il primo lotto venduto alle Farmacie ha scadenza Ottobre 2018.
Come la FM2, anche la FM1 viene fornita in barattoli bianchi da 5 grammi che NON possono mai essere dispensati direttamente al paziente, ma vengono impiegati dal Farmacista per la preparazione di farmaci galenici.
La concentrazione di principi attivi è:
- THC: range che va dal 13% al 20% (valore medio stimato 14-15%)
- CBD: < 1%
Si presta quindi ad essere un similare (!) di varietà come il Bedica (olandese). E per quanto riguarda il Bedrocan? Può essere considerata similare? In teoria no, in pratica possono esserci sovrapposizioni (es. un Bedrocan 19% e una FM1 18%), ovviamente se si guarda solo il THC e si esclude la genetica, profilo terpenico, eccetera.
Quali sono i TEMPI di approvvigionamento della cannabis?
OLANDESE: se parliamo di farmacie “rifornite”, normalmente in pochi giorni/settimana è possibile ottenere la preparazione.
I grossisti e gli ospedali che si devono invece approvvigionare dall’Olanda, possono richiedere 1-2 mesi di attesa a seconda della DISPONIBILITA’.
Va però detto anche che ormai ci sono Farmacie che dispongono di ampi quantitativi di scorte di cannabis terapeutica ed è quindi impossibile rimanerne sprovvisti: i pazienti devono solo cercare la Farmacia con scorte, ad esempio tramite il motore di ricerca galenico Cercagalenico.it (si aprirà una nuova finestra).
ITALIANA: come precedentemente scritto, lo Stabilimento Farmaceutico militare dichiara che in caso di DISPONIBILITA’, la cannabis FM2 e FM1 farmaceutica viene fornita in circa 15 giorni lavorativi alla Farmacia/Ospedale. Se non disponibile, possono passare anche diversi mesi di attesa.
La cannabis FM2 e cananbis FM1 terapeutica italiana potrà essere usata solo per le prescrizioni SSR (gratuite) o anche nelle prescrizioni a pagamento? Solo per cartine o anche per estratti o altro?
Come per la cannabis olandese e canadese, la FM2 potrà essere usata sia per la preparazione di galenici a pagamento che rimborsati dal SSR (in quest’ultimo caso però, ogni singola Regione deciderà autonomamente).
E potrà essere usata per la preparazione di cartine, oli, resine, ecc… esattamente come la cannabis olandese.
Molte testate giornalistiche scrivono che con la cannabis FM2 e FM1 di “Stato” le regioni cominceranno a permetterne la distribuzione nelle Farmacie. Ma non era già così?
Si, infatti. Si tratta di errori da parte dei giornalisti che (probabilmente) confondo la distribuzione della cannabis a pagamento tramite le farmacie (che già avviene dal 2013) con la distribuzione a carico SSR (che pure avviene da qualche mese in pochissime Regioni) e che partirà in ulteriori Regioni da quando sarà disponibile la cannabis FM2.
Che ricetta serve per poter ottenere cannabis FM2 e FM1 terapeutica?
Le modalità di prescrizione per ottenere cannabis FM2 o cannabis FM1 dello stabilimento Farmaceutico Militare di Firenze sono IDENTICHE a quelle della cannabis olandese, cambia solo il nome.
Questo significa che:
- per la prescrizione a pagamento (su ricetta bianca) di cannabis FM2 o FM1, il medico può scaricare i facsimile dedicati in questa pagina, sostituendo solamente il nome della cannabis Olandese (es. Bediol) con quello della varietà italiana (FM2 o FM1) e relative percentuali di THC/CBD.
- per la prescrizione a carico SSR nelle regioni in cui già era già rimborsata la cannabis olandese, le ricette vengono redatte alla stessa maniera, sostituendo solamente il nome della cannabis Olandese (es. Bediol) con quello della varietà italiana (FM2 o FM1) e relative percentuali di THC/CBD.
———————
A firma del Dr. Marco Ternelli, si rende disponibile al download una scheda riepilogativa sulla Cannabis terapeutica in Italia, incluso un appendice con tabelle di equivalenze tra olio, milligrammi e gocce.
Clicca QUI per scaricare il PDF gratuitamente.
———————
Ulteriori informazioni sulla cannabis ad uso medico possono essere reperite sul sito del Ministero della Salute e dello Stabilimento Chimico Farmaceutico Militare di Firenze.
Per cercare e visualizzare l’elenco completo delle Farmacie di Farmagalenica in grado di allestire preparazioni a base di cannabis (marijuana) terapeutica consultare il motore di ricerca Cercagalenico.it (si aprirà una nuova finestra).

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Cannabis medica FM2 FM1: guida completa sembra essere il primo su Farmagalenica.
]]>L'articolo Cannabis light (canapa legale): in Farmacia non si può? sembra essere il primo su Farmagalenica.
]]>Per chi ha fretta
- la cannabis light (canapa legale non stupefacente) non è legale ad uso terapeutico
- non è possibile coltivare canapa e rivenderla alle farmacie affinché ne facciano farmaci galenici
- le farmacie non possono utilizzare cannabis light (canapa legale) per effettuare preparazioni galeniche
- le infiorescenze di cannabis light sono “legali” solo ad uso tecnico R&D, ad eccezione dei semi; non può essere somministrata ad essere umani (uso interno/esterno)
- l’unica cannabis (ad oggi) legalmente vendibile ed utilizzabile in Farmacia è cannabis medica di grado farmaceutico (GMP), che soddisfi i requisiti della monografia di una farmacopea di un paese dell’UE (attualmente, quella tedesca) ossia sia classificata come farmaco
- prima o poi, la vendita di canapa light e relativi prodotti con CBD verrà bloccata o ridimensionata (v. oltre).
Per chi ha tempo 
Prima di iniziare diamo un po’ di definizioni, per capire gli argomenti trattati sulla cannabis light:
- Cannabis Sativa L.: è il nome botanico latino e scientifico della pianta, indipendentemente che sia uso ludico, medico, tecnico, alimentare, industriale che sia.
- canapa legale: conosciuta anche come canapone, è il termine con il quale ci si riferisce a Cannabis Sativa L. con contenuto di THC < 0,2% e quindi non è considerata stupefacente. La canapa legale è destinata all’uso industriale, tecnico, alimentare, tessile, ecc… Il limite di THC è tollerato fino allo 0.6% nelle analisi eseguite sulla coltivazione.
- cannabis light: è un slang inglese con cui ci si riferisce alla canapa legale di cui sopra. Niente di più.
- cannabis medica: è la Cannabis Sativa L. coltivata in GACP (Good Agricolture and Collection Practice) e GMP (Good Manufacturing Practice) mediate clonazione, in serre indoor e con metodica di germinazione riportata nel DM 9/11/15. Può contenere o meno THC, è standardizzata nel contenuto di alcuni cannabinoidi (es. THC, CBD, CBN) ed è di grado farmaceutico, destinata ad uso terapeutico.
Infine, ricordiamo che le parti vegetali della cannabis sono:
- infiorescenze (maschile/femminile)
- foglie
- gemme
- semi
- stelo/fusto
- radici
Quale cannabis può essere venduta in Italia ad uso medico/terapeutico?
Solo ed esclusivamente la cannabis medica, mediante ricetta medica e solo tramite le Farmacie. Tutta la cannabis medica, indipendentemente dal livello di THC è considerata stupefacente (es. Bedrolite che contiene solitamente lo 0,4% di THC è stupefacente).
Può essere prescritta e venduta come farmaco in virtù della legge Di Bella artt. 4 e 5 , dal fatto che soddisfa i requisiti della monografia della Farmacopea Tedesca e dal fatto che è coltivata in GAP e prodotta in GMP (oltre ad essere autorizzata dal Ministero della Salute).
Per approfondimenti, c’è un articolo dedicato.
Quale cannabis può essere venduta in Italia ad uso alimentare?
In Italia esiste una lista redata dal Ministero della Salute di piante che possono essere usata dall’industria degli integratori e/o dei prodotti erboristici (tisane, estratti, ecc…), ossia prodotti destinati all’assunzione umana; in tale lista sono presenti tutte le centinaia di piante che possiamo trovare in farmacia, erboristeria, negozi, supermercati e nei prodotti che le contengono. Tale lista è detta “lista positiva” o “delle piante ammesse“ e in essa compare la Cannabis sativa L. (!) seme e olio.
Questo vuol dire che l’unica parte utilizzabile per realizzare questi prodotti (erboristici o alimentari) sono il seme di canapa e l’olio di canapa (ottenuto dalla torchiatura del seme, non è l’olio di cannabis terapeutico).
Si può quindi usare la canapa infiorescenze per fare tisane, integratori, alimenti?
NO, perché non nella lista delle piante ammesse
Si può usare la canapa semi per fare tisane (?), integratori, alimenti (es. farina)?
SI, perché presente nella lista delle piante ammesse
NON SONO QUINDI UTILIZZABILI LE INFIORESCENZE DI CANAPA AD USO ALIMENTARE/ERBORISTICO, anche se a titolo < 0,2% THC (e ci mancherebbe, altrimenti il problema sarebbe altro), da vendere come tali in tisana, ecc…
È invece legale (ripetiamolo per l’ultima volta) vendere le parti (e i derivati) indicate nella lista: semi di canapa ad uso alimentare, perciò olio da semi, farine da macinatura dei semi, prodotti a base di farina di semi di canapa.
Come si spiega la vendita delle infiorescenze di “cannabis light” se non è utilizzabile?
Attenzione: “non utilizzabile” (terapeuticamente) non significa “non vendibile”.
Doverosa precisazione prima di continuare: la vendita della cannabis light o canapa legale a contenuto di THC < 0,2%, è possibile dal 1990 ossia da quando è stato regolamentata la coltivazione di cannabis industriale, stabilendo il limito entro il quale il coltivatore non era perseguibile con l’accusa di coltivazione di sostanze stupefacenti.
Perchè torna ora in auge? Sono cambiati i tempi? È il momento giusto culturalmente? È business? È alternativa alla carenza di cannabis medica?
La risposta alla domanda iniziale è: la canapa legale (cannabis light) non è classificata stupefacente in quanto ha contenuto di THC < 0,2% e può essere venduta in quanto classificata per uso tecnico (o R&D, Research and Development), identificato anche da frasi tipo uso esterno o non fumabile / non vaporizzabile.
La destinazione “uso tecnico” di un prodotto (sostanza chimica, materia prima) significa che quel prodotto, che potrebbe anche essere indicato ad essere somministrato nell’organismo umano (sia uso interno che esterno), NON è adatto ad essere somministrato (ingerito o applicato sulla cute) nell’uomo.
Un prodotto USO TECNICO non è adatto/consentito alla somministrazione umana? Perchè:
- non deve rispondere ai limiti di sicurezza rispetto alla stessa materia prima di grado alimentare o farmaceutico
- può contenere contaminanti o sostanze potenzialmente pericolose
- non deve essere necessariamente puro
Facciamo alcuni esempi con la Cannabis Sativa L. per capire.
Contenuto in muffe o batteri
Cannabis medica: deve OBBLIGATORIAMENTE avere valori inferiori a 10 UFC (Unità Formanti Colonie), ossia quasi sterile (nel senso, incontaminata).
Canapa ad uso tecnico: potenzialmente nessun limite (può essere quindi contaminata).
Contenuto in metalli pesanti
Cannabis medica: deve OBBLIGATORIAMENTE avere valori inferiori a determinati ppm (Parti Per Milione).
Canapa ad uso tecnico: potenzialmente nessun limite (può essere quindi contaminata da metalli pesanti)
Nota: va ricordato che la cannabis è una formidabile “spugna” (chelante) di metalli pesanti, che assorbe dalle radici e concentra in un punto specifico… le infiorescenze!
Contenuto in aflatossine
Cannabis medica: deve OBBLIGATORIAMENTE avere valori inferiori a determinati valori, stabiliti sicuri per la salute umana.
Canapa ad uso tecnico: potenzialmente nessun limite (può essere quindi contaminata).
Concludendo:
Stiamo forse dicendo che si potrebbe coltivare canapa legale su un terreno contaminato (es. di fianco all’Ilva di Taranto?), raccoglierla, conservarla in ambienti non salubri, e venderla come uso tecnico? ESATTAMENTE.
Qual è il senso dell’uso tecnico per la canapa legale? Almeno c’è il CBD (cannabidiolo)
Essendo classificata ad uso tecnico (e con contenuto di THC < 0,2%) diviene legale fornire il prodotto, che non può assolutamente avere alcuna indicazione terapeutica o claim salutistico. Nel primo caso si configurerebbe come farmaco (reato), nel secondo in multe amministrative salatissime.
Trattandosi di uso tecnico, possono essere vendute TUTTE le parti della pianta: ecco perché è possibile trovare un prodotto fatto con infiorescenze, semi e foglie.
La canapa legale o cannabis light ad uso tecnico rappresenta una fonte di approvvigionamento di CBD (cannabidiolo) che è una sostanza definita come materia prima cosmetica e materia prima farmaceutica essendo presente in un farmaco a base di THC/CBD (nabiximols) e, a breve, in un farmaco a base di CBD per il trattamento dell’epilessia farmacoresistente.
Cosa si vuole dire? Che indipendentemente che parliamo di cannabis medica, cannabis light o farmaco, il CBD ha una struttura chimica definita ed è sempre lo stesso, presente sempre e comunque.
Di conseguenza, la cannabis light può essere vista come un fonte di approvvigionamento di CBD… con sempre il problema dell’uso tecnico (contaminanti, metalli pesanti, assenza normativa regolatoria specifica, ecc…) che non lo rende quindi legale e legittimo da punto di vista di uso terapeutico.
In un esempio semplice: quale è il senso di “curare” se si può assumere canapa legale con alto contenuto in CBD, ma che potenzialmente porterebbe a vaporizzazione di muffe o ingerire (es.) cadmio?
Come fare a capire la qualità della canapa legale venduta?
Ad oggi, l’unico modo è la serietà/nome della ditta/e coltivatrice/produttrice che può decidere o meno di fornire analisi, certificazioni (rilasciate da?) su coltivazione, produzione e manipolazione, che attestino l’assenza o presenza di inquinanti, pesticidi, metalli pesanti, muffe, batteri presenti.
Ricordando anche che in un certificato ad uso tecnico, la non corrispondenza dei risultati di un test ai valori (arbitrariamente) impostati come limite, non ne esclude la vendibilità.
Alla domanda “è legale comprare canapa legale al grammo, credendo di pagare infiorescenza, invece si tratta di mix di fiori, semi e foglie?” la risposta è sempre una: SI, essendo ad uso tecnico, lo è.
Certamente è possibile per una ditta produrre canapa legale di qualità, ma il problema rimane sempre l’uso tecnico, non terapeutico e l’impossibilità di avere garanzie a priori, ma basate sulla serietà della ditta coltivatrice / produttrice.
Qual è la normativa che regola la vendita di infiorescenze di canapa legale, le etichette, frasi obbligatorie, ecc…?
Non c’è.
Le infiorescenze di canapa legale non rientrano nella definizione di “ad uso alimentare”, quindi non hanno obblighi di seguire la normativa dell’etichettatura degli alimenti.
E non rientrano nella definizione di “integratore”, quindi non hanno obblighi di seguire la normativa dell’etichettatura degli integratori alimentari.
Non rientrano neppure nella definizione di “uso terapeutico” (farmaco), quindi non hanno obblighi di seguire la normativa dell’etichettatura dei farmaci galenici (NBP, Norme di Buone Preparazione).
Questo spiega come mai confezioni di canapa legale riportano informazioni differenti, a volte mancanti rispetto ad altre confezioni di ditte diverse.
E spiega come è possibile che in alcune varietà di canapa non sia neppure riportata la concentrazione di THC dell’infiorescenza: non vi è alcun obbligo (con tutti i rischi che ne derivano): cannabis ad uso tecnico con contenuto > 0.6% THC è 100% illegale in quanto stupefacente.
Una sentenza della Cassazione a Dicembre 2018 ha stabilito che le infiorescenze < 0,2% di THC sono legali, mentre fino allo 0,6% sono solo tollerate, che non vuol dire legale.
Avendo un campo con diversi ettari, posso però coltivare canapa legale e venderla alle farmacie che la “trasformano” in uso terapeutico?
No.
In base a quanto detto, la canapa coltivata sarebbe ad uso industriale e non farmaceutico. Inoltre, per poter coltivare cannabis medica (ad uso terapeutico), la coltivazione deve essere autorizzata dal Ministero della Salute.
Molte farmacie vengono contattate da aziende per propongono la vendita di canapa legale (con THC < 0,2%) come tale o trasformata in “farmaco” ad uso terapeutico nel Laboratorio Galenico della Farmacia.
Non è possibile ne la prima ne la seconda cosa.
La prima, per quanto esposto finora nell’articolo: la canapa legale non può avere proprietà terapeutiche, si tratta di un prodotto ad uso tecnico, non è un prodotto di grado farmaceutico, non soddisfa i requisiti di Farmacopea, non è nella lista delle piante, parti e derivati ammesse.
La seconda (più pericolosa per il Farmacista poco attento): la lavorazione della canapa, anche se a titolo < 0,2% nelle infiorescenze può portare ad ottenere “prodotti” concentrati in THC (es. olio, tinture, edibili) che contengono THC a concentrazioni variabili tipo 0,0002% 0,1%, 0,5%, 1%, ecc… Il fatto che siano presenti anche solo tracce di THC in un prodotto della cannabis, si configura come reato di fabbricazione di sostanze stupefacenti (in quanto il THC è presente in Tabella II della sostanze stupefacenti e psicotrope d’abuso) dato che il limite dello 0,2% vale solo per le infiorescenze.
Un po’ come se nella Coca-Cola ci fosse lo 0,001% di cocaina, sostanza d’abuso.
La farmacia potrebbe vendere la canapa ad uso tecnico in infiorescenze?
Formalmente si. Ma, senza prenderci in giro, ci recheremmo in farmacia ad acquistare un prodotto ad uso tecnico (e che quindi non possiamo usare) sapendo che ci viene venduto (a voce) come terapeutico?
Quello che sarebbe auspicabile sarebbe canapa legale a contenuto in THC < 0,2% di grado farmaceutico GMP (quindi non a uso tecnico), compliant alla Farmacopea Tedesca che sarebbe vendibile in farmacia tale e quale, ma con ricetta medica, dato che sarebbe comunque infiorescenza non presente nella lista positiva, ma che il Medico può prescrivere sempre in base alla Legge Di Bella.

Possiamo fare un riassunto dei vari casi relativi alla Cannabis Sativa L. medica, alimentare, uso tecnico, …?
Certo, eccolo:
- Infiorescenze di Cannabis medica di grado farmaceutico (GMP), stupefacente: vendibili solo in Farmacia, con ricetta medica.
- Infiorescenze di Cannabis medica di grado farmaceutico (GMP), non stupefacente: compliant alla Farmacopea e con status GMP, vendibili con ricetta medica (non ne esistono attualmente), dato che non è nella lista negativa (piante non ammesse).
- Infiorescenze di Cannabis light (canapa legale) per uso alimentare con contenuto THC < 0.2%: non vendibili (non in lista positiva delle piante ammesse)
- Infiorescenze di Cannabis light (canapa legale) per uso terapeutico con contenuto THC < 0.2%: illegale/non esiste.
- Semi di Cannabis light per uso alimentare: vendibili in qualunque esercizio.
- Cannabis light ad uso tecnico (R&D) con contenuto THC < 0.2%: vendibile in qualsiasi esercizio (sconsigliate le Farmacie)
- Cannabis light ad uso tecnico (R&D) con contenuto THC > 0.2%: illegale/non esiste in Italia.
Quale il prossimo futuro per la cannabis light? Cosa aspettarsi dal mercato della canapa legale?
Molto probabilmente o una chiusura totale della vendita o un forte ridimensionamento.
[Edit di Novembre 2020: ci avevamo azzeccato! Se non fosse stato per il Ministro della Salute Speranza che ha sospeso il Decreto 15 Ottobre 2020, quanto previsto sopra si sarebbe avverato.]
Perché?
Perchè sta per entrare in commercio (nei prossimi mesi) un nuovo farmaco industriale (medicinale con AIC) a base di CBD, sciroppo orale registrato per alcune forme resistenti di epilessia.
Quando arriverà in Italia, di fatto il CBD (inteso come molecola, sostanza) diventerà a tutti gli effetti un farmaco: QUALSIASI prodotto contenente CBD sarà considerato farmaco e quindi dovrà essere autorizzato da AIFA (Agenzia Italiana del Farmaco), cosa che però avviene solo per i farmaci industriali.
Da quel momento, tutta la cannabis light non potrà più commercializzata nelle stesse modalità a cui siamo abituati oggi.
Pensiero libero: se foste una industria farmaceutica che ha speso decenni di ricerca per ottenere un farmaco, accettereste l’idea di non venderlo come dovrebbe perché il suo principio attivo è liberamente reperibile altrove? O fareste di tutto per proteggere i vostri investimenti?
Uno scenario meno apocalittico sarebbe se in concomitanza all’uscita del suddetto medicinale, venissero regolamentati i dosaggi di CBD, ossia si definisse a quali dosaggi il CBD viene considerato farmaco (caso sopra) e quando no, permettendo la commercializzazione di CBD come integratore, alimento, ecc.
In altre parole, potrebbe succedere che:
- fino a un certo dosaggio (es. < 10% CBD) l’infiorescenza è considerata alimento o integratore ed è acquistabile liberamente.
- oltre un certo dosaggio (es. > 10% CBD) l’infiorescenza è considerata farmaco ed è acquistabile solo con ricetta.
Cosa si intende per uso tecnico?
Inoltre, queste immagini sono eloquenti per capire perchè la cannabis light e CBD non possono durare per come li conosciamo ora:
- viene dichiarato che per studi fatti finora (quali?) non ci sono effetti collaterali. Falso, c’è addirittura un medicinale a base di CBD che ha il suo foglietto illustrativo con effetti collaterali molto comuni, comuni, non comuni, rari, rarissimi.
- vengono elencate proprietà terapeutiche a qualcosa che non è farmaco registrato con AIC (Autorizzazione all’immissione in commercio), che è un reato (!)
- tutto questo detto, avendo elencato le notevoli proprietà, nel retro dello stesso volantino viene dichiarato ad uso tecnico e di laboratorio per agricoltori e università. Quindi solo per gli agricoltori e universitari funziona?

Aggiornamento Giugno 2018: come aveva ampiamente anticipato la dichiarazione del Dr. Ternelli Marco, esce la notizia che il Consiglio Superiore di Sanità raccomanda di vietare la vendita della cannabis light in quanto potenzialmente pericolosa.
Aggiornamento Ottobre 2018: presentata una ricerca scientifica sul fatto di come la cannabis light possa essere lavorata per estrarre dosi “elevate” di THC. La strada si apre…
Aggiornamento Dicembre 2018: come previsto, ulteriore tassello sul CBD = farmaco. La FDA americana sta valutando la legittimità di utilizzare THC e CBD negli alimenti o integratori perché “se sono farmaci, non sono alimenti o integratori” ergo, non possono contenere CBD o THC.
Aggiornamento Febbraio 2019: vietata la vendita di CBD in Austria.
Aggiornamento Maggio 2019: ed eccoci al climax, la Cassazione vieta la vendita di cannabis infiorescenze e derivati (oli, resine, ecc…) se aventi effetto drogante (0.5% THC? Interpretazioni?). Non dite che non l’avevamo detto…
Aggiornamento Ottobre 2020: il CBD naturale diventa sostanza stupefacente in seguito alla pubblicazione in Gazzetta Ufficiale del Decreto 15 Ottobre 2020.
Aggiornamento 29 Ottobre 2020: il Ministro Speranza ha SOSPESO (non cancellato) l’entrata in vigore del Decreto 15 Ottobre 2020.
Per ogni domanda, punto non chiaro, richiesta, lasciate un commento nella sezione sottostante.

Farmacista appassionato di Galenica, Legislazione Farmaceutica e Farmaci al banco. Amministratore di Farmagalenica.it, Farmacosmetica.it e Cercagalenico.it.
Nel 2013 si è specializzato in preparazioni galeniche a base di cannabinoidi e cannabis medica e ha conseguito un Master alla Bedrocan BV. Da sempre lavora presso l’omonima Farmacia.
Iscrizione Albo dei Farmacisti
L'articolo Cannabis light (canapa legale): in Farmacia non si può? sembra essere il primo su Farmagalenica.
]]>